
【题目】可用于检测CO的某气敏传感器的工作原理如图所示。下列说法不正确的是

A.工作过程中化学能转化为电能
B.工作一段时间后溶液的pH几乎不变
C.电极I上发生反应:CO - 2e- + H2O = CO2 + 2H+
D.电极II上发生反应:O2 + 2H2O + 4e- = 4OH![]()
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】乙烯的产量是衡量一个国家石油化工水平的重要标志。聚乙烯是以乙烯为原料合成的一种人们常用的高分子材料。下列有关叙述正确的是( )
A.乙烯合成聚乙烯的反应属于化合反应
B.乙烯合成聚乙烯的化学方程式是:nCH2=CH2 ![]()
![]()
C.聚乙烯在自然界中很难降解,容易导致“白色污染”
D.聚乙烯是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,且所含碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图所示:
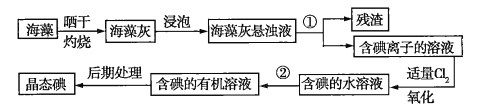
(1)指出制取碘的过程中有关实验操作的名称:①__________,②__________。
(2)操作②中可供选择的有机试剂是_________(填序号)。
A.甲苯、酒精 B.四氯化碳、苯 C.汽油、乙酸 D.汽油、甘油
(3)现需做使海藻灰中的碘离子转化为有机溶液中的碘单质的实验,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、药品,尚缺少的玻璃仪器是__________、___________。
(4)要从碘的苯溶液中提取碘和回收苯,还需要经过蒸馏操作。进行蒸馏操作时,需使用水浴加热,目的是__________,最后晶态碘在________中聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为某城市某日空气质量报告,下列叙述与报告内容不相符的是

A. 该日空气首要污染物是PM10
B. 该日空气质量等级属于中度污染
C. 污染物NO2、CO可能主要来源于机动车尾气
D. PM2.5、PM10指的是悬浮颗粒物,会影响人体健康
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某金属有机多孔材料FJI-H14在常温常压下对CO2具有超高的吸附能力,并能高效催化CO2与环氧乙烷衍生物的反应,其工作原理如图所示。下列说法不正确的是( )
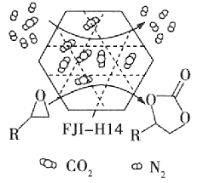
A.该材料的吸附作用具有选择性
B.该方法的广泛使用有助于减少CO2排放
C.在生成 的过程中,有极性共价键形成
的过程中,有极性共价键形成
D.其工作原理只涉及化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中发生如下反应:X(g)+3Y(g) ![]() 2Z(g) ΔH<0,下图表示该反应的速率(v)随时间(t)变化的关系,t1、t3、t4时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中不正确的是( )
2Z(g) ΔH<0,下图表示该反应的速率(v)随时间(t)变化的关系,t1、t3、t4时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中不正确的是( )
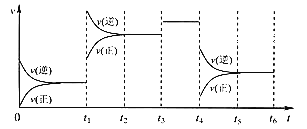
A. t1时升高了温度 B. t3时加入了催化剂
C. t4时降低了压强 D. 在t3~t4时间内,X的体积分数最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用H2O2、KI和洗洁精可完成“大象牙膏”实验(短时间内产生大量泡沫),某同学依据文献资料对该实验进行探究。
(1)资料1:KI在该反应中的作用:H2O2 + I![]() = H2O + IO
= H2O + IO![]() ;H2O2 + IO
;H2O2 + IO![]() = H2O + O2↑+ I
= H2O + O2↑+ I![]() 。总反应的化学方程式是_______________________________________________。
。总反应的化学方程式是_______________________________________________。
(2)资料2:H2O2分解反应过程中能量变化如图所示,其中①有KI加入,②无KI加入。下列判断正确的是______(填字母)。
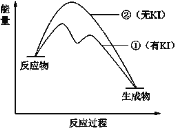
a.加入KI后改变了反应的路径
b.加入KI后改变了总反应的能量变化
c.H2O2 + I![]() = H2O + IO
= H2O + IO![]() 是放热反应
是放热反应
(3)实验中发现,H2O2与KI溶液混合后,产生大量气泡,溶液颜色变黄。再加入CCl4,振荡、静置,气泡明显减少。
资料3:I2也可催化H2O2的分解反应。
① 加CCl4并振荡、静置后还可观察到___________________________________,说明有I2生成。
② 气泡明显减少的原因可能是:
ⅰ. H2O2浓度降低;
ⅱ._________________________________________。
以下对照实验说明ⅰ不是主要原因:向H2O2溶液中加入KI溶液,待溶液变黄后,分成两等份于A、B两试管中。A试管加入CCl4,B试管不加CCl4,分别振荡、静置。观察到的现象是________________________。
(4)资料4:I![]() + I
+ I![]()
![]() I
I![]() K= 640。
K= 640。
为了探究体系中含碘微粒的存在形式,进行实验:向20 mL一定浓度的H2O2溶液中加入10 mL 0.10 mol·L-1 KI溶液,达平衡后,相关微粒浓度如下:
微粒 | I | I | I |
浓度/ (mol·L-1) | 2.5×10-3 | a | 4.0×10-3 |
① a =____________________。
② 该平衡体系中除了含有I![]() 、I
、I![]() 和I
和I![]() 外,一定还含有其他含碘微粒,理由是_____________________。
外,一定还含有其他含碘微粒,理由是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
(1)实验一:取等物质的量浓度等体积H2O2溶液分别进行下列实验,实验报告如下表所示。

试回答:
①实验1、2研究的是__________________________对H2O2分解速率的影响。
②实验2、3的目的是_______________________________________________。
(2)实验二:经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:

① 定性分析:如图甲可通过观察________________________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_________________________。
②定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是__________________________________。
(3)实验三:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显但不久突然褪色,反应速率明显加快。
①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是_____________________的影响。
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是_________。
A、硫酸钾 B、硫酸锰 C、水 D、氯化锰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器中发生反应4A(s)+3B(g)=2C(g)+D(g),经2 min,B的物质的量减少0.6 mol,下列对该反应速率表示正确的是
A.用B表示的反应速率:v (B)=0.3 mol·L-1·min-1
B.分别用B、C表示的反应速率其比值为2∶3
C.用D表示的平均反应速率为:v (D)= 0.05 mol·L-1·min-1
D.用A表示的反应速率为:v (A)=0.4 mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com