
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述不正确的是( )
4NO(g)+6H2O(g),下列叙述不正确的是( )
①平衡时,υ正(O2)=υ逆(O2)必成立
②关系式5υ正(O2)=4υ逆(NO)总成立
③用上述四种物质NH3、O2、NO、H2O表示正反应速率的数值中,υ正(H2O)最大
④若投入4molNH3和5molO2,通过控制外界条件,必能生成4molNO
A.①②B.②③C.①③D.②④
科目:高中化学 来源: 题型:
【题目】下图为室温时不同pH下磷酸盐溶液中含磷微粒形态的分布,其中a、b、c三点对应的pH分别为2.12、7.21、11.31,其中δ表示含磷微粒的物质的量分数,下列说法正确的是______
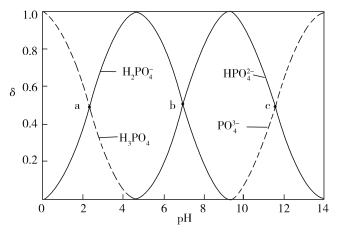
A.2 mol H3PO4与3 mol NaOH反应后的溶液呈中性
B.NaOH溶液滴定Na2HPO4溶液时,无法用酚酞指示终点
C.H3PO4的二级电离常数的数量级为107
D.溶液中除OH离子外,其他阴离子浓度相等时,溶液可能显酸性、中性或碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物①在一定条件下可以制备②,下列说法错误的是
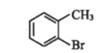 ①→
①→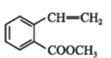 ②
②
A.①不易溶于水
B.①的芳香族同分异构体有3种(不包括①)
C.②在碱性条件下的水解是我们常说的皂化反应
D.②中所有碳原子可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温室效应和资源短缺等问题和如何降低大气中的CO2含量并加以开发利用引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g),如图表示该反应进行过程中能量 (单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量 (单位为kJ·mol-1)的变化。
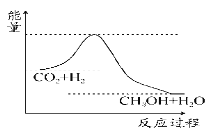
(1)关于该反应的下列说法中,正确的是________。
A.ΔH>0,ΔS>0
B.ΔH>0,ΔS<0
C.ΔH<0,ΔS<0
D.ΔH<0,ΔS>0
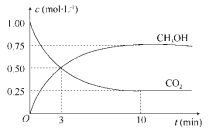
(2)为探究反应原理,现进行如下实验:在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2)____________________, CO2转化率为_________。相同温度下,某一时刻若该容器中含有1mol H2、1.2mol CO2、0.8 mol CH3OH、1.5mol H2O,则此时反应所处的状态为___________________________ (填“向正反应方向进行中”、 “向逆反应方向进行中”或“平衡状态”),理由______________________________________。
(3)在温度容积不变的条件下,能说明该反应已达平衡状态的是________(填写序号字母):
a.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶3∶1∶1
b.容器内压强保持不变
c.容器内的密度保持不变
d.H2的消耗速率与CH3OH的消耗速率之比为3∶1
(4)下列条件能使上述反应的反应速率增大,且平衡向正反应方向移动的是________(字母)。
a.及时分离出CH3OH气体
b.适当升高温度
c.保持容器的容积不变,再充入1 mol CO2和3 mol H2
d.选择高效的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+3B=2C+D在四种不同情况下的反应速率分别为①v(A)=0.15mol·L-1·s-1 ②v(B)=0.6mol·L-1·s-1 ③v(C)=0.5mol·L-1·min-1 ④v(D)=0.45mol·L-1·s-1。则反应进行由快到慢的顺序为( )
A.④>③>①>②B.④>②>①>③
C.②>③>④>①D.④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中的Ⅰ是某抗肿瘤药物的中间体,B的核磁共振氢谱有3组峰,C的分子式为C7H8O,D分子中有两个相同且处于相邻位置的含氧官能团,E的相对分子质量比D大34.5。
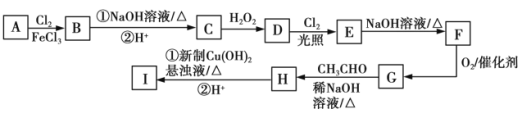
已知:RCHO+R1CH2CHO![]() RCH=C(R1)CHO+H2O。
RCH=C(R1)CHO+H2O。
请回答下列问题:
(1)C的名称是______,B的结构简式为_________,D转化为E的反应类型是____________。
(2)I中官能团的名称为______,I的分子式为________。
(3)写出E转化为F的化学方程式____________。
(4)X是G酸化后的产物,X有多种芳香族同分异构体,符合下列条件且能发生银镜反应的同分异构体有____种(不包括X),写出核磁共振氢谱有4组峰的物质的结构简式____________。
①遇FeCl3溶液发生显色反应 ②苯环上有两种类型的取代基
(5)参照上述流程,以乙醇为原料(其他无机试剂自选)可制取2﹣丁烯酸,写出相应的合成路线__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有H+、Mg2+、Al3+三种阳离子,逐滴加入0.1mol/L NaOH溶液,消耗NaOH溶液体积和生成沉淀关系如图,则下列说法正确的是( )
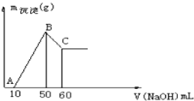
A. 横坐标为0-50mL时,所有反应为:Mg2++2OH-=Mg(OH)2↓ Al3++3OH-=Al(OH)3↓
B. B点生成沉淀的总物质的量0.02mol
C. 若往C点的溶液中加入足量盐酸,沉淀将全部溶解
D. H+、Mg2+、Al3+三种阳离子物质的量浓度之比为:2:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叠氮化钠(NaN3)是一种白色剧毒晶体,是汽车安全气囊的主要成分。NaN3易溶于水,微溶于乙醇,水溶液呈弱碱性,能与酸发生反应产生具有爆炸性的有毒气体叠氮化氢。实验室可利用亚硝酸叔丁酯(tBuNO2,以tBu表示叔丁基)与N2H4、氢氧化钠溶液混合反应制备叠氮化钠。
(1)制备亚硝酸叔丁酯
取一定NaNO2溶液与50%硫酸混合,发生反应H2SO4+2NaNO2===2HNO2+Na2SO4。可利用亚硝酸与叔丁醇(tBuOH)在40℃左右制备亚硝酸叔丁酯,试写出该反应的化学方程式:____________。
(2)制备叠氮化钠(NaN3)
按如图所示组装仪器(加热装置略)进行反应,反应的化学方程式为:tBuNO2+NaOH+N2H4===NaN3+2H2O+tBuOH。
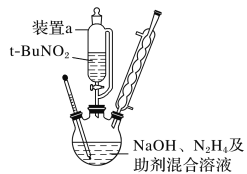
①装置a的名称是______________;
②该反应需控制温度在65℃,采用的实验措施是____________________;
③反应后溶液在0℃下冷却至有大量晶体析出后过滤。
所得晶体使用无水乙醇洗涤。试解释低温下过滤和使用无水乙醇洗涤晶体的原因是____________。
(3)产率计算
①称取2.0g叠氮化钠试样,配成100mL溶液,并量取10.00mL溶液于锥形瓶中。
②用滴定管加入0.10mol·L-1六硝酸铈铵[(NH4)2Ce(NO3)6]溶液40.00mL(假设杂质均不参与反应)。
③充分反应后将溶液稀释并酸化,滴入2滴邻菲罗啉指示液,并用0.10mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]为标准液,滴定过量的Ce4+,终点时消耗标准溶液20.00mL(滴定原理:Ce4++Fe2+===Ce3++Fe3+)。
已知六硝酸铈铵[(NH4)2Ce(NO3)6]与叠氮化钠反应生成硝酸铵、硝酸钠、氮气以及Ce(NO3)3,试写出该反应的化学方程式____________________________;计算叠氮化钠的质量分数为________(保留2位有效数字)。若其他操作及读数均正确,滴定到终点后,下列操作会导致所测定样品中叠氮化钠质量分数偏大的是____________(填字母)。
A.锥形瓶使用叠氮化钠溶液润洗
B.滴加六硝酸铈铵溶液时,滴加前仰视读数,滴加后俯视读数
C.滴加硫酸亚铁铵标准溶液时,开始时尖嘴处无气泡,结束时出现气泡
D.滴定过程中,将挂在锥形瓶壁上的硫酸亚铁铵标准液滴用蒸馏水冲进瓶内
(4)叠氮化钠有毒,可以使用次氯酸钠溶液对含有叠氮化钠的溶液进行销毁,反应后溶液碱性明显增强,且产生无色无味的无毒气体,试写出反应的离子方程式:____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿![]() (主要成分为
(主要成分为![]() ,含FeO杂质)为原料冶炼铝的工艺流程如下:
,含FeO杂质)为原料冶炼铝的工艺流程如下:

下列说法正确的是( )
A.试剂X可以是氢氧化钠溶液,也可以是盐酸溶液
B.反应①过滤后所得沉淀为氢氧化铁
C.图中所示转化反应都不是氧化还原反应
D.反应②的化学方程式为CO2 + Na[Al(OH)4] = NaHCO3 + Al(OH)3↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com