
����Ŀ����ͼ�еĢ���ij������ҩ����м��壬B�ĺ˴Ź���������3��壬C�ķ���ʽΪC7H8O��D��������������ͬ�Ҵ�������λ�õĺ��������ţ�E����Է���������D��34.5��
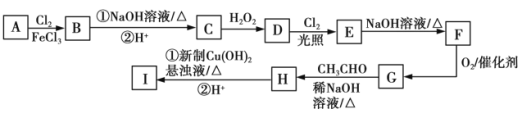
��֪��RCHO+R1CH2CHO![]() RCH=C(R1)CHO+H2O��
RCH=C(R1)CHO+H2O��
��ش��������⣺
(1)C��������______��B�Ľṹ��ʽΪ_________��Dת��ΪE�ķ�Ӧ������____________��
(2)I�й����ŵ�����Ϊ______��I�ķ���ʽΪ________��
(3)д��Eת��ΪF�Ļ�ѧ����ʽ____________��
(4)X��G�ữ��IJ��X�ж��ַ�����ͬ���칹�壬���������������ܷ���������Ӧ��ͬ���칹����____�֣�������X����д���˴Ź���������4�������ʵĽṹ��ʽ____________��
����FeCl3��Һ������ɫ��Ӧ���������ڱ��������������͵�ȡ����
(5)�����������̣����Ҵ�Ϊԭ�ϣ��������Լ���ѡ������ȡ2����ϩ�ᣬд����Ӧ�ĺϳ�·��__________________��
���𰸡��Լ����ӻ�4-������ ![]() ȡ����Ӧ ̼̼˫�����Ȼ������ǻ� C9H8O4
ȡ����Ӧ ̼̼˫�����Ȼ������ǻ� C9H8O4 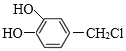 +3NaOH
+3NaOH ![]()
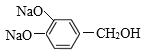 +NaCl+2H2O 8
+NaCl+2H2O 8 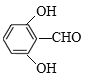 ��
�� ��
��![]()
![]()
��������
A��Cl2��FeCl3�����·�Ӧ��˵��A�����к��б��������������ϵ��ȴ���Ӧ������B��B�ĺ˴Ź���������3��壬˵��B��������3��Hԭ�ӣ�B��NaOHˮ��Һ���ȣ�Ȼ���ữ�õ�C��C�ķ���ʽΪC7H8O���ڷ�Ӧ������Cԭ�������䣬̼���ṹ���䣬���ƿ�֪A��![]() ��B��
��B��![]() ��C��
��C��![]() ��C��H2O2��������D�����������֪��Ϣ��D��������������ͬ�Ҵ�������λ�õĺ��������ţ�E����Է���������D��34.5����DΪ
��C��H2O2��������D�����������֪��Ϣ��D��������������ͬ�Ҵ�������λ�õĺ��������ţ�E����Է���������D��34.5����DΪ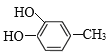 ��D��Cl2�ڹ��������·������ϵ�ȡ����Ӧ����E��
��D��Cl2�ڹ��������·������ϵ�ȡ����Ӧ����E�� ��E��NaOHˮ��Һ���ȷ�����Ӧ����F��
��E��NaOHˮ��Һ���ȷ�����Ӧ����F�� ��F��O2����������G��
��F��O2����������G��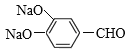 ��G��CH3CHO���������Ϣ��Ӧ����HΪ��
��G��CH3CHO���������Ϣ��Ӧ����HΪ��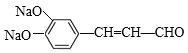 ��H������Cu(OH)2�ڼ��������·���ȩ����������Ӧ��Ȼ���ữ�ɵ�I��
��H������Cu(OH)2�ڼ��������·���ȩ����������Ӧ��Ȼ���ữ�ɵ�I��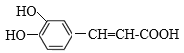 ���ݴ˷������
���ݴ˷������
��������������֪AΪ![]() ��BΪ
��BΪ![]() ��CΪ
��CΪ![]() ��DΪ
��DΪ ��EΪ
��EΪ ��FΪ
��FΪ ��GΪ
��GΪ ��HΪ
��HΪ ��IΪ
��IΪ ��
��
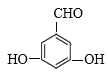
(1) CΪ![]() ������Ϊ�Լ����ӻ�4-�����ӣ�B�ṹ��ʽΪ
������Ϊ�Լ����ӻ�4-�����ӣ�B�ṹ��ʽΪ![]() ��DΪ
��DΪ ��D��Cl2�ڹ��������·������ϵ�ȡ����Ӧ����E��
��D��Cl2�ڹ��������·������ϵ�ȡ����Ӧ����E�� ������Dת��ΪE�ķ�Ӧ������ȡ����Ӧ��
������Dת��ΪE�ķ�Ӧ������ȡ����Ӧ��
(2)IΪ �����к��еĹ���������Ϊ��̼̼˫�����Ȼ������ǻ���I�ṹ��ʽΪ
�����к��еĹ���������Ϊ��̼̼˫�����Ȼ������ǻ���I�ṹ��ʽΪ �����Cԭ�Ӽ۵���Ϊ4����֪�����ʽΪC9H8O4��
�����Cԭ�Ӽ۵���Ϊ4����֪�����ʽΪC9H8O4��
(3)EΪ ��E��NaOHˮ��Һ���ȷ�����Ӧ����FΪ
��E��NaOHˮ��Һ���ȷ�����Ӧ����FΪ ���÷�Ӧ�ķ���ʽΪ��
���÷�Ӧ�ķ���ʽΪ�� +3NaOH
+3NaOH![]()
 +NaCl+2H2O��
+NaCl+2H2O��
(4) GΪ ��X��G�ữ��IJ����XΪ
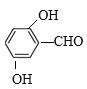
��X��G�ữ��IJ����XΪ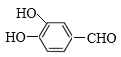 ��X�ķ�����ͬ���칹�壬�ܷ���������Ӧ���ҷ�����������������FeCl3��Һ������ɫ��Ӧ���ڱ��������������͵�ȡ���������ܵĽṹ����������������-OH��-OH��-CHO��������
��X�ķ�����ͬ���칹�壬�ܷ���������Ӧ���ҷ�����������������FeCl3��Һ������ɫ��Ӧ���ڱ��������������͵�ȡ���������ܵĽṹ����������������-OH��-OH��-CHO��������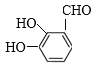 ��
�� ��
�� ��
��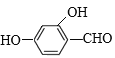 ��
�� ������������������HCOO-��-OH��������
������������������HCOO-��-OH��������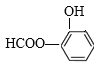 ��
��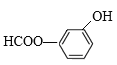 ��
��![]() ����˷���������ͬ���칹������Ϊ5+3=8�֣��˴Ź���������4�������ʵĽṹ��ʽΪ��
����˷���������ͬ���칹������Ϊ5+3=8�֣��˴Ź���������4�������ʵĽṹ��ʽΪ�� ��
�� ��
��![]() ��
��
(5)CH3CH2OH����������CH3CHO��CH3CHO��CH3CHO��NaOHˮ��Һ�м��ȷ�����Ӧ����CH3CH=CHCHO��CH3CH=CHCHO������Cu(OH)2����Һ������з���ȩ��������Ӧ��Ȼ���ữ�õ�CH3CH=CHCOOH�������Ҵ�Ϊԭ����ȡ2-��ϩ��ĺϳ�·��Ϊ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ2NO2![]() 2NO+O2�ڶ����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�ǣ� ��
2NO+O2�ڶ����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�ǣ� ��
����λʱ��������nmolO2��ͬʱ����2nmolNO2
����λʱ��������nmolO2��ͬʱ����2nmolNO
����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ����֮��Ϊ2:2:l��״̬
������������ɫ���ٸı��״̬
�����������ܶȲ��ٸı��״̬
����������ƽ����Է����������ٸı��״̬
A. �٢ܢ� B. �ڢۢ� C. �٢ۢ� D. �٢ڢۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС��Ϊ̽���¶ȡ�ѹǿ�Կ��淴ӦA(g)��B(g) ![]() C(g)��D(s)��Ӱ�죬����������ʵ�飺���������£���һ���ݻ�Ϊ10 L���ܱ������г���1 mol A��1 mol B����Ӧ��ƽ��ʱ��������и����ʵ���Ũ��Ϊ[Ũ��1]��Ȼ��ı������������������ʵ�飺��ֻ�����¶ȣ���ֻ�ı���ϵѹǿ���ֱ�����ƽ��ʱ�����и����ʵ���Ũ��Ϊ[Ũ��2]��[Ũ��3]�����ҳ�ʵ������٢���ʵ������[Ũ��2]��[Ũ��3]�Ķ�Ӧ��ϵ�����������н��ۣ����д������
C(g)��D(s)��Ӱ�죬����������ʵ�飺���������£���һ���ݻ�Ϊ10 L���ܱ������г���1 mol A��1 mol B����Ӧ��ƽ��ʱ��������и����ʵ���Ũ��Ϊ[Ũ��1]��Ȼ��ı������������������ʵ�飺��ֻ�����¶ȣ���ֻ�ı���ϵѹǿ���ֱ�����ƽ��ʱ�����и����ʵ���Ũ��Ϊ[Ũ��2]��[Ũ��3]�����ҳ�ʵ������٢���ʵ������[Ũ��2]��[Ũ��3]�Ķ�Ӧ��ϵ�����������н��ۣ����д������
A | B | C | |
Ũ��1 | 0.05 mol��L��1 | a mol��L��1 | 0.05 mol��L��1 |
Ũ��2 | 0.078 mol��L��1 | 0.078 mol��L��1 | 0.022 mol��L��1 |
Ũ��3 | 0.06 mol��L��1 | 0.06 mol��L��1 | 0.04 mol��L��1 |
Ũ��4 | 0.07 mol��L��1 | 0.07 mol��L��1 | 0.098 mol��L��1 |
A. ��[Ũ��3]��[Ũ��1]�ıȽϣ����ж�ƽ���ƶ���ԭ������������ϵ��ѹǿ
B. ��[Ũ��2]��[Ũ��1]�ıȽϣ����ж�����Ӧ�Ƿ��ȷ�Ӧ
C. [Ũ��1]��a��0.05
D. ����ijѧ����ʵ��ٹ����У���ø�������ijһʱ�̵�Ũ��Ϊ[Ũ��4]����[Ũ��1]�Ƚϣ��ɷ��ָ�ͬѧ�ڲⶨ[Ũ��4]��������ʱ�����˺ܴ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������(NOSO4H)��Ҫ����Ⱦ�ϡ�ҽҩ�ȹ�ҵ��ʵ��������ͼװ��(�г�װ����)�Ʊ�����NOSO4H�����ⶨ��Ʒ�Ĵ��ȡ���֪��NOSO4H��ˮ�ֽ⣬������Ũ��������ֽ⡣
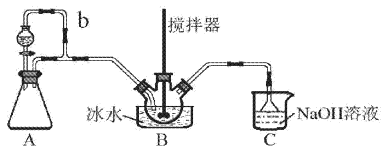
��1��װ��A��ȡSO2
��A�з�Ӧ�Ļ�ѧ����ʽΪ___��
�ڵ���b��������___��
��2��װ��B��ŨHNO3��SO2��ŨH2SO4�����·�Ӧ�Ƶ�NOSO4H��
�ٸ÷�Ӧ����ά����ϵ�¶Ȳ��ø���20�棬��ȡ�Ĵ�ʩ������ˮԡ�⣬��������___(ֻд1��)��
�ڿ�ʼ��Ӧ����������������NOSO4H���¶ȱ仯������Ӧ�ٶ����Լӿ죬��ԭ����___��
��3��װ��C����Ҫ������___(�����ӷ���ʽ��ʾ)��
��4����ʵ��װ�ô��ڿ��ܵ���NOSO4H�������͵�ȱ����___��
��5���ⶨ����������NOSO4H�Ĵ���
ȷ��ȡ1.380g��Ʒ����250mL�ĵ���ƿ�У�����0.1000mol��L-1��60.00mL��KMnO4����Һ��10mL25%H2SO4��Һ��Ȼ��ҡ�ȡ���0.2500mol��L-1�����Ʊ���Һ�ζ������IJ�������Һ�����Ϊ20.00mL��
��֪��2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
����ƽ��__MnO4-+__C2O42-+__=__Mn2++__+__H2O
�ڵζ��յ�ʱ������Ϊ___��
������������Ĵ���=___������ȷ��0.1%��[M(NOSO4H)=127g��mol-1]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Կ��淴Ӧ4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)��������������ȷ���ǣ� ��
4NO(g)+6H2O(g)��������������ȷ���ǣ� ��
��ƽ��ʱ������(O2)=����(O2)�س���
�ڹ�ϵʽ5����(O2)=4����(NO)�ܳ���
����������������NH3��O2��NO��H2O��ʾ����Ӧ���ʵ���ֵ�У�����(H2O)���
����Ͷ��4molNH3��5molO2��ͨ�����������������������4molNO
A.�٢�B.�ڢ�C.�٢�D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A��B���ڹ̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3A(g)+B(g) 2C(g)+2D(g)����Ӧ���е�10sĩ�����A�����ʵ���Ϊ1.8mol��B�����ʵ���Ϊ0.6mol��C�����ʵ���Ϊ0.8mol����
(1)��C��ʾ10s�ڷ�Ӧ��ƽ����Ӧ����Ϊ__��
(2)10sĩ��������D��Ũ��Ϊ__��
(3)���ı���������������D��������α仯(��������������С���������������)��
��� | �ı������ | ����D������ |
�� | �����¶� | ___ |
�� | ����A��Ũ�� | ___ |
�� | ʹ�������� | ___ |
�� | �����³���Ne (��������ϵ��Ӧ) | ___ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����V1mL1.0mol��L-1HCl��Һ��V2mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ������ͼ��ʾ(ʵ����ʼ�ձ���V1+V2=50mL)���밴Ҫ����գ�
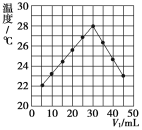
��ʵ������˷�Ӧ__(���������������ͷ���)����������__�ܿ���ת��Ϊ__�ܣ�ͨ��ʾ��ͼ�������Եó�������ʵ��ʱ�������¶�__(����������������������������)22�档
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����14�֣��屽��һ�ֻ���ԭ�ϣ�ʵ���Һϳ��屽��װ��ʾ��ͼ���й��������£�
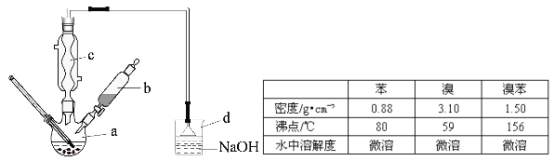
�����кϳɲ���ش����⣺
��1����a�м���15mL��ˮ����������м����b��С�ļ���4.0mLҺ̬�壬��a�е��뼸���壬�а�ɫ��������������Ϊ������ ���塣�����μ���Һ����꣬װ��d�������� ��
��2��Һ�����������в�������ᴿ��
����a�м���10mLˮ��Ȼ����˳�ȥδ��Ӧ����м��
����Һ������10mLˮ��8mL10%��NaOH��Һ��10mLˮϴ�ӡ�NaOH��Һϴ�ӵ������� ����ֳ��Ĵ��屽�м�����������ˮ�Ȼ��ƣ����á����ˣ������Ȼ��Ƶ��� ��
��3�������Ϸ���������屽�л����е���Ҫ����Ϊ ��Ҫ��һ���ᴿ�����в����б������ (������ȷѡ��ǰ����ĸ)��
A.�ؽᾧ B.���� C.���� D.��ȡ
��4���ڸ�ʵ���У�a���ݻ����ʺϵ��� (������ȷѡ��ǰ����ĸ)��
A.25mL B. 50mL C.250mL D.500mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������Ϊ��ɫ���壬�����������ӹ��ɣ���֪�������ӹ���Ϊƽ�������Σ����������ӵĹ��ͺ��������е����ӻ���ʽΪ�� ��
A. ƽ�������� sp2�ӻ�B. V�� sp2�ӻ�
C. ������ sp3�ӻ�D. ֱ���� sp�ӻ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com