
【题目】关于如图所示装置的叙述,正确的是
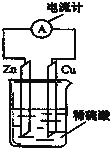
A.该装置构成原电池,锌易失电子作负极、Cu 作正极,负极上电极反应式为 Zn-2e-=Zn2+,所以锌的质量逐渐减少
B.电流从负极锌沿导线流向正极铜
C.该装置是将电能转化为化学能的装置,为原电池
D.氢离子在锌片上被还原,所以锌片上有气泡生成
科目:高中化学 来源: 题型:
【题目】下列关于常见有机物的说法中正确的是( )
![]() 棉花、蚕丝和聚乙烯的主要成分都是纤维素
棉花、蚕丝和聚乙烯的主要成分都是纤维素
![]() 甲烷、乙醇和乙酸在一定条件下都能发生取代反应
甲烷、乙醇和乙酸在一定条件下都能发生取代反应
![]() 等质量的乙烷、乙烯、苯充分燃烧,消耗氧气的量由多到少
等质量的乙烷、乙烯、苯充分燃烧,消耗氧气的量由多到少
![]() 除去乙酸乙酯中残留的乙酸,加过量饱和Na2CO3溶液振荡后,静置分液
除去乙酸乙酯中残留的乙酸,加过量饱和Na2CO3溶液振荡后,静置分液
![]() 苯分子中含有碳碳双键和单键,既能发生加成反应,也能发生取代反应
苯分子中含有碳碳双键和单键,既能发生加成反应,也能发生取代反应
![]() 石油分馏和煤的干馏属于物理变化,石油的裂化、裂解都属于化学变化
石油分馏和煤的干馏属于物理变化,石油的裂化、裂解都属于化学变化
A.①⑤⑥B.②③④C.①②③D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知尿素的结构式为:![]() ,尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3。
,尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3。
(1)C、N、O三种元素的电负性由大到小顺序是__________。
(2) NH4+中H—N—H键角比NH3中H—N—H键角大,原因为______________________。
(3)美国科学家合成了结构呈“V”形的N5+,已知该离子中各原子均达到8电子稳定结构。则有关该离子的下列说法中正确的是_____。
A.每个N5+中含有35个质子和36个电子 B.该离子中有非极性键和配位键 C.该离子中含有2个π键 D.与PCl4+互为等电子体
(4)Fe(Ⅲ)除可与H2NCONH2形成配合物[Fe(H2NCONH2)6](NO3)3外,FeCl3溶液也可与KSCN溶液混合,得到含多种配合物的红色溶液,其中配位数为5的配合物的化学式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,22.4L氯仿中含有的氯原子数目为3NA
B.1mol羟基中含有的电子数为10NA
C.常温常压下,50gC7H16分子中含有的共价键数目为11NA
D.14g乙烯与2-丁烯混合物中含有碳原子数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2NCOONH4是工业由氨气合成尿素的中间产物。在一定温度下、体积不变的密闭容器中发生反应H2NCOONH4(s)![]() 2NH3(g)+CO2(g),能说明该反应达到平衡状态的是①每生成34g NH3的同时消耗44g CO2 ②混合气体的平均相对分子质量不变 ③NH3的体积分数保持不变 ④混合气体的密度保持不变 ⑤c(NH3):c(CO2)=2:1
2NH3(g)+CO2(g),能说明该反应达到平衡状态的是①每生成34g NH3的同时消耗44g CO2 ②混合气体的平均相对分子质量不变 ③NH3的体积分数保持不变 ④混合气体的密度保持不变 ⑤c(NH3):c(CO2)=2:1
A. ①③⑤ B. ①③④ C. ②④ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某华人科学家和他的团队研发出“纸电池” (如图)。这种一面镀锌、一面镀二氧化锰的超薄电池在使用印刷与压层技术后,变成一张可任意裁剪大小的“电纸”,厚度仅为0.5毫米,可以任意弯曲和裁剪。纸内的离子“流过”水和氧化锌组成电解液,电池总反应式为: Zn+2MnO2+H2O=ZnO+2MnO(OH)。下列说法正确的是

A.该电池的正极材料为锌
B.该电池反应中二氧化锰发生了氧化反应
C.电池的正极反应式为2MnO2 +2H2O+2e-= 2MnO(OH)+2OH-
D.当有0.1mol锌溶解时,流经电解液的电子数为1.204×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尼泊金甲酯用作化妆品防腐剂,其结构为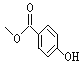 。下列有关说法正确的是( )
。下列有关说法正确的是( )
A.1mol尼泊金甲酯完全燃烧消耗7molO2
B.该化合物能与溴水反应,也能与NaHCO3反应
C.该化合物的同分异构体可能含有羧基
D.1mol该化合物最多可与4molH2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述变化理论上计量结果正确的是( )
A. 标准状况下,用含空气和氨气体积各半的烧瓶进行喷泉实验,所得溶液的物质的量浓度约为![]()
B. 相同质量的两份铝,分别放入足量的![]() 和
和![]() 溶液中充分反应,消耗的
溶液中充分反应,消耗的![]() 和
和![]() 之比为1∶1
之比为1∶1
C. 将![]() 逐滴加入到
逐滴加入到![]() 溶液中,产生
溶液中,产生![]() 的体积约为
的体积约为![]() (标准状况下)
(标准状况下)
D. 向![]() 的
的![]() 溶液中通入足量的
溶液中通入足量的![]() 气体,生成
气体,生成![]() 沉淀
沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验装置的科学设计是实验是否取得预期效果的关键。请回答下列有关实验装置的相关问题:

I.图一中A为教材制备乙酸乙酯的实验装置,甲同学认为图一中B装置比A要好,则冷却水应从______口进入;乙同学认为图一中C装置效果更好,理由是_______。
Ⅱ.“摩尔盐”[(NH4)2Fe(SO4)26H2O]是分析化学中的重要试剂。已知:摩尔盐隔绝空气加热至500℃时可完全分解。某学习小组欲探究其分解产物。
(1)[提出猜想]小组同学认为分解产物可能有以下几种情况:
A.Fe2O3、SO2、NH3、H2O B.FeO、SO3、NH3、H2O
C.FeO、SO2、NH3、H2O D.Fe2O3、SO3、SO2、NH3、H2O
根据所学知识,可确定_________不成立(填序号)
(2)[药品验纯]甲同学提出可以用湿润的红色石蕊试纸、稀盐酸和_________溶液检验出“摩尔盐”中的三种离子;取一定量的“摩尔盐”配成溶液,取少量溶液置于试管中,向其中滴加_______(填试剂名称和实验现象),则“摩尔盐”未因氧化而变质。
(3)[实验探究]为检验分解产物,甲同学设计了如下实验装置。
①取一定量“摩尔盐”置于加热管A中,加热至分解完全后打开K,再通入N2,目的是________。
②实验中观察到A中固体逐渐变为红棕色,B、C中均产生白色沉淀.C中发生反应的离子方程式为________。
③实验验证取A中残留物少许加入稀硫酸溶解,再滴入KMnO4稀溶液,不褪色证明产物不含______。
(4)[实验结论与反思]通过实验现象和认真反思,上述猜想中一定正确的是______。(填序号)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com