
【题目】氨是一种重要的化工原料,可以用来制备氮化硅(Si3N4)肼(N2H4)、氢氰酸(HCN)。
(1)已知:Si(s)+2Cl2(g)====SiCl4(g) △H1=akJ·mol-1
N2(g)+3H2(g) ![]() 2NH3(g) △H2=bkJ·mol-1
2NH3(g) △H2=bkJ·mol-1
3Si(s)+2N2(g)====Si3N4(s) △H3=ckJ·mol-1
H2(g)+Cl2(g)====2HCl(g) △H4=dkJ·mol-1
则反应3SiCl4(g)+4NH3(g)====Si3N4(s)+12HCl(g)的△H=________________kJ·mol-1(用a、b、c、d表示)。
(2)肼的制备方法是用次氯酸钠氧化过量的氨。
已知ClO-水解的方程式为:ClO-+H2 O=HClO+OH-。常温下,该水解反应的平衡常数为K=1.0×10-6mol·L-1,则1.0mol· L -1NaCIO溶液的pH=________。
(3)工业上利用氨气生产氢氰酸(HCN)的反应为:CH4(g)+NH3(g) ![]() HCN(g)+3H2 (g) △H>O
HCN(g)+3H2 (g) △H>O
①其他条件一定,达到平衡时NH3转化率随外界条件X变化的关系如图所示。X代表的是________(填“温度”或“压强”)。

②其他条件一定,向2L密闭容器中加人 n mol CH4和2 mol NH3,平衡时NH3体积分数随n变化的关系如图所示。若反应从开始到a点所用时间为10min,该时间段内用CH4的浓度变化表示的反应速率为________mol·L-1·min-1;平衡常数:K(a) ________K(b)(填“>”“=”或“<”)
③工业上用电解法处理含氰电镀废水(pH=10)的装置如图所示。

阳极产生的氯气与碱性溶液反应生成ClO-,ClO-将CN-氧化的离子方程式为:_____CN-+ _____ClO-+ ________====_____CO32-+_____N2↑+________+________若电解处理2 mol CN-,则阴极产生气体的体积(标准状况下)为________L。
【答案】c+6d-3a-2b 11 压强 0.025 = 2 5 20H- 2 l 5 Cl- H2O 112
【解析】
运用盖斯定律计算反应热;依据勒夏特列原理分析平衡的移动方向;根据得失电子数目守恒规律配平氧化还原反应。
(1) 已知:Si(s)+2Cl2(g)====SiCl4(g) △H1=akJ·mol-1 ①
N2(g)+3H2(g) ![]() 2NH3(g) △H2=bkJ·mol-1 ②
2NH3(g) △H2=bkJ·mol-1 ②
3Si(s)+2N2(g)====Si3N4(s) △H3=ckJ·mol-1 ③
H2(g)+Cl2(g)====2HCl(g) △H4=dkJ·mol-1 ④
根据盖斯定律,③+6![]() ④-3
④-3![]() ①-2
①-2![]() ②得3SiCl4(g)+4NH3(g)====Si3N4(s)+12HCl(g),△H=△H3+6
②得3SiCl4(g)+4NH3(g)====Si3N4(s)+12HCl(g),△H=△H3+6![]() △H4-3
△H4-3![]() △H1-2
△H1-2![]() △H2= c+6d-3a-2b kJ·mol-1,
△H2= c+6d-3a-2b kJ·mol-1,
故答案为:c+6d-3a-2b;
(2) 1.0mol· L -1NaCIO溶液中,c(ClO-)= 1.0mol· L -1,已知ClO-+H2 O=HClO+OH-,该水解反应的平衡常数为K=c(HClO) c(OH-)/ c(ClO-)= c2(OH-)=1.0×10-6mol·L-1,c(OH-)= 1.0×10-3mol·L-1,则c(H+)=10-14/10-3=10-11,pH=11,
故答案为:11;
(3) ①根据图示,X越大转化率越小,平衡逆向移动,该反应为吸热,温度升高平衡正向移动,增大压强,平衡逆向移动,
故答案为:压强;
②设 10min时,反应的氨气的物质的量为x
CH4(g)+NH3(g) ![]() HCN(g)+3H2 (g)
HCN(g)+3H2 (g)
开始(mol) 2 2 0 0
反应(mol) x x x 3x
a点(mol) 2-x 2-x x 3x
则(2-x)/2-x+x+3x=30%,x=0.5,v(CH4)=(0.5mol/2L)/10min=0.025 mol·L-1·min-1;平衡常数只和温度有关,所以K(a)=K(b),
故答案为:0.025,=;
③由题干知,0H-参加反应,ClO-被还原成Cl-同时产物中还有水生成,再根据转移电子数相等及原子守恒规律配平得:
2 CN-+5ClO-+20H-====2CO32-+N2↑+5Cl- +H2O;根据反应方程式得,处理2mol CN-消耗5mol ClO-,消耗5molCl2,所以阴极生成5mol氢气,则V(H2)=22.4mol/L![]() 5mol=112L,
5mol=112L,
故答案为:2,5,20H-,2,1,5 Cl-,H2O;112。


科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如下微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是

A. 断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl—![]() Cl2↑+H2↑
Cl2↑+H2↑
B. 断开K2,闭合K1时,石墨电极附近溶液变红
C. 断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl—
D. 断开K1,闭合K2时,石墨电极作正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在生产、生活中应用时,起还原作用的是 ( )
A. 铁粉作食品袋内的脱氧剂 B. 纯碱作除酸剂
C. 生石灰在烧煤时作脱硫剂 D. 明矾作净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D1、D2均为有机化合物,请根据图示回答问题.

(1)直链有机化合物A的结构简式是______________;
(2)①的反应类型是____________________;.
(3)②的反应类型是__________________;
(4)③的反应类型是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示。以下说法不正确的是

A. 中间室Cl—移向左室 B. 处理后的含硝酸根废水pH降低
C. X气体为CO2 D. 电路中每通过1 mol电子,产生标准状况下氮气的体积为2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲证明乙炔能与高锰酸钾酸性溶液反应,实验方案如下:将电石与水反应生成的气体通入高锰酸钾酸性溶液,溶液褪色,证明二者发生了反应.请回答:
(1)制备乙炔的反应的化学方程式是______________。
(2)该同学的实验方案存在的问题是______________。
(3)为了解决上述问题,需重新选择实验装置,备选装置如图所示.

①将装置编号按顺序填在横线上_____→B→_____。
②B装置中所盛放的试剂是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将SO2通入BaCl2溶液至饱和的过程中,始终未观察到溶液中出现浑浊,若再通入另一种气体A,则产生白色沉淀。制备气体A的试剂不能是
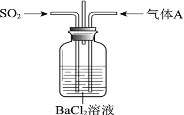
A. 大理石和稀盐酸
B. NaOH和NH4Cl
C. Cu和浓硝酸
D. MnO2和浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的铁与一定量的浓HNO3在加热条件下恰好完全反应,得到硝酸铁溶液和NO2 、N2O4 、NO的混合气体,这些气体与6.72 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铁溶液中加入2 mol·L-1 的NaOH 溶液至Fe3+恰好沉淀,则消耗NaOH 溶液的体积是( )
A. 600 mLB. 300 mLC. 240 mLD. 180 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以二氧化碳和氢气为原料制取乙醇的反应为:2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下的密闭容器中,按CO2和H2的物质的量比为1︰3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是( )
CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下的密闭容器中,按CO2和H2的物质的量比为1︰3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是( )

A. a点的平衡常数小于b点
B. b点,υ正(CO2)=υ逆(H2O)
C. a点,H2和H2O物质的量相等
D. 其他条件恒定,充入更多H2,乙醇的物质的量分数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com