
��17�֣���2012?�㶫��������㷺Ӧ������ҩ�ͻ�����ҵ��ijͬѧ�����üױ���������Ӧ�Ʊ������ᣬ��Ӧԭ����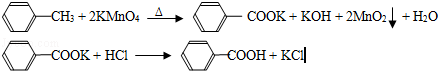
ʵ�鷽����һ�����ļױ���KMnO4��Һ��100�淴Ӧһ��ʱ���ֹͣ��Ӧ�����������̷����������ͻ���δ��Ӧ�ļױ���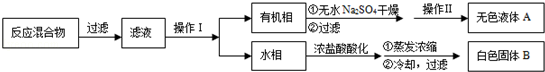
��֪�������������122���۵�122.4�棬��25���95��ʱ�ܽ�ȷֱ�Ϊ0.3g��6.9g�����������л��ﶼ�й̶��۵㣮
��1���������� ������������ ����
��2����ɫҺ��A���� �������Լ���A���Լ����� ������������
��3���ⶨ��ɫ����B���۵㣬��������115�濪ʼ�ۻ����ﵽ130��ʱ�����������ۣ���ͬѧ�Ʋ��ɫ����B�DZ�������KCl�Ļ�����������·��������ᴿ�ͼ��飬ʵ���������Ʋ���ȷ�����ڴ������ɱ������ݣ�
| ��� | ʵ�鷽�� | ʵ������ | ���� |
| �� | ����ɫ����B����ˮ�У������ܽ⣬��_________�� ��_________�� | �õ���ɫ�������ɫ��Һ | |
| �� | ȡ������Һ���Թ��У���_________�� | ���ɰ�ɫ���� | ��Һ��Cl�� |
| �� | �����ɫ���壬��_________�� | ��_________�� | ��ɫ�����DZ����� |
 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����п��ZnFe2O4���ǶԿɼ������еİ뵼���������ʵ�����Ʊ�ԭ��Ϊ��
Zn2++2Fe2++3C2O42��+6H2O ZnFe2(C2O4)3��6H2O������������(a)
ZnFe2(C2O4)3��6H2O������������(a)
ZnFe2(C2O4)3��6H2O  ZnFe2O4+2CO2��+4CO��+6H2O ����������(b)
ZnFe2O4+2CO2��+4CO��+6H2O ����������(b)
��1�������Ʊ�ԭ��������������ԭ��Ӧ���� ��ѡ���a����b������
��2���Ʊ�ZnFe2(C2O4)3��6H2Oʱ����ѡ�õ�ҩƷ�У�
��(NH4)2Fe(SO4)2��6H2O����ZnSO4��7H2O����(NH4)2C2O4��7H2O��
�ٳ���ҩƷʱ�������ϸ����n(Fe2+)/n(Zn2+)= ��
��ѡ�õļ��Ϸ�ʽ�� (����ĸ)��
a����һ�������ȣ���ͬʱ���뷴Ӧ������ˮ���裬Ȼ��������75�档
b����һ�������ȣ���ͬʱ���뷴Ӧ����ˮ�����Һ��Ȼ������Ȼ�����µ�75�档
c����һ�������ȣ������ϲ������Һ�ף��������������Һ�ң��ס���ͬʱ���ȵ�75�棬Ȼ������Һ�����������Һ�У����������衣
��3������Һ�з����ZnFe2(C2O4)3��6H2O����ˡ�ϴ�ӡ���ϴ����ȫ�������� ��
��4��ZnFe2(C2O4)3��6H2O�ȷֽ����þƾ���ƣ����õ��Ĺ������������� �� ��
��5��ij��ѧ����С�����÷Ͼɸɵ��пƤ�������������������ͼ��Ϣ����ʵ����ṩ���Լ���ȡ������ZnSO4��Һ��
ʵ���п�ѡ�õ��Լ����£�
��a��30%H2O2����b��������ˮ��
��c��1.0 mol��L��1NaOH��Һ��
��d��3mol��L-1ϡ���
��e����ZnO��ĩ��
��f����п�ۡ�
ʵ�鲽������Ϊ���ٽ�пƬ��ȫ�����Թ�����3mol��L��1ϡ���ᣬ���� ��ѡ����ĸ����ͬ�����ڼ��� ���ۼ��ȵ�60�����Ҳ����Ͻ��裻
�ܹ��˵�ZnSO4��Һ�����в���ۼ��ȵ���ҪĿ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
��16�֣�ijͬѧ���������˽�����и��������Ե��������Σ������κ�̼���Ρ���ͬѧ����ʵ����֤��һ��ʵ��������в����εĺ������������ϵ�֪���ᣨH2C2O4����һ�ֶ�Ԫ�л����ᣬ���н�ǿ�Ļ�ԭ�ԣ�����ƣ�CaC2O4��������ˮ������ϡ���ᡣ��ش��������⣺
��1����ѧ����������ĥ�ɷ�ĩ����ˮ���ݡ����˵õ�������ҺA����ĥ����ʹ�õ�ʵ������������Ϊ ��
��2�����ʵ�鷽����֤�����к��в����κ�̼���Σ��������Ԥ������ͽ��ۡ�
| ʵ�鲽�� | Ԥ������ͽ��� |
| ����1��������ҺA�������ԣ��μ�����CaCl2��Һ�� | �ٳ��ְ�ɫ������˵�������� �� |
| ����2��ȡ����1�ij������Թ��У�����������ϡ���ᣬ������ȫ�ܽ⣬������������ɫ��ζ������ͨ�����ʯ��ˮ�С� | �� �� |
| ����3������2�õ�����Һ�еμӼ��θ��������Һ�� | �� �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��������Ӱ�����ǵ������뽡����ij�����������п��ܺ������¿����������ӣ�Na+��NH4+��Mg2+��Al3+��SO42����NO3����Cl�� ��ijͬѧ�ռ��˸õ���������������Ҫ��Ԥ������������Һ����Ʋ���������µ�ʵ�飺
��֪��3NO3��+ 8Al + 5OH�� + 2H2O 3NH3 + 8AlO2��
3NH3 + 8AlO2��
�������ϵ�ʵ�����������ͬѧ�ó��Ľ��۲���ȷ����
�����п϶�����NH4+��Mg2+��SO42����NO3��
������һ������Al3+
�����п��ܴ���Na+��Cl��
�������п��ܴ���NaNO3��NH4Cl��MgSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��12�֣��Ȼ�����Ʒ�к�����̼��ء�����غͲ�����ˮ�����ʡ�Ϊ���ᴿ�Ȼ��أ��Ƚ���Ʒ��������ˮ�У���ֽ������ˣ��ٽ�����Һ����ͼ��ʾ������в�����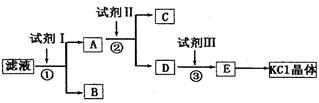
�ش��������⣺
(1)��ʼʱ��Һ��pH_____7������ڡ���С�ڡ����ڡ�������ԭ����__________________�������ӷ���ʽ��ʾ����
(2)�Լ�I�Ļ�ѧʽΪ______�����з�����Ӧ�����ӷ���ʽΪ_____________________��
(3)�Լ�II�Ļ�ѧʽΪ_____�����м����Լ�II��Ŀ����_________________________��
(4)�Լ�III��������_____�����з�����Ӧ�����ӷ���ʽΪ________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��15�֣�CoCl2��6H2O��һ������Ӫ��ǿ������һ������ˮ�����Ҫ�ɷ�ΪCO2O3��Co
��OH��3����������Fe2O3��Al2O3��MnO�ȣ���ȡCoCl2��6H2O�Ĺ����������£�
��֪���ٽ���Һ���е���������Ҫ��H+��CO2+��Fe2+��Mn2+��Al3+�ȣ�
�ڲ���������������������ʽ����ʱ��Һ��pH���±�������������Ũ��Ϊ��0��01 mo1��L-l��
��CoCl2��6H2O�۵�Ϊ86�棬������110��120��ʱ��ʧȥ�ᾧˮ������ˮ�Ȼ��ܡ�
��1��д������������Co2O3������Ӧ�����ӷ���ʽ ��
��2��д��NaC1O3������Ӧ����Ҫ���ӷ���ʽ ������������Һ���мӹ���NaClO3ʱ�����ܻ������ж����壬д�����ɸ��ж���������ӷ���ʽ ��
��3������Na2CO3��pH��a'�����������õ��ij����ɷ�Ϊ____ ��
��4����ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ������Һ���м�����ȡ����Ŀ���� ����ʹ�õ����pH��Χ��____ ��
| A��2��0��2��5 | B��3��0��3��5 | C��4��0��4��5 | D��5��0��5��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
1,2����������������Ϳ����������Ӽ���������������ɫҺ�壬�ܶ���2��18g/cm3���е�131��4�棬�۵�9��79�棬������ˮ�������ڴ����ѡ���ͪ���л��ܼ�����ʵ�����п�������ͼ��ʾװ���Ʊ�1,2-�������顣���з�Һ©������ƿa��װ���Ҵ���Ũ����Ļ��Һ���Թ�d��װ��Һ��(���渲������ˮ)��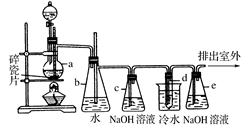
(1)д���������Ʊ�1,2-���������������ѧ��Ӧ����ʽ_____________________________��
(2)��ȫƿb���Է�ֹ�����������Լ��ʵ�����ʱ�Թ�d�Ƿ�����������д����������ʱƿb�е�����________________________________________��
(3)����c��NaOH��Һ�������ǣ� ��
(4)ijѧ������ʵ��ʱ��ʹ��һ������Һ�壬����ȫ����ɫʱ���������Ҵ���Ũ������Һ��������������³������࣬���װ�õ�������û�����⣬�Է�������ܵ�ԭ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
(13��)ij�о���ѧϰС����̽��Na2CO3��Һ��MgCl2��Һ��Ӧ������ɫ�����ijɷ֣�С���Ա������ʵ��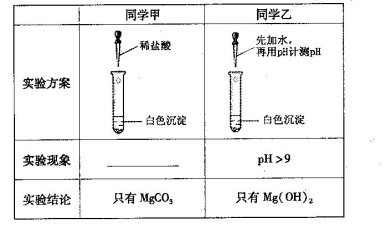
��1���������õĽ��۷������۲쵽��ʵ��������___________________________��
��2����̽��������ɷ�ǰ���ס��Ҷ������������Һ�з��������ϴ�Ӳ����ͬѧ����Ϊ���Dz�δ������ϴ�Ӹɾ������ü�ʵ��֤�����Ĺ۵㡣
��3��ͬѧ����Ϊ���۲�������������Ksp(MgCO3)___Ksp [Mg(OH)2](ѡ���������)�����Գ�����δ����MgCO3�����������ϵ�֪���ð�ɫ���������ӦΪMgx(OH)y(CO3)z��nH2O��Ϊȷ����
����ľ�����ɣ��������ͼװ�ý���ʵ��(���мг�װ����ʡ��)��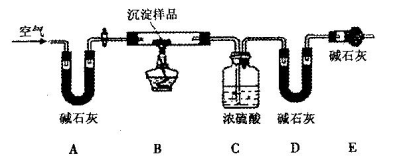
��4���뽫����Ƶ�ʵ�鲽�貹��������
�ټ��װ�������ԣ�
����װ��ҩƷ�����������װ�õ������������Ӹ�װ�ã�
��________________________________________________________��
��ֹͣ���ȣ�����ͨ�����ֱ��ʵ��������ٴγ�������������װ�õ�������
��5��װ��E�м�ʯ�ҵ�������_________________________________________________��
����ʵ�������������£�(���������ѻ���Ϊ��Ӧ�����ʵ���)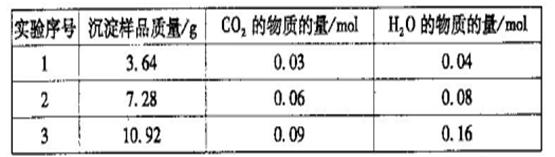
��6������ʵ�����ݿ�֪����_________��������ϴ�����ݣ�Ӧ��ȥ����ʵ�����ݼ���
�øð�ɫ����������Ϊ___________(ѡ�����)��
a��Mg2(OH)2CO3��3H2O b��Mg(OH)2(CO3)2��3H2O
c��Mg4(OH)2(CO3)3��3H2O d��Mg5(OH)4(CO3)3��2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�����л�����ϩ������ȥ��ϩ�õ������ļ��飬�������ͨ��ʢ��������Щ�Լ���ϴ��ƿ�� ��
| A������ʯ��ˮ��ŨH2SO4 | B������KMnO4��ŨH2SO4 |
| C����ˮ��ŨH2SO4 | D��ŨH2SO4����ˮ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com