
【题目】锗是重要的半导体材料,应用于航空航天测控、光纤通讯等领域.一种提纯二氧化锗粗品(主要含GeO2、As2O3)的工艺如下:
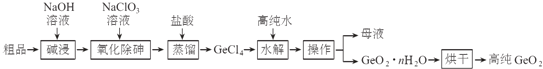
已知:①“碱浸”过程中的反应为:
GeO2+2NaOH=Na2GeO3+H2O
As2O3+2NaOH=2NaAsO2+H2O
②“蒸馏”过程中的反应为:Na2GeO3+6HCl=2NaCl+GeCl4+3H2O
③GeCl4的熔点为-49.5℃,AsCl3与GeCl4的沸点分别为130.2℃、84℃.
(1)锗的原子序数为32,锗在元素周期表中的位置为第 ______ 周期 ______ 族.
(2)“氧化除砷”的过程是将NaAsO2氧化为Na3AsO4,其反应方程式为: ______ .
(3)传统的提纯方法是将粗品直接加入盐酸中蒸馏,其缺点是 ______ .
(4)工业上与蒸馏操作相关的设备有 ______
A.蒸馏釜 B.离心萃取机 C.冷凝塔 D.加压过滤机
(5)“水解”操作时发生的化学反应方程式为 ______ ,“水解”操作时保持较低温度有利于提高产率,其最可能的原因是 ______ (答一条即可).
(6)若1吨二氧化锗粗品(含杂质30%)经提纯得0.745吨的高纯二氧化锗产品,则杂质脱除率为 ______.
【答案】四 IVA 3NaAsO2+NaClO3+6NaOH=3Na3AsO4+NaCl+3H2O 馏出物中将会含有AsCl3,降低了产品纯度 AC GeCl4+(n+2)H2O=GeO2nH2O↓+4HCl 该水解反应为放热反应,温度较低时反应平衡常数较大,反应物平衡转化率更高或温度高时GeCl4易挥发降低产率 85%
【解析】
⑴根据锗的原子序数为32,与碳是同一主族元素,得出周期表位置。
⑵根据氧化还原反应原理来书写方程式。
⑶AsCl3与GeCl4的沸点分别为130.2℃、84℃,传统的提纯方法是将粗品直接加入盐酸中蒸馏,其缺点是馏出物中将会含有AsCl3。
⑷蒸馏釜与蒸馏烧瓶相似的性质,冷凝管和冷凝塔有相似的性质。
⑸“水解”操作时保持较低温度有利于提高产率,其最可能的原因是该水解反应为放热反应,温度较低时反应平衡常数较大,反应物平衡转化率更高或温度高时GeCl4易挥发降低产率。
⑹若1吨二氧化锗粗品(含杂质30%)即杂质为0.3吨,经提纯得0.745吨的高纯二氧化锗产品,说明还有0.045吨的杂质还未除掉,除掉了0.255吨的杂质,再进行计算脱除率。
⑴锗的原子序数为32,与碳是同一主族元素,因此锗在元素周期表中的位置为第四周期IVA族,故答案为:四;IVA。
⑵“氧化除砷”的过程是将NaAsO2氧化为Na3AsO4,其反应方程式为:3NaAsO2+NaClO3+ 6NaOH = 3Na3AsO4+NaCl+3H2O,故答案为:3NaAsO2+NaClO3+ 6NaOH = 3Na3AsO4 + NaCl+3H2O。
⑶AsCl3与GeCl4的沸点分别为130.2℃、84℃,传统的提纯方法是将粗品直接加入盐酸中蒸馏,其缺点是馏出物中将会含有AsCl3,降低了产品纯度,故答案为:馏出物中将会含有AsCl3,降低了产品纯度。
⑷蒸馏釜与蒸馏烧瓶相似的性质,冷凝管和冷凝塔有相似的性质,工业上与蒸馏操作相关的设备有AC,故答案为:AC。
⑸“水解”操作时发生的化学反应方程式为GeCl4 + (n+2)H2O = GeO2nH2O↓ + 4HCl,“水解”操作时保持较低温度有利于提高产率,其最可能的原因是该水解反应为放热反应,温度较低时反应平衡常数较大,反应物平衡转化率更高或温度高时GeCl4易挥发降低产率,故答案为:该水解反应为放热反应,温度较低时反应平衡常数较大,反应物平衡转化率更高或温度高时GeCl4易挥发降低产率。
⑹若1吨二氧化锗粗品(含杂质30%)即杂质为0.3吨,经提纯得0.745吨的高纯二氧化锗产品,说明还有0.045吨的杂质还未除掉,除掉了0.255吨的杂质,因此杂质脱除率为 ![]() ,故答案为:85%。
,故答案为:85%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】2005年诺贝尔化学奖授予了研究烯烃复分解反应的科学家,以表彰他们作出的卓越贡献。烯烃复分解反应原理如下:C2H5CH=CHCH3+CH2=CH2![]() C2H5CH=CH2+CH2=CHCH3
C2H5CH=CH2+CH2=CHCH3
现以烯烃C5H10为原料,合成有机物M和N,合成路线如下:

(1)按系统命名法,有机物A的名称是_______。
(2)B的结构简式是__________。
(3)C![]() D的反应类型是___________。
D的反应类型是___________。
(4)写出D![]() M的化学方程式________。
M的化学方程式________。
(5)已知X的苯环上只有一个取代基,且取代基无甲基,则N的结构简式为_______。
(6)满足下列条件的X的同分异构体共有_______种,写出任意一种的结构简式_________。
①遇FeCl3溶液显紫色 ②苯环上的一氯取代物只有两种
(7)写出E![]() F合成路线(用结构简式表示有机物,箭头上注明试剂和反应条件)。______
F合成路线(用结构简式表示有机物,箭头上注明试剂和反应条件)。______
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种无机物之间的转化关系如下图所示(反应条件省略,部分产物省略)。下列推断不正确的是( )

A.若L为强碱,则E可能为NaCl溶液、F为K
B.若L为强酸,则E可能为Na2S、F为H2O2
C.若L为弱酸,则E可能为Mg、F为CO2
D.若L为强酸,则E可能为NH4Cl、F为Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】洗煤和选煤过程中排出的煤矸石(主要含Al2O3、SiO2及Fe2O3)会占用大片土地,造成环境污染。某课题组利用煤矸石制备聚合氯化铝流程如下:
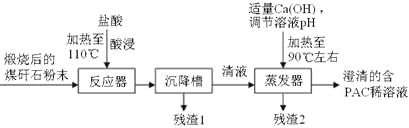
已知:聚合氯化铝([Al2(OH)nCl6-n]m(1≤n≤5,m≤10),商业代号PAC)是一种新型、高效絮凝剂和净水剂。
(1)酸浸的目的是___________________________;实验需要的500mL3.0 mol·L-1的盐酸,配制时所需要的玻璃仪器除量筒、烧杯、玻璃棒外还有______________________。
(2)若m=n=2,则生成PAC的化学方程式是_____________________。
(3)从含PAC的稀溶液中获得PAC固体的实验操作方法是_______、_________、_________。
(4)为了分析残渣2中铁元素的含量,某同学称取5.000g残渣2,先将其预处理使铁元素还原为Fe2+,并在容量瓶中配制成100mL溶液;然后移取25.00mL试样溶液,用1.000×10-2mol·L-1KMnO4标准溶液滴定,消耗标准溶液20.00mL。已知反应式为Fe2++MnO4-+H+—Fe3++Mn2++H2O(未配平)。判断滴定终点的依据是_______________________;残渣2中铁元素的质量分数为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是信息产业、太阳能电池光电转化的基础材料。锌还原四氯化硅是一种有着良好应用前景的制备硅的方法,该制备过程示意如下:

(1)焦炭在过程Ⅰ中作______剂。
(2)过程Ⅱ中的Cl2用电解饱和食盐水制备,制备Cl2的化学方程式是____。
(3)整个制备过程必须严格控制无水。
①SiCl4遇水剧烈水解生成SiO2和一种酸,反应的化学方程式是_____。
②干燥Cl2时,从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,然后再通入到浓H2SO4中。冷却的作用是____。
(4)Zn还原SiCl4的反应如下:
反应1: 400℃~756℃ ,SiCl4(g) + 2Zn(l)![]() Si(s) + 2ZnCl2(l) ΔH1<0
Si(s) + 2ZnCl2(l) ΔH1<0
反应2: 756℃~907℃ ,SiCl4(g) + 2Zn(l)![]() Si(s) + 2ZnCl2(g) ΔH2<0
Si(s) + 2ZnCl2(g) ΔH2<0
反应3: 907℃~1410℃,SiCl4(g) + 2Zn(g)![]() Si(s) + 2ZnCl2(g) ΔH3<0
Si(s) + 2ZnCl2(g) ΔH3<0
① 对于上述三个反应,下列说法合理的是_____。
a.升高温度会提高SiCl4的转化率 b.还原过程需在无氧的气氛中进行
c.增大压强能提高反应的速率 d.Na、Mg可以代替Zn还原SiCl4
② 实际制备过程选择“反应3”,选择的理由是____。
③ 已知Zn(l)=Zn(g) ΔH = +116 KJ/mol 。若SiCl4的转化率均为90%,每投入1mol SiCl4,“反应3”比“反应2”多放出_____kJ的热量。
(5)用硅制作太阳能电池时,为减弱光在硅表面的反射,采用化学腐蚀法在其表面形成粗糙的多孔硅层。腐蚀剂常用稀HNO3和HF的混合液。硅表面首先形成SiO2,最后转化为H2SiF6。用化学方程式表示SiO2转化为H2SiF6的过程_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分短周期元素原子半径与原子序数的关系如图所示.则下列说法正确的是( )
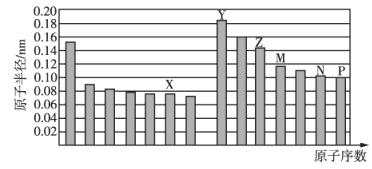
A.简单离子半径:![]()
B.简单氢化物的稳定性:![]()
C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D.Z的氧化物既能溶解于Y的最高价氧化物对应水化物的水溶液中,也能溶解于P的氢化物的水溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表回答下列有关问题.
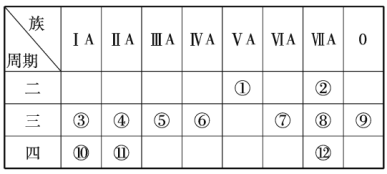
(1)写出下列元素符号:①______,⑥______,⑦______,______.
(2)这些元素中最活泼的金属元素是______(填元素符号,下同),最活泼的非金属元素是______,最不活泼的元素是______.
(3)这些元素的最高价氧化物对应的水化物中酸性最强的是______(填化学式,下同),碱性最强的是______,呈两性的氢氧化物是______,写出三者之间两两反应的化学方程式:______;______;______.
(4)这些元素(除0族元素外)中原子半径最小的是______(填元素符号,下同),原子半径最大的是______.
(5)在③与④中,单质的化学性质较活泼的是______(填元素符号),怎样用化学实验证明?______在⑧与中,单质的化学性质较活泼的是____________(填元素符号),怎样用化学实验证明?_____________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)写出乙烯分子的电子式:________。
(2)写出(2﹣甲基﹣1,3﹣丁二烯)的结构简式_____________。
(3)立方烷 ![]() 的一氯代物有__________种,它的六氯代物有________种。
的一氯代物有__________种,它的六氯代物有________种。
(4)下列物质的沸点按由高到低的顺序排列正确的是________。
①CH3(CH2)2CH3 ②CH3(CH2)3CH3 ③(CH3)3CH ④(CH3)2CHCH2CH3
A.②④①③ B.④②①③ C.④③②① D.②④③①
(5)下列选项中互为同系物的是________;互为同分异构体的是________;属于同种物质的是________。
①O2和O3 ②1H、2H、3H ③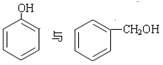 ④
④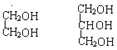 ⑤
⑤![]() ⑥戊烯和环戊烷 ⑦
⑥戊烯和环戊烷 ⑦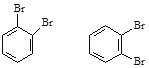
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用甲苯合成苯甲醛:
 ,
,
下列说法正确的是
A. 甲苯分子中所有原子都在同一平面内 B. 反应①②③的反应类型相同
C. 一氯甲苯的同分异构体有3种 D. 苯甲醇可与金属钠反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com