
【题目】某研究小组为探讨反应A(g)+2B(g) ![]() 2C(g)+D(s)在催化剂存在的条件下对最适宜反应条件进行了一系列的实验,并根据所得实验数据绘制出下图:图中C%为反应气体混合物中C的体积百分含量(所有实验的反应时间相同)。
2C(g)+D(s)在催化剂存在的条件下对最适宜反应条件进行了一系列的实验,并根据所得实验数据绘制出下图:图中C%为反应气体混合物中C的体积百分含量(所有实验的反应时间相同)。
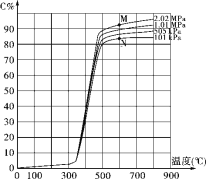
(1)该反应的反应热为ΔH_____0(填“>”、“<”或“=”)。
(2)点M和点N处平衡常数K的大小是:KM______KN(填“>”、“<”或“=”)。
(3)工业上进行该反应获得产品C的适宜条件是:度为______℃,选择该温度的理由是________________,压强为______,选择该压强的理由是__________________ 。
(4)试解释图中350℃前C%变化平缓而后急剧增大、500℃以后又缓慢增加的可能原因:_____________。
【答案】> = 500 低于500℃时,C%值太小,高于500℃时C%随温度的升高而增大的幅度不明显,但由于升温带来的燃料及设备成本要求会明显增加 101kPa 随着压强的增大,C%的增大幅度并不明显,而由于压强增大而带来的动力,设备成本的大幅度增加,故选择常压 该反应需要在特定的催化剂作用下才能顺利进行,而该催化剂只有在350℃以上才能体现催化活性并在500℃左右时催化效果最好,500℃以上的变化为温度变化导致平衡移动的情形
【解析】
试题(1)从图像看出,随着温度升高,C%增大,说明温度升高平衡向正反应方向移动,则反应是吸热反应,所以△H>0。(2)平衡常数只和温度有关,M、N两点所处的温度相同,故KM=KN。(3)获得产品C 的适宜条件是:温度为500℃,因为低于500℃时,C%值太小,高于500℃时C%随温度的升高而增大的幅度不明显,但由于升温带来的燃料及设备成本要求会明显增加。压强选择:101k Pa,是因为:随着压强的增大,C%的增大幅度并不明显,而由于压强增大而带来的动力,设备成本的大幅度增加,故选择常压。(4)350℃前C%变化平缓而后急剧增大、500℃以后又缓慢增加的可能原因是:该反应需要在特定的催化剂作用下才能顺利进行,而该催化剂只有在350℃以上才能体现催化活性并在500℃左右时催化效果最好,500℃以上的变化为温度变化导致平衡移动的情形。


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】下列各图象能正确反映其对应操作中各量变化关系的是 ( )
A.  用一定质量的高锰酸钾加热制氧气
用一定质量的高锰酸钾加热制氧气
B.  向一定质量的石灰石中加入过量的稀盐酸
向一定质量的石灰石中加入过量的稀盐酸
C.  向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
D.  分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量
分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在25℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,则该反应的燃烧热的热化学方程式应为_________________。
(2)化学反应的焓变与反应物和生成物的键能有关。所谓键能就是:在101kPa、298 K时,断开1 mol气态AB为气态A、气态B时过程的焓变,用ΔH298(AB)表示;断开化学键时ΔH>0[如H2(g)=2H(g) ΔH= +436 kJ·mol-1],形成化学键时ΔH<0[如2H(g)=H2(g) ΔH= - 436 kJ·mol-1]。
已知:H2(g)+Cl2(g)=2HCl(g) ΔH= -185 kJ·mol-1 ΔH298(H2)=+ 436 kJ·mol-1 ,ΔH298(Cl2)= +247 kJ·mol-1则ΔH298(HCl)=__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热值是指一定条件下单位质量的物质完全燃烧所放出的热量。已知H2(g)、CO(g)和CH3OH(l)的热值分别为143 kJ· g-1、10 kJ·g-1和23 kJ·g-1。请回答下列问题:
(1)写出CO燃烧反应的热化学方程式为__________________________________________。
(2)表示甲醇燃烧热的热化学方程式为__________________________________________。
(3)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为__________________________。
(4)白磷与氧可发生如下反应:P4(g)+5O2(g)![]() P4O10(g)。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ/mol、P—O b kJ/mol、P=O c kJ/mol、O=O d kJ/mol根据图示的分子结构和有关数据计算该反应的反应热_____________。
P4O10(g)。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ/mol、P—O b kJ/mol、P=O c kJ/mol、O=O d kJ/mol根据图示的分子结构和有关数据计算该反应的反应热_____________。
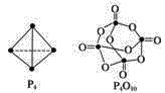
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO- + H+
CH3COO- + H+
(1)某温度时,0.1 mol·L-1的醋酸溶液中的c(H+) 与0.01 mol·L-1的醋酸溶液中的c(H+)的比值______(填“大于”“小于”或“等于”)10。
(2)已知:25 ℃时,该电离平衡的平衡常数为1.75×10-5。
①求该温度时,a mol·L-1的醋酸溶液中c1(H+)=________________mol·L-1 (用含a的代数式表示)。[提示:此时电离度比较小,进行简化计算,平衡时c(CH3COOH)可用初始浓度代替,水电离出的c(H+)、c(OH-)忽略不计,下同]
②若该温度时向该溶液中加入一定量的CH3COONH4(假设溶液体积不变),使溶液中c(CH3COO-)为b mol·L-1,则此时c2(H+)=____________________mol·L-1(用含a、b的代数式表示)。
③c1(H+)________(填“大于”“小于”或“等于”)c2(H+)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,发生反应:①M(s)+N(g) R(g) ΔH= - Q1 kJ/mol
②2 R(g)+N(g) 2T(g) ΔH= - Q2 kJ/mol(已知Q1、Q2、Q3均为正值)
下列说法正确的是
A. 1molR(g)的能量总和大于1molM(s)与1molN(g)的能量总和
B. 将2mol R(g)与1molN(g)充分混合,在一定条件下充分反应,放出热量Q2 kJ
C. 当1molM(s)完全转化为T(g)时(假定无热量损失),放出热量(Q1+0.5Q2)kJ
D. M(g)+N(g) R(g) ΔH= - Q3 kJ/mol,则Q3 < Q1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T1时,将气体X和气体Y各1.6mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g),一段时间后达到平衡。反应过程中测定的数据如表:下列说法正确的是
2Z(g),一段时间后达到平衡。反应过程中测定的数据如表:下列说法正确的是
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 1.2 | 1.1 | 1.0 | 1.0 |
A. 反应0~4 min的平均速率υ(Z)=0.25 mol/(Lmin)
B. T1时,反应的平衡常数K1=1.2
C. 其他条件不变,9 min后,向容器中再充入1.6 molX,平衡向正反应方向移动,再次达到平衡时X的浓度减小,Y的转化率增大
D. 其他条件不变,降温到T2达到平衡时,平衡常数K2=4,则此反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】防治雾霾天气的主要措施有机动车临时交通管制、工矿企业停业限产、扬尘污染控制等。
(1)PM2.5是环保部门监测空气质量的重要指标。将某PM2.5样本用蒸馏水处理制成待测试样,测得试样中无机离子(OH-忽略不计)的种类和平均浓度如下表:
离子种类 | Na+ | NH4+ | SO42- | NO3- |
浓度(mol/L) | 2.0×10-6 | 2.8×10-5 | 3.5×10-5 | 6.0×10-5 |
则试样的pH为________________________。
(2)一定条件下,以CO和H2合成清洁能源CH3OH,其热化学方程式为CO(g)+2H2(g) CH3OH(g) ΔH,CO的平衡转化率与温度、压强的关系如图所示:

①该可逆反应的ΔH__________0(填“>”“<”或“=”)。A、B、C三点对应的平衡常数KA、KB、KC的大小关系是______________。压强:p1__________p2(填“>”“<”或“=”)。在T1条件下,由D点到B点过程中,正、逆反应速率之间的关系:v(正)___________v(逆)(填“>”“<”或“=”)。
②若在恒温恒容条件下进行上述反应,能表示该可逆反应达到平衡状态的是_________(填字母)。
A.CO的体积分数保持不变
B.容器内混合气体的密度保持不变
C.容器内混合气体的平均摩尔质量保持不变
D.单位时间内消耗CO的浓度等于生成CH3OH的浓度
③向恒压密闭容器中充入2 mol CO和4 mol H2,在p2、T2条件下达到平衡状态C点,此时容器容积为2 L,则在该条件下反应的平衡常数K为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别调节0.01mol·L-1HCOOH溶液、0.01mol·L-1氨水的pH,系统中微粒浓度的负对数值(-lgc)与pH的关系分别如下图所
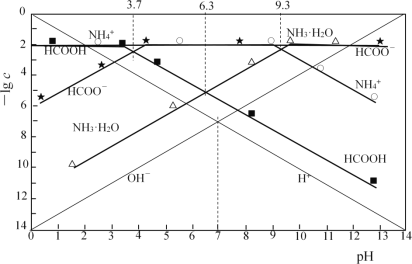
下列说法错误的是
A. 25℃时,NH3·H2O![]() NH4++OH-的lgK=-4.7
NH4++OH-的lgK=-4.7
B. 25℃时,0.01mol·L-1HCOOH溶液的pH为3.7
C. HCOONa溶液中加入NH4Cl至溶液呈中性:c(Cl-)>c(Na+)>c(HCOO-)
D. HCOONa溶液中加入KHSO3至溶液呈中性:c(HCOOH) +c(H2SO3) = c(SO32-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com