
【题目】锌与浓硫酸反应,随着硫酸的浓度下降,产生的气体中混有H2,为证实相关分析,化学小组的同学设计了如图所示的实验装置,对反应后的气体(X)取样进行组分分析(遇有气体吸收过程,视为完全吸收)。
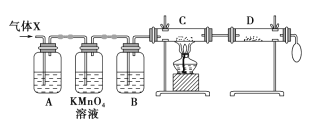
(1)A中加入的试剂可能是_________,KMnO4 溶液的作用是_________,若高锰酸钾溶液与B 之间不再添加装置,请描述观察到何种现象能表明已达到使用高锰酸钾溶液的目的_______________。
(2)可证实气体 X 中混有较多氢气的实验现象是:C中 _____________,D中______________。
【答案】 品红溶液 吸收过量SO2 高锰酸钾溶液颜色变浅,但没有褪成无色 C中黑色粉末变红色 D中白色粉末变蓝色
【解析】锌和浓硫酸反应生成硫酸锌,二氧化硫和水,浓硫酸随反应进行浓度变小后,稀硫酸和锌反应生成氢气,因此气体X中含有二氧化硫和氢气。因二氧化硫具有漂白性,所以A中加入的试剂可能是品红试液,作用是检验SO2的存在;酸性高锰酸钾溶液的目的是吸收生成的二氧化硫气体,则B装置中加浓硫酸吸收气体中的水分,装置C将残留的气体通过灼热的氧化铜反应,目的是验证该气体具有还原性,装置D无水硫酸铜检验水,若变蓝色则C装置反应生成水。
(1)根据上述分析,A中加入的试剂可能是品红试液;酸性高锰酸钾溶液的目的是吸收过量的二氧化硫气体,若高锰酸钾溶液与B 之间不再添加装置,应该看到高锰酸钾溶液颜色变浅,但没有褪成无色,说明二氧化硫全部纯净,故答案为:品红溶液;吸收过量SO2;高锰酸钾溶液颜色变浅,但没有褪成无色;
(2)由以上分析得,装置C中所装药品为CuO;若看到C中黑色粉末变为红色,D中的白色固体变为蓝色,可以证实气体X中混有较多的氢气,故答案为:C中黑色粉末变红色;D中白色粉末变蓝色。


科目:高中化学 来源: 题型:
【题目】Ni-MH电池在工农业生产和日常生活中具有广泛用途,废旧电池中含有大量金属元素,其回收利用具有非常重要的意义。一种利用废Ni-MH电池正极材料(主要含有Ni(OH)2,还含有少量Fe、Cu、Ca、Mg、Mn、Zn的氢氧化物)制备电子级硫酸镍晶体的工艺流程如下图所示:

回答下列问题:
(1)“浸出”时温度、硫酸浓度、浸出时间对镍浸出率的影响如下图:
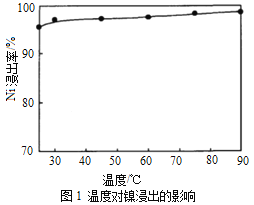
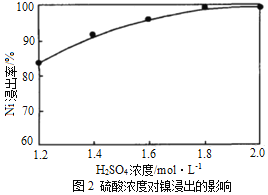
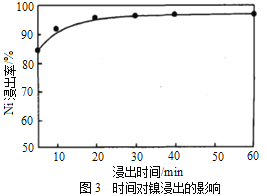
则“浸出”时最适宜的条件为_______________。
(2)在“滤液1”中加入双氧水可将Fe2+转化为难溶的针铁矿(FeOOH),写出反应的离子方程式:______________。
(3)“滤液2”中加入NaF可将滤液中Ca2+、Mg2+转化为难溶的CaF2和MgF2。当加入过量NaF后,所得“滤液3”中c(Mg2+)∶c(Ca2+)=0.67,则MgF2的溶度积为_____________[已知Ksp(CaF2)=1.10×10-10]。
(4)向“滤液3”中加入(NH4)2S2O8可以除锰,在此过程中(NH4)2S2O8与MnSO4反应生成含锰元素的一种黑色不溶物、硫酸铵及硫酸,写出该反应的化学方程式___________________。
(5)向“滤液4”加入有机萃取剂后,Zn2+与有机萃取剂(用HA表示)形成易溶于萃取剂的络合物ZnA2·2HA。该过程可以表示为:Zn2++4HA![]() ZnA2·2HA+2H+
ZnA2·2HA+2H+
①已知加入萃取剂后,锌的萃取率随料液pH变化如图所示。试分析pH增大时,锌的萃取率逐渐增大的原因是___________________。
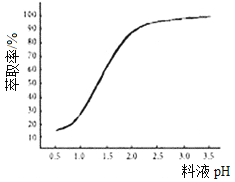
②“操作X”的名称是_____________。
(6)上述回收镍的过程中,使用了1kg含镍37.1%的正极材料,最终得到纯净的NiSO4·7H2O1.686kg,则镍的回收率为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞是一种治疗急性脑缺血的药物,部分合成流程如下。下列说法正确的是( )

A. 化合物X、Y和丁苯酞三种分子中各含有1个手性碳原子
B. 化合物Y可以发生取代、加成和加聚反应
C. 可用Na2CO3溶液鉴别化合物X和化合物Y
D. 化合物X、Y和丁苯酞各1 mol最多消耗NaOH的量均为1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
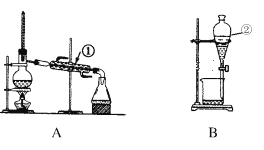

(1)从氯化钾溶液中得到氯化钾固体,选择装置________ (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置________。
(2)将溴的四氯化碳溶液和水分离开选择的装置是___________,下列是进行该操作的步骤,正确的顺序是____________。
①将混合物倒入分液漏斗中,并放在铁架台的铁圈上静置,分层;
②从分液漏斗上口倒出上层溶液
③将分液漏斗的玻璃塞打开或使玻璃塞上的凹槽对准漏斗颈部的小孔
④分液漏斗下面导管紧贴烧杯内壁,旋开活塞,用烧杯接收溶液
⑤检查分液漏斗活塞和颈部的玻璃塞是否漏水
(3)装置A中①的名称是______________,进水的方向是从________口进水。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为2KNO3+S+3C=K2S+N2↑+3CO2↑,该反应中被还原的元素是( )
A.C
B.N
C.N和S
D.N和C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等质量的 SO2气体和 SO3气体相比较,正确的说法是
A. 密度比为 4:5 B. 物质的量之比为 4:5
C. 体积比为 1:1 D. 原子数之比为 3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列说法不正确的是( )
A. 向滴有酚酞的Na2CO3溶液中加BaCl2固体,溶液红色变浅,则说明溶液中存在Na2CO3的水解平衡
B. 0.01mol/LCH3COOH溶液pH>2,说明CH3COOH为弱电解质
C. 含1molNH3H2O的溶液中加入HCl溶液,放出的热量小于57.3kJ,说明NH3H2O为弱电解质
D. 10mLpH=5的NH4Cl溶液稀释至1L,pH<7,则说明NH4Cl为弱电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com