
����Ŀ����Ҫ��ش��������⣺
��.ij�¶��£�һ��10L�ĺ����ܱ������У�X��Y��Z��Ϊ���壬�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ��������գ�
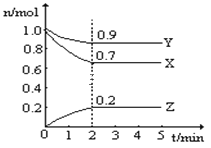
��1���÷�Ӧ�Ļ�ѧ����ʽΪ___��
��2����Ӧ��ʼ��2min��������Z��ʾ��ƽ����Ӧ����Ϊ___��
��.�ں��º��ݵ��ܱ������У����������������ٷ����仯ʱ��
����������ѹǿ�����������ܶ����������������ʵ���������������ɫ����������ƽ����Է�������������Ӧ���������ķ�Ӧ����֮�ȵ��ڻ�ѧ������֮��
һ����֤��2SO2(g)+O2(g) ![]() 2SO3(g)�ﵽƽ��״̬����__������ţ�
2SO3(g)�ﵽƽ��״̬����__������ţ�
��.��6molA������2molB������2L�ܱ������л�ϲ���һ�������·�����Ӧ��3A��g��+B��g��![]() xC��g��+2D��g��������5min��Ӧ�ﵽƽ��״̬�������ڵ�ѹǿ��С����֪D��ƽ����Ӧ����Ϊ0.2mol/��L��min��������д���пհף�
xC��g��+2D��g��������5min��Ӧ�ﵽƽ��״̬�������ڵ�ѹǿ��С����֪D��ƽ����Ӧ����Ϊ0.2mol/��L��min��������д���пհף�
��x����ֵΪ__��
��5minʱB��ת����Ϊ__��
���������¶ȣ�V��__���������������С����������������
���𰸡�3X+Y![]() Z 0.01mol/(L��min) �٢ۢ� 1 50% ���
Z 0.01mol/(L��min) �٢ۢ� 1 50% ���
��������
��1����ͼ֪��X��Y�����ʵ����ֱ����0.3mol��0.1mol��˵��X��Y�Ƿ�Ӧ�Z�����ʵ�������0.2mol��Z����������ݻ�ѧ����ʽ�и����ʵ����ʵ����ĸı���֮�ȵ��ڻ�ѧ������֮�ȣ����Ը÷�Ӧ�Ļ�ѧ����ʽΪ3X+Y![]() 2Z����Ϊ��3X+Y
2Z������3X+Y![]() Z��
Z��
��2����Ӧ��ʼ��2min������Z��Ũ������![]() =0.02mol/L��
=0.02mol/L��![]() =
=![]() =0.01 mol/(L��min)������0.01mol/(L��min)��
=0.01 mol/(L��min)������0.01mol/(L��min)��
��.��1�����ڷ�Ӧ2SO2(g)+O2(g)![]() 2SO3(g)��
2SO3(g)��
������Ӧ�����������С�ķ�������������ѹǿ���䣬��������������䣬��Ӧ�ﵽƽ��״̬��
����Ӧ�ں��������н��У��ҷ�Ӧ�ﶼΪ���壬���������ܶ�ʼ�ղ��䣬�ܶȲ��䲻һ���ﵽƽ��״̬��
����Ϊ��Ӧǰ������ķ��������ȣ����Ե��������������ʵ������ٷ����仯ʱ����Ӧ��ƽ��״̬��
����Ӧ�ﶼΪ��ɫ���壬����������ɫʼ�ղ��䣬��ɫ���䲻һ���ﵽƽ��״̬��
������![]() =
=![]() ����Ӧ����������ʼ�ղ��䣬����������ƽ����Է����������䣬�������ʵ������䣬�����֤����ƽ��״̬��
����Ӧ����������ʼ�ղ��䣬����������ƽ����Է����������䣬�������ʵ������䣬�����֤����ƽ��״̬��
����Ӧ���ж��ǰ�����Ӧ���������ķ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ����Ƿ�ﵽƽ��״̬�ء�
�ۺ����Ϸ������٢ۢ��������⡣
��Ϊ���٢ۢ���
��.���ﵽƽ��ʱ�������ڵ�ѹǿ��С������x+2��3+1����xΪ����������x=1����Ϊ��1��
��ƽ��ʱ�����ɵ�D�����ʵ���Ϊ0.2mol/��L�qmin����5min��2L=2mol�����ݻ�ѧ����ʽ����2molD����Ҫ����1molB��B��ת����Ϊ![]() ��100%=50%����Ϊ��50%��
��100%=50%������50%��
�������¶ȣ���������Ӧ���ʻ����淴Ӧ���ʶ�����V�����Ϊ�����


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ϡ��ˮ�д��ڵ���ƽ��NH3��H2O ![]() NH4+��OH��������������ȷ����
NH4+��OH��������������ȷ����
A.��ˮϡ�ͺ���Һ��c (H+)��С
B.ͨ������HCl(g)����Һ��c(NH4+)��С
C.��������Ũ��ˮ������ƽ�������ƶ�
D.��������NH4Cl���壬��Һ��pH��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ZYX4���ڻ�������������ҪӦ�ü�ֵ�����ӻ��������ʽ��ͼ��ʾ��X��Y��Z��ԭ��������������Ķ�����Ԫ�أ�����ֻ��һ��Ϊ����Ԫ�أ�X�����ڱ���ԭ�Ӱ뾶��С��Ԫ�ء����������д������ ( )

A.Z�Ƕ�����Ԫ���н�������ǿ��Ԫ��
B.Y������������Ӧˮ�����������
C.X��Y�����γɷ���ʽΪYX3���ȶ�������
D.������ZYX4��ǿ��ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.�ںϳɰ���ҵ�У�����NH3����������Ӧ���ʣ����ԭ��ת����
B.�����½��еķ�Ӧ2NO2(g)![]() N2O4(g)��ƽ��ʱ���ݻ��������2mol��NO2�����ٴδﵽƽ��ʱNO2�����������ԭƽ���
N2O4(g)��ƽ��ʱ���ݻ��������2mol��NO2�����ٴδﵽƽ��ʱNO2�����������ԭƽ���
C.�����£�MgO(s)��C(s)��Mg(s)��CO(g)�����Է����У������H��0
D.������pH=2����������H2O�������c(H��)��1.0��10��2mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���ʵ��������������ó��Ľ�����ȷ����
ѡ�� | ʵ����������� | ���� |
A | ��FeBr2��Һ��ͨ������Cl2����Һ��dz��ɫ��Ϊ��ɫ | Cl2������ǿ��Br2 |
B | �����£������pH��3��HA��HB������ֱ��ˮϡ�ͣ���Һ����������ͼ
| HA���Ա�HB�� |
C | ������SO2��BaCl2��Һ��ͨ������X�����ְ�ɫ���� | X���������� |
D | ȡ���õ�Na2O2��ĩ�������еμӹ��������ᣬ������ɫ���� | ����Ϊ���� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2002��ŵ������ѧ������ߵĹ���֮һ�Ƿ����˶��л�����ӽ��нṹ�������������䷽�����ü������ģ�10��9g��������ͨ�������ǵ����ӻ���ʹ��Ʒ���Ӵ������ӻ��������������ѳɸ�С�����ӡ���C2H6���ӻ���ɵõ�C2H6����C2H5����C2H4��������Ȼ��ⶨ���ʺɱȡ�ij�л�����Ʒ���ʺɱ�����ͼ��ʾ���������Ӿ���һ����λ����ɣ��ź�ǿ��������ӵĶ����йأ�������л���������� ��
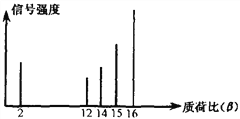

A. �״� B. ���� C. ���� D. ��ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��Ȼ�ѧ����ʽ��������ȷ����( )
A. ��֪�����ȼ����Ϊ890.3kJmol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪCH4(g)+2O2(g)�TCO2(g)+2H2O(g)��H=-890.3kJmol-1
B. ��֪C(ʯī��s)�TC(���ʯ��s)��H��0������ʯ��ʯī�ȶ�
C. ��֪�к���Ϊ��H=-57.4kJmol-1����1molϡ���������ϡNaOH��Һ��Ӧ�ķ�Ӧ�Ⱦ����к���
D. ��֪S(g)+O2(g)�TSO2(g)��H1��S(s)+O2(g)�TSO2(g)��H2�����H1����H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ģ�����a mol FeBr2����Һ�У�ͨ��x mol Cl2�����и���Ϊͨ��Cl2�����У���Һ�ڷ�����Ӧ�����ӷ���ʽ�����в���ȷ���� (����)
A. x��0.6a��2Br����Cl2===Br2��2Cl��
B. x��0.4a��2Fe2����Cl2===2Fe3����2Cl��
C. x��a��2Fe2����2Br����2Cl2===Br2��2Fe3����4Cl��
D. x��1.5a��2Fe2����4Br����3Cl2===2Br2��2Fe3����6Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵��������ǣ� ��
A.�ö��Ե缫��� Na2SO4��Һ���� 2 mol����ת��ʱ,�ɼ��� 18 g ˮ�ָ�
B.�ö��Ե缫��� CuSO4��Һ��������1 mol Cu(OH)2�ָ����ǰŨ��ʱ����·��ת����4mol e��
C.��Mg��Al��������NaOH��Һ�����ԭ��أ�Mg��������Al������
D.Ҫ��ʵ�� Cu��H2SO4(ϡ) �T CuSO4��H2���ķ�Ӧ�����ڵ����н��У��� Cu Ϊ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com