
【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向FeBr2溶液中通入适量Cl2,溶液由浅绿色变为黄色 | Cl2氧化性强于Br2 |
B | 常温下,等体积pH=3的HA和HB两种酸分别加水稀释,溶液导电能力如图
| HA酸性比HB弱 |
C | 向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀 | X具有氧化性 |
D | 取久置的Na2O2粉末,向其中滴加过量的盐酸,产生无色气体 | 气体为氧气 |
A.AB.BC.CD.D
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】某小组依据氧化还原反应:2Ag+(aq)+Cu(s)==Cu2+(aq)+2Ag(s)设计的原电池如图所示,下列说法正确的是
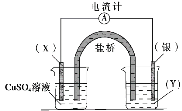
A.电极X可以是碳棒也可以是银棒
B.盐桥中的阳离子流向CuSO4溶液所在烧杯
C.银电极为电池的负极,发生的电极反应为Ag-e-=Ag+
D.外电路中电流的方向是从银电极流向X电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为_________________
(2)反应开始至2 min,气体Z的平均反应速率为___________。
(3)若X、Y、Z均为气体,反应达到平衡时
①压强是开始时的_________倍;
②若此时将容器的体积缩小为原来的![]() 倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为_________(填“放热”或“吸热”)反应。
倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为_________(填“放热”或“吸热”)反应。
(4) 25°C时,pH=2的盐酸和醋酸各1mL分别加水稀释,pH随溶液体积变化的曲线如下图所示。请回答如下问题

①曲线_________(填“Ⅰ”或“Ⅱ”)代表盐酸的稀释过程
②a溶液的导电性比c溶液的导电性_________(填“强”或“弱”)
③将a、b两溶液加热至30°C,c(Cl-)/c(CH3COO-)_________(填“变大”、“变小”或“不变”)
④设稀释前的醋酸电离度为0.1%,醋酸的电离常数Ka=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的反应:X(g) + Y(g)![]() 2Z(g),下列说法能充分说明该反应已达到化学平衡状态的是 ( )
2Z(g),下列说法能充分说明该反应已达到化学平衡状态的是 ( )
A.X、Y、Z的浓度相等B.正、逆反应速率均等于零
C.X、Y、Z在容器中共存D.X、Y、Z的浓度均不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量混合物在密闭容器中发生反应:mA(g)+nB(g)![]() pC(g)达平衡后,将气体体积缩小到原来的1/2,当达到新的平衡时,B物质的浓度为原来的1.9倍,若压缩过程中保持温度不变,则下列说法正确的是
pC(g)达平衡后,将气体体积缩小到原来的1/2,当达到新的平衡时,B物质的浓度为原来的1.9倍,若压缩过程中保持温度不变,则下列说法正确的是
A.m+n<pB.平衡向逆反应方向移动C.A的转化率降低D.C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
Ⅰ.某温度下,一个10L的恒容密闭容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
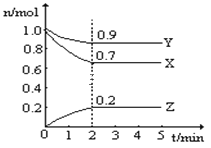
(1)该反应的化学方程式为___;
(2)反应开始至2min,以气体Z表示的平均反应速率为___;
Ⅱ.在恒温恒容的密闭容器中,当下列物理量不再发生变化时:
①混合气体的压强②混合气体的密度③混合气体的总物质的量④混合气体的颜色⑤混合气体的平均相对分子质量⑥各反应物或生成物的反应速率之比等于化学计量数之比
一定能证明2SO2(g)+O2(g) ![]() 2SO3(g)达到平衡状态的是__(填序号)
2SO3(g)达到平衡状态的是__(填序号)
Ⅲ.将6molA气体与2molB气体在2L密闭容器中混合并在一定条件下发生反应:3A(g)+B(g)![]() xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L·min),请填写下列空白:
xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L·min),请填写下列空白:
①x的数值为__;
②5min时B的转化率为__;
③若升高温度,V逆__(填“变大”“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TiCl3是烯烃定向聚合的催化剂、TiCl4可用于制备金属Ti。
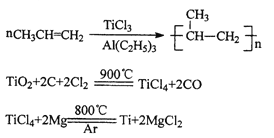
(1)Ti3+的基态核外电子排布式为__________
(2)丙烯分子中,碳原子轨道杂化类型为__________
(3)Mg、Al、Cl第一电离能由大到小的顺序是___________
(4)写出一种由第2周期元素组成的且与CO互为等电子体的阴离子的电子式________
(5)TiCl3浓溶液中加入无水乙醚,并通入HCl至饱和,在乙醚层得到绿色的异构体,结构式分别是[Ti(H2O)6]Cl3、[Ti(H2O)5Cl]Cl2·H2O。1mol[Ti(H2O)6]Cl3中含有σ键的数目为______.
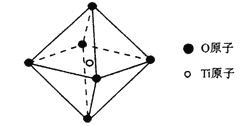
(6)钛酸锶具有超导性、热敏性及光敏性等优点,该晶体的晶胞中Sr位于晶胞的顶点,O位于晶胞的面心,Ti原子填充在O原子构成的正八面体空隙的中心位置,据此推测,钛酸锶的化学式为_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
![]() A. 向含有CaCO3沉淀的水中通入CO2 至沉淀恰好溶解,再向溶液中加入NaHCO3 饱
A. 向含有CaCO3沉淀的水中通入CO2 至沉淀恰好溶解,再向溶液中加入NaHCO3 饱
和溶液,又有CaCO3沉淀生成
B. 向Na2 CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2 CO3的物质的量之比为1:2.
C. 等质量的NaHCO3和Na2 CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
D. 向Na2 CO3饱和溶液中通入CO2,有NaHCO3结晶析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO![]() 2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/mol/L | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
c(CO)/mol/L | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H______0(填写“>”、“<”、“=”。
(2)前2s内的平均反应速率v(N2)=_____________。
(3)在该温度下,反应的平衡常数K=______________。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是_____。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
实验编号 | T/℃ | NO初始浓度mol/L | CO初始浓度mol/L | 催化剂的比表面积m2/g |
Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
Ⅱ | 124 | |||
Ⅲ | 350 | 124 |
①请在上表格中填入剩余的实验条件数据________________。
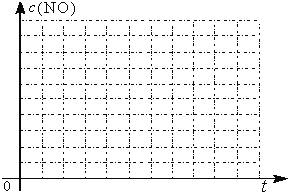
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com