
【题目】298K时,向20mL 0.1mol/L某酸HA溶液中逐滴加入0.1mol/LNaOH溶液,混合溶液的pH变化曲线如图所示。下列说法错误的是
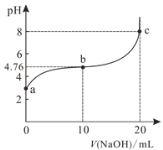
A.a点溶液的pH为2.88
B.b点溶液中:c(Na+)>c(A-)>c(HA)
C.b、c之间一定存在c(Na+)=c(A-)的点
D.a、b、c三点中,c点水的电离程度最大
【答案】B
【解析】
A.当加入10mL0.1mol/LNaOH溶液时,溶液中c(HA)=c(A-) ,由HAH++A-可知Ka=![]() =c(H+)=10-4.76,则0.1mol/L的某酸HA中的c(H+)可用三段式进行计算,设电离的c(HA)为xmol/L:
=c(H+)=10-4.76,则0.1mol/L的某酸HA中的c(H+)可用三段式进行计算,设电离的c(HA)为xmol/L:

HA的电离平衡常数K=![]() =
=![]() =10-4.76,剩余的c(HA)=0.1-x≈0.1mol/L,解得x=10-2.88,所以a点溶液的pH为2.88,A正确;
=10-4.76,剩余的c(HA)=0.1-x≈0.1mol/L,解得x=10-2.88,所以a点溶液的pH为2.88,A正确;
B.b溶液显酸性,c(H+)>(OH-),由电荷守恒可知c(Na+)<c(A-),B错误;
C.溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(A-),当溶液pH=7呈中性时c(H+)=c(OH-),则c(Na+)=c(A-),所以b、c之间一定存在c(Na+)=c(A-)的点,C正确;
D.a、b点中溶液显酸性, HA电离出的H+对水的电离起抑制作用,c点酸碱恰好完全反应生成盐NaA,对水的电离起促进的作用,所以a、b、c三点中,c点水的电离程度最大,D正确;
答案选B。


科目:高中化学 来源: 题型:
【题目】某二元酸H2A在水溶液中发生电离:H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++A2-。下列叙述不正确的是( )
H++A2-。下列叙述不正确的是( )
A. 在NaHA溶液中一定是:c(Na+)>c(HA-)>c(OH-)>c(H+)
B. 在Na2A溶液中一定是:c(Na+)>c(A2-)>c(OH-)>c(H+)
C. 在NaHA溶液中一定是:c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-)
D. 在H2A溶液中一定是:c(H+)=c(HA-)+2c(A2-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行如下实验,研究化学反应中的热量变化。

请回答下列问题:
(1)反应后①中温度升高,②中温度降低。由此判断铝条与盐酸的反应是________反应(填“放热”或“吸热”,下同),Ba(OH)2·8H2O与NH4Cl的反应是________反应。
(2)1.00L 1.00mol/L H2SO4溶液与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,该反应的中和热为______,表示其中和热的热化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类或归类正确的一组是( )
①液氨、液氧、干冰、纯碱均为化合物 ②盐酸、氢氧化铁胶体、空气、氨水均为混合物 ③氢氧化钾、小苏打、硫酸、烧碱均为电解质 ④碘酒、牛奶、豆浆、肥皂水均为胶体 ⑤![]() 、
、![]() 、
、![]() 、
、![]() 均为钠盐
均为钠盐
A.①和②B.②和③C.②和④D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科学技术的发展,阿伏加德罗常数的测定手段越来越多,测定的精度也越来越高。现有一种简单可行的测定方法,具体步骤为:
①准确称取mg干燥后的NaCl固体细粒并转移到定容仪器A中;
②用滴定管向A仪器中加苯,不断振荡,继续加苯到A仪器的刻度,
计算出NaCl固体的体积V cm3。
(1)步骤①中仪器A最好使用_______________(填序号)
A.量筒 B.烧杯 C.容量瓶 D.试管
(2)步骤②中是否用酸式滴定管还是用碱式滴定管_____________,理由是__________。
(3)能否用水代替苯_________,理由是_____________________。
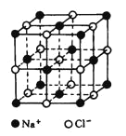
(4)已知NaCl晶体中,靠得最近的Na+、Cl-间的距离为a cm(如图),则用上述方法测得的阿伏加德常数NA的表达式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在古代,橘红色的铅丹(Pb3O4)用于入药和炼丹,人们对其中重金属铅的毒性认识不足。已知:PbO2为棕黑色粉末。某化学兴趣小组对铅丹的一些性质进行实验探究并测定其组成。
回答下列问题:
(1)性质实验
实验操作 | 现象 | 解释或结论 |
①将适量铅丹样品放入小烧杯中,加入2mL6mol/L的HNO3溶液,搅拌 | _____ | Pb3O4+4HNO3=PbO2+ 2Pb(NO3)2+2H2O |
②将上述混合物过滤,所得滤渣分为两份,一份加入2mL浓盐酸,加热 | 有刺激性的黄绿色气体产生 | 反应的化学方程式: _______ |
③另一份滤渣加入硝酸酸化的Mn(NO3)2溶液,搅拌 | 得紫色溶液 | 结论:_______ |
(2)组成测定
①准确称取0.530g干燥的铅丹样品,置于洁净的小烧杯中,加入2mL6mol/L的HNO3溶液,搅拌使之充分反应,分离出固体和溶液。该分离操作名称是_____________。
②将①中所得溶液全部转入锥形瓶中,加入指示剂和缓冲溶液,用0.04000mol/L的EDTA溶液(显酸性)滴定至终点,消耗EDTA溶液36.50mL。EDTA与Pb2+的反应可表示为Pb2++H2Y2-=PbY2-+2H+,滴定时EDTA溶液应盛装在_______________中。滤液中含Pb2+__________mol。
③将①中所得固体PbO2全部转入另一锥形瓶中,往其中加入适量HAc与NaAc的混合液和8g固体 KI,摇动锥形瓶,使PbO2全部反应而溶解,发生反应PbO2+4I-+4HAc =PbI2+I2+4Ac-+2H2O,此时溶液呈透明棕色。以0.05000mol/L的Na2S2O3标准溶液滴定,发生反应I2+2S2O32-=S4O62-+2I-,至溶液呈淡黄色时加入2%淀粉溶液1mL,继续滴定至溶液_______,即为终点,用去Na2S2O3溶液30.80mL。
根据②、③实验数据计算,铅丹中Pb(Ⅱ)与Pb(Ⅳ)的原子数之比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素的原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍。请回答下列问题:
(1)F的基态原子价电子排布式为____________________ 。
(2)B、C、D、E的原子的第一电离能由小到大的顺序为_______________(用元素符号回答)
(3)下列关于B2A2分子和A2D2分子的说法正确的是______________
A 分子中都含有σ键和π键
B 中心原子都sp杂化
C 都是含极性键和非极性键的非极性分子
D 互为等电子体
E.B2A2分子的沸点明显低于A2D2分子
(4)F2+能与BD分子形成[F(BD)4]2+,其原因是BD分子中含有_________
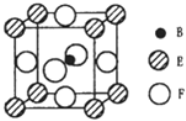
(5)由B、E、F三种元素形成的一种具有超导性的晶体,晶胞如图所示.B位于E和F原子紧密堆积所形成的空隙当中.与一个F原子距离最近的F原子的数目为_________,该晶体的化学式为_______.若该晶体的相对分子质量为M,阿伏加德罗常数为NA,B、E、F三种元素的原子半径分别为r1pm、r2pm、r3pm,则该晶体的密度表达式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据VSEPR模型判断,下列微粒中所有原子都在同一平面上的是( )
A. SO32- 和NO2-B. NO3- 和SO32-C. ![]() 和ClO3-D. PO43- 和SO32-
和ClO3-D. PO43- 和SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对矿井下空气进行氧气含量测定既能保证矿工的身体健康又能为瓦斯灾害处理提供数据。缺氧场所常采用伽伐尼电池型氧传感器检测氧气浓度,该传感器结构如图所示,工作电极为Pb,对比电极为Pt,电池液为KOH溶液。下列说法不正确的是

A.氧在对比电极被还原
B.工作电极的电极反应为Pb+2OH--2e-=Pb(OH)2
C.外电路电子由对比电极流向工作电极
D.该传感器测定氧气浓度时不需外加电源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com