
����Ŀ������������һ�ֳ�����ʳƷ���Ӽ���Ϊ����ijʳƷ���������κ�����ͨ����1kg��Ʒ�к�SO2�����ƣ���ij�о�С��ͬѧ���������ʵ�鷽����
I.��ȡ��ƷWg���������ϡ���
II.��I�в�����SO2������H2O2��Һ���գ�
III.��II������Һ��0.lmolL-1����������Һ�ζ����������ΪVmL��
IV.���ݴ�����
������С��ͬѧ��ʵ�����ơ����������ݴ�����������ȷ����( )
A.����I�п���ϡ�������ϡ����
B.1kg��Ʒ�к�SO2������Ϊ![]() g
g
C.��������ˮ���滻II�е���������H2O2��Һ�����Բⶨ�����Ӱ��
D.����I�����ɵ�SO2������װ����δ��H2O2��Һ���գ����ܵ��²���������κ���ƫ��
���𰸡�D
��������
I.�з�����Ӧ��![]() ��II. �з�����Ӧ��
��II. �з�����Ӧ��![]() ��III. �з�����Ӧ��
��III. �з�����Ӧ��![]() ,�ɴ˿�֪����֮���ת�����̼���ϵΪ��
,�ɴ˿�֪����֮���ת�����̼���ϵΪ��![]() ���ݴ˽��
���ݴ˽��
A.����I�в�����ϡ�������ϡ���ᣬ��Ϊ�������ǿ�����ԣ��ܽ�������������������Ӷ��ò�����������A����
B.�ɴ˿�֪����֮���ת�����̼���ϵΪ��![]() ��n(NaOH) =
��n(NaOH) =![]() ����Wg��Ʒ��
����Wg��Ʒ��![]() ��1kg��Ʒ�к�SO2������Ϊ
��1kg��Ʒ�к�SO2������Ϊ![]() g����B����
g����B����
C.��������ˮ���滻II�е���������H2O2��Һ������������ˮ�������������ƣ�����������������ƫ�ߣ����⺬��ƫ�ߣ���C����
D.����I�����ɵ�SO2������װ����δ��H2O2��Һ���գ������������������ƫ�ͣ�������������ƫ�ͣ�������ƫ�ͣ���D��ȷ��
��ѡ��D��


 ���Ӣ��������ϵ�д�
���Ӣ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Σ���Լ�ǿ�Ķ������壬Ҳ�Ƕ���������Ҫ�ɷ�֮һ��![]() ����������Һ�п�ʵ����Ȼ���Ĵ�������ԭ����ͼ��ʾ������˵����ȷ���ǣ� ��
����������Һ�п�ʵ����Ȼ���Ĵ�������ԭ����ͼ��ʾ������˵����ȷ���ǣ� ��
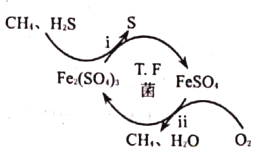
A.![]() ����������б���ԭ
����������б���ԭ
B.�¶�Խ�ߣ�Խ��������Ȼ���Ĵ�����
C.�����������Ҫ��������![]() ��Һ
��Һ
D.�����ϣ���Ҫ�������������ͬ״̬��![]() �����һ��
�����һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ú����̽��(��Ҫ�ɷ�ΪMnO2��������MgO��Fe2O3��Al2O3��SiO2)Ϊԭ�ϣ��Ʊ������̡�þ��һ�ֹ�������·�����£�
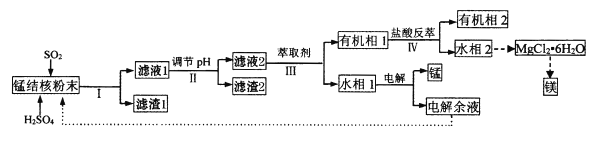
��֪���ټ�����������ܶȻ�(25��)���±���ʾ��
��ѧʽ | Mg(OH)2 | Mn(OH)2 | Al(OH)3 | Fe(OH)3 |
Ksp | 1.8��10-11 | 1.8��10-13 | 1.0��10-33 | 4.0��10-38 |
����Һ��ij����Ũ����1.0��10-6mol��L-1ʱ����Ϊ�����ӳ�����ȫ��
����������⣺
(1)���̽�˷�ĩ����MnO2��SO2��Ӧ�����ӷ���ʽΪ_____��
(2)����Һ1����c(Mn2+)Ϊ0.18mol��L-1������pH���ķ�ΧΪ_______��������2���ijɷ�Ϊ______��
(3)������������ȡ������ȡ�ijɷ���___�����������á����ᷴ�͡���������____��
(4)MgCl2��6H2O��ȡ��ˮMgCl2ʱ����Ҫ�ڸ����HCl�����м��ȷֽ⡣HCl������Ϊ__________��
(5)�ù��������г������Һ��ѭ�������⣬����ѭ�����õ��Լ�Ϊ____��
(6)һ�ֺ����ٵ��߾�(����̫ƽ�����)���������������Դ���Ϊ���ӹ��廹ԭMnO2����Mn2+�Ļ�����ͼ��ʾ��д����Ӧ�ڢ۵��ܷ�Ӧ�����ӷ���ʽ____________��
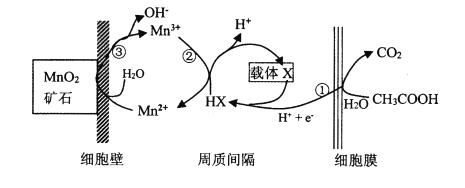
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¹������ڼ�ʹ�ô����������������ж�������(ClO2)����������(NaClO2)������ǿ�����ԡ�������Ư��ʱ�����˺�֯�������ˮ������ʱ����������ζ��ij�о���ѧϰС����������װ���ɶ��������Ʊ�NaClO2��3H2O����̽�������ʡ�
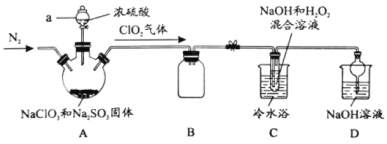
�������ϣ�
��ClO2����Ӧ�����������κ������Ρ�
��NaClO2������Һ���¶ȵ���38��ʱ�����ľ�����NaClO2��3H2O������38��ʱ�����ľ�����NaClO2������60��ʱNaClO2�ֽ��NaClO3��NaCl��
�ش��������⣺
(1)����a������_________��
(2)װ��A�з�����Ӧ�Ļ�ѧ����ʽ��________��
(3)�����ȥCװ���е���ˮԡ�����²�Ʒ�п��ܻ��е�������_______��
(4)��Ҫ��װ��C��Ӧ�����Һ�����ˮNaClO2����IJ����������£���������в�������۵����ݡ�
�ټ�ѹ��55�������ᾧ�� �ڳ��ȹ��ˣ���_________�� �ܵ���60�����õ���Ʒ��
(5)д��װ��C��Ӧ�����ӷ���ʽ________��
(6)ʵ���������ͨ��һ��ʱ��N2��Ŀ����________��
(7)��������ԭ���Ʊ���NaClO2��3H2O���������������������ӵ��������ⶨ����(������I-��������Ӧ)�Ĵ��ȣ��������£�(��֪��I2��2![]() ��
��![]() ��2I-)ȡ��Ʒ0.6000 g���Ƴ�250 mL��Һ������ȡ��25.0 mL��������KI���������ϡ���ᣬ�ٵμӼ��ε�����Һ��Ȼ����0.0600 mol/L Na2S2O3����Һ�ζ���������________(��ʵ������)���ﵽ�ζ��յ㣬�����ĸñ���Һ25.00 mL���������������NaClO2��3H2O�İٷֺ���Ϊ______(�������3λ��Ч����)��
��2I-)ȡ��Ʒ0.6000 g���Ƴ�250 mL��Һ������ȡ��25.0 mL��������KI���������ϡ���ᣬ�ٵμӼ��ε�����Һ��Ȼ����0.0600 mol/L Na2S2O3����Һ�ζ���������________(��ʵ������)���ﵽ�ζ��յ㣬�����ĸñ���Һ25.00 mL���������������NaClO2��3H2O�İٷֺ���Ϊ______(�������3λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ������з��ĶԶ��ױ���ɫ�ϳ���Ŀȡ���½�չ����ϳɹ�����ͼ��ʾ��

����˵������ȷ����
A. �����ϩ����̼ԭ�ӿ��ܹ�ƽ��
B. ������ˮ����M�ͶԶ��ױ�
C. �Զ��ױ���һ�ȴ�����2��
D. M��ij��ͬ���칹�庬�б����������Ʒ�Ӧ�ų�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������״������Ⱦ�Ժ��²��ԱȽ�ǿ��������ֿ�����Ч��Ԥ������״������Ⱦ�����粼�ǿ��ֵĺ��IJ��ϣ���Ҫ�Ǿ۱�ϩ������˵����ȷ���ǣ� ��
A.�۱�ϩ���������7��ԭ�ӹ�ƽ��
B.�۱�ϩ��ʹ���Ը��������Һ��ɫ
C.�۱�ϩ�����ã�C3H6��n��ʾ����һ�ִ�����
D.���۱�ϩ����ά�ض�����Ȼ�ĸ߷��ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ����ѡ��3�����ʽṹ������]
��ͤ���о�С���������ҽ����������As2O3���׳���˪����Ѫ�������Ե��������ã�����N�����ף�P�����飨As���ȶ���VA���Ԫ�أ�����Ԫ�صĻ��������о�����������������Ҫ��;���ش��������⣺
��1��Asԭ�ӵĺ�������Ų�ʽΪ ��
��2��P��S��ͬһ���ڵ�����Ԫ�أ�P�ĵ�һ�����ܱ�S��ԭ���� ��
��3��NH4+��H��N��H�ļ��DZ�NH3��H��N��H�ļ��� �����С������ԭ���� ��
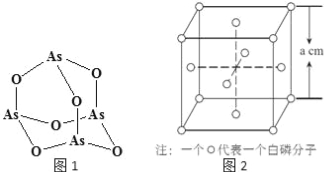
��4��Na3AsO4�к��еĻ�ѧ�����Ͱ��� ��AsO43���Ŀռ乹��Ϊ ��As4O6�ķ��ӽṹ��ͼ1��ʾ�����ڸû�������As���ӻ���ʽ�� ��
��5��������NH5�е�����ԭ������㶼�����ȶ��ṹ����NH5�� ���壮
��6�����ף�P4���ľ������ڷ��Ӿ��壬�侧���ṹ��ͼ2��СԲȦ��ʾ�����ӣ�����֪�����ı߳�Ϊa cm�������ӵ�����ΪNA mol��l����þ����к��е�Pԭ�ӵĸ���Ϊ ���þ�����ܶ�Ϊ gcm��3���ú�NA��a��ʽ�ӱ�ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ѧ��FulvioCacace���˻���˼��������о������N4������ӡ�N4���ӽṹ��ͼ��ʾ������˵����ȷ����( )
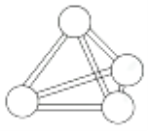
A.N4���ӵļ���Ϊ109��28��B.N4���ۡ��е��N2��
C.N4������ֻ���зǼ��Լ�D.0.5molN4�����������ۼ���Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̽�������ڲ�ͬ��Һ�еĸ�ʴ�����ʵ��װ�����������£�
ʵ��װ�� | ʵ������ |
|
|
����˵������ȷ����
A.�ٵĸ�����Ӧ��Fe-3e-=Fe3+
B.�۵�������Ӧ��O2+2H2O+4e-=4OH-
C.�ڿ���ͬʱ�������ⸯʴ��������ʴ
D.�����ĵ绯ѧ��ʴ����������Ϊ������Һ��pH�й�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com