
| A、平衡向正反应方向移动 |
| B、混合气体的平均摩尔质量增大 |
| C、CO2的转化率增大 |
| D、逆反应速率减小 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时,pH变化曲线如图所示,下列判断正确的是( )
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时,pH变化曲线如图所示,下列判断正确的是( )| A、a、c两点溶液的导电能力相同 |
| B、a、b、c三点溶液中水的电离程度:a>b=c |
| C、用等浓度的NaOH溶液分别与等体积的b、c两点溶液恰好完全反应,消耗NaOH溶液的体积相等 |
| D、b点溶液中存在微粒浓度关系:c(H+)=c(OH-)+c(NH3?H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
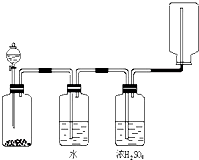
| A、锌和盐酸生成氢气 |
| B、亚硫酸钠和浓硫酸生成二氧化硫 |
| C、碳酸钙和盐酸生成二氧化碳 |
| D、氯化钠和浓硫酸生成氯化氢 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(A) |
| c(B) |
| c(A) |
| c(B) |
| A、若其他条件不变,升高温度,则a>b |
| B、保持温度、压强不变,充入惰性气体,则有a=b |
| C、在该温度下,保持容积固定不变,向容器内补充A气体,则a>b |
| D、若a=b,则容器中的反应一定是使用了催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯银在空气中久置变黑发生的是电化学腐蚀 |
| B、镀铜的铁制品,镀层破损后铁制品锈蚀更快 |
| C、用锌与稀硫酸反应制取氢气时,粗锌比纯锌反应快 |
| D、阴极电保护法是将被保护的金属与外加电源的负极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com