
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是( )
A.R的原子半径比Z的大 B.R的氢化物的热稳定性比W的强
C.X与Y形成的化合物只有一种 D.Y的最高价氧化物的水化物的酸性比W的强
科目:高中化学 来源: 题型:
下列有关物质性质的说法错误的是( )
A.热稳定性:HCl>HI B.原子半径:Na>Mg
C.酸性: H2SO3>H2SO4 D.结合质子能力:S2->Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组为了检验硫酸亚铁铵晶体中含有NH 、Fe2+、SO
、Fe2+、SO 和H2O,设计了如下实验步骤:①取少量晶体放在试管内,用酒精灯加热,试管口有液体产生说明晶体中含有水;
和H2O,设计了如下实验步骤:①取少量晶体放在试管内,用酒精灯加热,试管口有液体产生说明晶体中含有水;
②将加热后剩余的晶体溶解于水,加入盐酸酸化的氯化钡溶液,有白色沉淀生成,说明晶体中含有SO ;
;
③滤去白色沉淀,向滤液中加入过量的浓氢氧化钠溶液,加热,有能使红色石蕊试纸变蓝的气体产生,说明晶体中含有NH ;
;
④向步骤③的剩余液体中加入KSCN溶液,无明显变化,再加入少量氯水,溶液变血红色,说明晶体中含有亚铁离子。其中不能达到实验目的的是( )
A.①③④ B.①④
C.③④ D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列不能说明氯元素的非金属性比硫元素强的事实是( )
①HCl比H2S稳定 ②HClO氧化性比H2SO4强 ③HClO4酸性比H2SO4强 ④Cl2能与H2S反应生成S ⑤Cl原子最外层有7个电子,S原子最外层有6个电子 ⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS。
A.②⑤ B.①② C.①②④ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
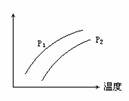
右图表示温度、压强对达平衡的可逆反应:2L(g) 2M(g)+N(g) △H>0的影响(P1<P2 ) 图中y轴表示的意义是 ( )
2M(g)+N(g) △H>0的影响(P1<P2 ) 图中y轴表示的意义是 ( )
A.混合物中L的百分含量
B.混合气体的密度
C.L的转化率
D.混合气体的平均分子量
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组为了探究“铁与水蒸气”的反应的产物,进行了下列实验:用如图所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒高温下不与水和铁反应).
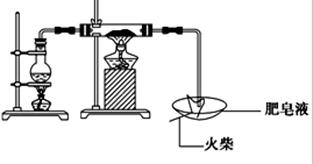
(1)如何检查该装置的气密性:
(2)写出铁与水蒸气反应的化学方程式
(3)验证固体产物中铁元素的价态
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;1mol/L CuSO4、3mol/L H2SO4、3mol/L HNO3、30%H2O2、0.01mol/L KMnO4、20%KSCN、蒸馏水。
在答题卡上按下表的格式写出实验步骤、预期现象与结论。
| 实验步骤 | 预期现象与结论 | |
| 步骤1 | 取反应后干燥的固体ag于试管中,加入足量的1mol/L CuSO4溶液,充分振荡,经固液分离、洗涤后,再向固体中滴加足量的 ,振荡溶解,过滤后将滤液配成250mL溶液,待用。 | |
| 步骤2 | 取少量步骤1中滤液于试管中,
|
|
| 步骤3 | 取少量步骤1中滤液于试管中,
|
|
步骤1中加入足量1mol/L CuSO4溶液的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于金属及金属键的说法正确的是
A.金属键具有方向性与饱和性
B.金属键是金属阳离子与自由电子间的相互作用
C.金属导电是因为在外加电场作用下产生自由电子
D.金属具有光泽是因为金属阳离子吸收并放出可见光
查看答案和解析>>
科目:高中化学 来源: 题型:
根据碘与氢气反应的热化学方程式:
(ⅰ)I2(g)+H2(g)  2HI(g) ΔH=-9.48 kJ·mol-1
2HI(g) ΔH=-9.48 kJ·mol-1
(ⅱ)I2(s)+H2(g)  2HI(g) ΔH=+26.48 kJ·mol-1
2HI(g) ΔH=+26.48 kJ·mol-1
下列判断正确的是
A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应(ⅰ)的产物比反应(ⅱ)的产物稳定
D.反应(ⅱ)的反应物总能量比反应(ⅰ)的反应物总能量低
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生做乙醛还原性的实验,取1 mol·L-1的硫酸铜溶液2 mL和0.4 mol·L-1的氢氧化钠溶液4 mL,在一个试管里混合后加入0.5 mL 40%的乙醛溶液加热至沸腾,无砖红色沉淀,实验失败的原因是( )
A.氢氧化钠的量不够 B.硫酸铜的量不够
C.乙醛溶液太少 D.加热时间不够
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com