
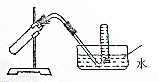
 如图装置可用于( )
如图装置可用于( )| A. | 加热NaHCO3制CO2 | B. | 用Cu和稀HNO3反应制NO | ||
| C. | 用NH4Cl与浓NaOH溶液反应制NH3 | D. | 用NaCl于浓H2SO4反应制HCl |
科目:高中化学 来源: 题型:选择题
| A. | 1:9 | B. | 10:1 | C. | 9:1 | D. | 1:10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HNO3+KOH═KNO3+H2O | B. | 2HCl+Cu(OH)2═CuCl2+2H2O | ||
| C. | CH3COOH+NaOH═CH3COONa+H2O | D. | HCl+NH3•H2O═NH4Cl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol/L | B. | 1.5mol/L | C. | 3mol/L | D. | 7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液 | B. | 氨水 | C. | CuO | D. | KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
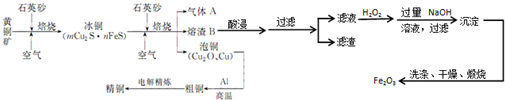
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用燃烧的方法鉴别真丝围巾和纯棉围巾 | |
| B. | 在烹调中加料酒和食醋,增加食物的香味 | |
| C. | 用工业酒精兑制饮用酒出售来提高利润 | |
| D. | 食用加碘盐,预防因缺碘引起的甲状腺肿大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com