
| A、1 mol Cl2作为氧化剂得到的电子数为NA |
| B、在0℃,101 kPa时,22.4 L氢气中含有NA个氢原子 |
| C、14 g氮气中含有7 NA个电子 |
| D、NA个一氧化碳分子和0.5 molCH4所含原子数相同 |
| V |
| Vm |
| V |
| Vm |
| 22.4L |
| 22.4L/mol |
| m |
| M |
| 14g |
| 28g/mol |


科目:高中化学 来源: 题型:
| A、进行蒸发操作时,应加热至混合物中有大量晶体析出时停止加热,用余热蒸干 |
| B、进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸过量,氢氧化钠不足 |
| B、氢氧化钠过量,盐酸不足 |
| C、两容器中投入的铝的质量为2.7g |
| D、条件不足,无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
| B、2.8g乙烯中含有共价键的数目为0.5NA |
| C、标准状况下,11.2L苯中含有分子的数目为0.5NA |
| D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生铁和钢都是铁的合金 |
| B、生铁的含碳量一定比钢高 |
| C、生铁的韧性优于钢,所以生铁有着比钢更广泛的用途 |
| D、生铁和钢都不是纯铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子晶体中都存在共价键 |
| B、金属晶体的熔点都比分子晶体的熔点高 |
| C、SiO2晶体中每个硅原子与两个氧原子以共价键相结合 |
D、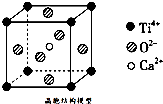 某物质晶胞结构如图,该物质的化学式为CaTiO3(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶点) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有多种元素符合本题条件 |
| B、符合本题的HxROy有一元酸和多元酸 |
| C、z与x的数值相等 |
| D、R可能是第二周期元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com