
| 1 |
| 2 |
| 1 |
| 2 |
| 393.5kJ |
| 12 |
| 1 |
| 2 |
| 285.8 |
| 2 |
| ||
|


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��m��n | B��m=n |
| C��m��n | D������ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��̼�����Ƶ�ˮ�ⷴӦ��HCO3-+H2O?CO32-+H+ |
| B����Ƭ������������Һ��Ӧ��Al+2OH-�TAlO2-+H2�� |
| C����������Һ��ͨ��������2H2SO3+O2�T4H++2SO42- |
| D�������������Һ��ͨ������SO2���壺ClO-+SO2+H2O�THClO+HSO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
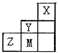
| A���ǽ����ԣ�Y��Z��M |
| B��ԭ�Ӱ뾶��M��Z��Y |
| C����̬�⻯����ȶ��ԣ�Y��M��Z |
| D��ZM2�����и�ԭ�ӵ�����������8e-�ȶ��ṹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢ� | B���٢ڢ� |
| C���ڢۢ� | D���٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������ʵ���ҳ��õ�һ�ֻ�ѧ�Լ���ij�����Լ�ƿ�ϱ�ǩ�IJ���������ͼ��ʾ�����ñ�ǩ�ṩ����Ϣ���ش��������⣺
������ʵ���ҳ��õ�һ�ֻ�ѧ�Լ���ij�����Լ�ƿ�ϱ�ǩ�IJ���������ͼ��ʾ�����ñ�ǩ�ṩ����Ϣ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 mol Cl2��Ϊ�������õ��ĵ�����ΪNA |
| B����0�棬101 kPaʱ��22.4 L�����к���NA����ԭ�� |
| C��14 g�������7 NA������ |
| D��NA��һ����̼���Ӻ�0.5 molCH4����ԭ������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������֮�ȵ���1��1 |
| B��ԭ����֮�ȵ���3��2 |
| C������֮�ȵ���7��11 |
| D��������֮�ȵ���7��11 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com