
| A、碳酸氢钠的水解反应:HCO3-+H2O?CO32-+H+ |
| B、铝片跟氢氧化钠溶液反应:Al+2OH-═AlO2-+H2↑ |
| C、亚硫酸溶液中通入氧气:2H2SO3+O2═4H++2SO42- |
| D、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3- |


科目:高中化学 来源: 题型:
| A、盐酸、氢氧化钠、氯化钠 |
| B、氢氧化钠、氢氧化钡、硫酸 |
| C、硫酸氢钠、碳酸钠、氢氧化钠 |
| D、硫酸铜、盐酸、硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、增大压强,平衡不移动,说明(m+n)一定等于(p+q) |
| B、升高温度,A的转化率减小,说明正反应是吸热反应 |
| C、若增加B的量,平衡体系颜色加深,说明B必是气体物质 |
| D、若B是气体,增加A的量,A、B转化率都一定增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、进行蒸发操作时,应加热至混合物中有大量晶体析出时停止加热,用余热蒸干 |
| B、进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
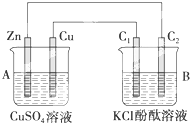 按如图所示装置进行实验,并回答下列问题:
按如图所示装置进行实验,并回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、雾属于胶体,能产生丁达尔效应 |
| B、持续大雾天气给农业生产、交通运输等带来很大影响 |
| C、大雾的形成与汽车的尾气排放有很大关系 |
| D、“PM2.5”悬浮在空气中形成胶体,严重危害人体健康 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 定时间/小时 | 0 | 1 | 2 | 4 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子晶体中都存在共价键 |
| B、金属晶体的熔点都比分子晶体的熔点高 |
| C、SiO2晶体中每个硅原子与两个氧原子以共价键相结合 |
D、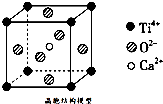 某物质晶胞结构如图,该物质的化学式为CaTiO3(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶点) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com