
| A、有多种元素符合本题条件 |
| B、符合本题的HxROy有一元酸和多元酸 |
| C、z与x的数值相等 |
| D、R可能是第二周期元素 |


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
| A、1 mol Cl2作为氧化剂得到的电子数为NA |
| B、在0℃,101 kPa时,22.4 L氢气中含有NA个氢原子 |
| C、14 g氮气中含有7 NA个电子 |
| D、NA个一氧化碳分子和0.5 molCH4所含原子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子数之比等于1:1 |
| B、原子数之比等于3:2 |
| C、质量之比等于7:11 |
| D、质子数之比等于7:11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
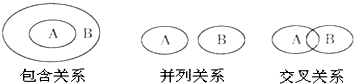
| A、纯净物与混合物属于包含关系 |
| B、化合物与电解质属于包含关系 |
| C、单质与化合物属于交叉关系 |
| D、氧化还原反应与化合反应属于并列关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲烷和氯气的混合气体在光照后,瓶壁上有油状液滴附着 |
| B、乙烯通入溴的四氯化碳溶液中,溶液褪色 |
| C、苯滴加到溴水中,振荡后水层接近无色 |
| D、将灼热的铜丝迅速插入乙醇中,反复多次,有刺激性气味产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
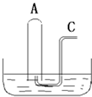 如图所示:在B槽中装有500mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B槽的水中,充分反应,试管A中余下气体的体积为0.5amL.
如图所示:在B槽中装有500mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B槽的水中,充分反应,试管A中余下气体的体积为0.5amL.查看答案和解析>>
科目:高中化学 来源: 题型:
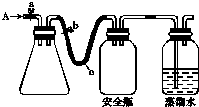 实验室用下列方法测定某水样中O2的含量.
实验室用下列方法测定某水样中O2的含量.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢气和氯气点燃生成氯化氢,氯化氢受热分解为氢气和氯气 |
| B、氮气和氢气在高温、高压、催化剂作用下可以生成氨气,同时氨气又分解为氮气和氢气 |
| C、单质溴可以置换出碘,氯气又可以置换出溴 |
| D、氯气和水反应生成盐酸和次氯酸,次氯酸光照条件下可分解为盐酸和氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com