
【题目】下列措施对增大反应速率明显有效的是
A. Na与水反应时增大水的用量
B. 将锌与稀硫酸反应时,向溶液中加入少量CuSO4晶体
C. Fe与稀硫酸反应制取氢气时,改用浓硫酸
D. 用碳还原Fe2O3冶炼铁时,增大碳的用量
科目:高中化学 来源: 题型:
【题目】古代染坊常用某种“碱剂”精炼丝绸,该“碱剂”的主要成分是一种盐,能促进蚕丝表层胶蛋白杂质水解而除去,使丝绸洁白、质感柔软、色泽光亮。这种“碱剂”可能是
A.食盐B.熟石灰C.明矾D.草木灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,将V L HCl气体溶解在1 L水(水的密度为1 g/cm3)中,形成饱和溶液,所得溶液的密度为ρ g/mL,质量分数为ω,物质的量浓度为c mol/L,溶解度为s g,下列关系式不正确的是( )
A. c=1000Vρ/(36.5V+22400) B. ω=36.5V/(36.5V+22400)
C. ρ=(36.5V+22400)/(22.4+22.4V) D. s=36.5V/224
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸镧咀嚼片是一种不含钙和铝的磷酸盐结合剂,用于慢性肾衰患者高磷血症的治疗。碳酸镧可由 LaCl3 为原料来制备,整个反应在较低的pH条件下进行,避免生成碱式碳酸镧[La(OH)CO3]。
(1)化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。
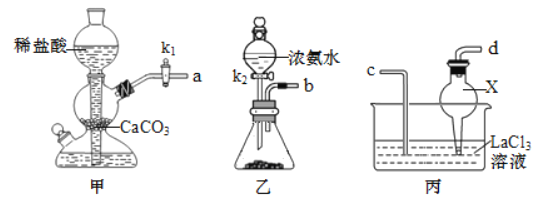
①仪器 X 的名称为________;检验装置甲气密性良好的方法是___________。
②实验中 K1、 K2 打开的先后顺序为________;为保证碳酸镧的纯度,实验过程中需要注意的问题有____________。
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
①为了高磷血症患者的安全,通常选用碳酸氢钠溶液,过程中会发生两个平行反应,其离子方程式为_______和____________。
②选择碳酸氢钠溶液制备碳酸镧的优点是___________(任写一条)。
③T℃时,碳酸镧的溶解度为1.0×10-7 mol·L-1, HCO3-的电离平衡常数为 6.0×10-11。请计算反应 2LaCl3+3NaHCO3![]() La2(CO3)3↓+3NaCl+3HCl 的平衡常数 K=_________。
La2(CO3)3↓+3NaCl+3HCl 的平衡常数 K=_________。
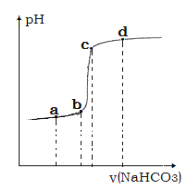
④利用手持技术测定溶液的 pH 从而监控反应过程,得到如图曲线。请说明 bc 段变化的原因__________。
(3)碳酸镧(式量为 458)质量分数的测定:准确称取15.0g产品试样,溶于10.0mL 稀盐酸中,加入 10mLNH3-NH4Cl 缓冲溶液,加入 0.2g 紫脲酸铵混合指示剂,用 0.5 mol·L-1EDTA(Na2H2Y)标准溶液滴定至呈蓝紫色(La3++H2Y2-= LaY-+2H+),消耗 EDTA 溶液 60.00mL。则产品中碳酸镧的质量分数 w=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() 。
。
(1)该反应生成物中所含官能团的名称是_______;在一定条件下能发生______(填序号)反应。
①银镜反应 ②酯化反应 ③还原反应
(2)某氯代烃A的分子式为C6H11Cl,它可以发生如下转化:
![]()
结构分析表明:E的分子中含有2个甲基,且没有支链,试回答:
①有关C的说法正确的是_____________(填序号)。
a.分子式为C6H10O2
b.C属于醛类,且1 mol C与足量的新制Cu(OH)2反应可得 4 mol Cu2O
c.C具有氧化性,也具有还原性
d.由D催化氧化可以得到C
②写出下列转化关系的化学方程式,并指出反应类型。
A→B:____________________________________________,_____________;
D→E:____________________________________________,_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸具有止血功效,存在于多种中药中,其结构简式为 。
。
(1)写出咖啡酸中两种含氧官能团的名称:________;
(2)根据咖啡酸的结构,列举三种咖啡酸可以发生的反应类型:________、________、________;
(3)蜂胶的分子式为C17H16O4,在一定条件下可水解生成咖啡酸和一种醇A,则醇A的分子式为________。
(4)已知醇A含有苯环,且分子结构中无甲基,写出醇A在一定条件下与乙酸反应的化学方程式:___________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X.Y、Z、W四种短周期元素,它们在周期表中位置如图所示,下列说法正确的是
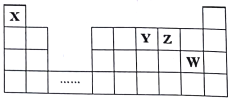
A. 四种元素的原子半径由小到大的顺序为:r(X)<r(Z)<r(W)<r(Y)
B. X、Y、Z既能形成离子化合物,又能形成共价化合物
C. X与其余三种元素之间形成的核外电子总数为10的微粒只有2种
D. H2Z的熔点比HW高,是因为它们的晶体类型不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法不正确的是
A. 1mol-CH3中含有的质子数为10NA
B. H2O2+Cl2= 2HCl+O2反应中,每生成32gO2,转移2NA个电子
C. 3.6gCO和N2的混合气体含中子数为1.8NA
D. 6.2g白磷含有0.3 NA P-P键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二草酸合铜(II)酸钾晶体{K2[Cu(C2O4)2]·2H2O}(其相对式量为354),是一种工业用化工原料。微溶于冷水,可溶于热水,微溶于酒精,干燥时较为稳定,加热时易分解。现以胆矾和草酸为原料制备二草酸合铜( II)酸钾晶体流程如下:

(已知:H2C2O4![]() CO↑十CO2↑+H2O)
CO↑十CO2↑+H2O)
请回答:
(1)第①步操作要微热溶解,其原因是加快溶解速率和________。
(2)为了将滤纸上的黑色固体充分转移到热的KHC2O4溶液中,以下操作方案中最合理的是______。
A.用水溶解滤纸上的黑色固体,然后将溶液转入热的KHC2O4溶液中
B.用硫酸溶液溶解滤纸上的氧化铜,然后转入热的KHC2O4溶液中
C.黑色固体连同滤纸一起加入到热的KHC204溶液中,待充分反应后趁热过滤
D.先将黑色固体转入溶液中,再在空气中灼烧滤纸,将剩余的固体转入热的KHC2O4溶液中
(3)50℃水浴加热至反应充分,写出该反应的化学方程式___________。
(4)步骤③所用的洗涤剂最合适的是_______。
(5)二草酸合铜(II)酸钾晶体的制备也可以用CuSO4晶体和K2C2O4溶液反应得到。从硫酸铜溶液中获得硫酸铜晶体的实验步骤为:加入适量乙醇、蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
①加入适量乙醇的优点有:
a.缩短加热的时间,降低能耗;b.________ 。
②在蒸发浓缩的初始阶段可通过_______(填操作名称)回收乙醇。
(6)准确称取制取的晶体试样l.000g溶于NH3·H2O中,并加水定容至250mL,取试样溶液25.00mL于锥形瓶中,再加入l0mL 3.000mol/L的H2SO4溶液,用0.01000mol/L的KMnO4溶液滴定,消耗KMnO4标准液20.00mL,则该产品的纯度是_______ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com