
【题目】(1)14g CO 在氧气中燃烧生成 CO2,放出33.6kJ 热量,写出 CO 燃烧热的化学方程式 。
(2)已知500mL 0.2mol/L的硫酸与含11.2g氢氧化钾的稀溶液反应,放出热量11.46kJ,表示该反应中和热的化学方程式为: 。
(3)下列物质中均含有极性共价键的是 。
A. NH3; CO2; NH4Cl; NaOH;
B. H2O ; NH4Cl ; H2SO4 ; H2O2 ;
C. CaCl2 ; CO2 ; Na2O2 ; Ca(OH)2
【答案】
(1)CO(g)+O2(g)=CO2(g) △H =-67.2 kJmol-1;
(2)△H=-57.3kJmol-1,答案为:![]() H2SO4(aq)+KOH(aq)=
H2SO4(aq)+KOH(aq)=![]() K2SO4(aq)+H2O(l) △H=-57.3kJmol-1;(3)AB.
K2SO4(aq)+H2O(l) △H=-57.3kJmol-1;(3)AB.
【解析】
试题分析:(1)14g CO 的物质的量为0.5mol,在氧气中燃烧生成 CO2,放出33.6kJ 热量,1molCO完全燃烧生成CO2放出热量67.2kJ,CO 燃烧的热化学方程式为:CO(g)+O2(g)=CO2(g) △H =-67.2 kJmol-1,答案为:CO(g)+O2(g)=CO2(g) △H =-67.2 kJmol-1;(2)已知500mL 0.2mol/L的硫酸与含11.2g氢氧化钾的稀溶液反应,其中硫酸的物质的量为0.1mol,氢氧化钾的物质的量为0.2mol,生成水的物质的量为0.2mol,放出热量11.46kJ,反应的热化学方程式为:![]() H2SO4(aq)+KOH(aq)=
H2SO4(aq)+KOH(aq)=![]() K2SO4(aq)+H2O(l) △H=-57.3kJmol-1,答案为:
K2SO4(aq)+H2O(l) △H=-57.3kJmol-1,答案为:![]() H2SO4(aq)+KOH(aq)=
H2SO4(aq)+KOH(aq)=![]() K2SO4(aq)+H2O(l) △H=-57.3kJmol-1;(3)下列物质中均含有极性共价键的是A. NH3; CO2; NH4Cl; NaOH,均含有极性共价键,A正确;B. H2O ; NH4Cl ; H2SO4 ; H2O2 ,均含有极性共价键,B正确;C.CaCl2 ; CO2 ; Na2O2 ; Ca(OH)2,CaCl2只有离子键,Na2O2只有离子键和非极性共价键,C错误,答案为:AB.
K2SO4(aq)+H2O(l) △H=-57.3kJmol-1;(3)下列物质中均含有极性共价键的是A. NH3; CO2; NH4Cl; NaOH,均含有极性共价键,A正确;B. H2O ; NH4Cl ; H2SO4 ; H2O2 ,均含有极性共价键,B正确;C.CaCl2 ; CO2 ; Na2O2 ; Ca(OH)2,CaCl2只有离子键,Na2O2只有离子键和非极性共价键,C错误,答案为:AB.


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】下列反应中属于吸热反应的是( )
A.镁与盐酸反应放出氢气
B.氢氧化钠与盐酸的反应
C.硫在空气或氧气中燃烧
D.Ba(OH)28H2O与NH4Cl反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置测定中和热的实验步骤如下:

①量取50mL 0.25mol/L H2SO4溶液倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。请回答:
(1)如右图所示,仪器A的名称是_________ ______;
(2)NaOH溶液稍过量的原因 ____________________________。
(3)加入NaOH溶液的正确操作是_______(填字母)。
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(4)使硫酸与NaOH溶液混合均匀的正确操作是 ________ __________________。
(5)设溶液的密度均为1g·cm-3,中和后溶液的比热容c=4.18 J·(g·℃)-1,请根据实验数据写出该中和热的热化学方程式_______________________________

(6)上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(7)怎样才能确保读取混合液的最高温度?_______ ____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列材料的特性及用途说法错误的是(
A.高纯硅用于制造光导纤维,实现光电信号转化
B.石英中无色透明的晶体就是通常所说的水晶,其主要成分是二氧化硅
C.光导纤维导光的能力很强,是非常好的通讯材料
D.硅胶多孔,吸附水能力强,可以用作催化剂的载体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。


(1)电解NO制备NH4NO3原理如左图所示:
①阳极为_______ (填X或Y),Y的电极反应式为________________________________。
②为使电解产物完全转化为NH4NO3,需要补充的物质A的化学式为________________。
(2)用如图装置进行模拟电解NO2气体实验,可回收硝酸。
①电解时NO2发生反应的电极反应式_________________________________。
②若有标准状况下2.24 LNO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为_________________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氯水与SO2气体都具有漂白性,若将等体积的氯气和SO2通入到水中,得到的溶液是否具有漂白性?_______________(填“是”或“否”). 用化学方程式表示其中的原因 。
(2)氨气在实验室中可快速制得,请写出相关的化学方程式:
。
验满的方法是: 。
(3)写出铜在浓硝酸中反应的离子方程式:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素。

请用化学用语回答下列问题:
(1)E元素在周期表中的位置: 。
(2)A、D、E元素简单离子半径由大到小的顺序为 > > (填微粒符号)。
(3)F与D同主族且相邻,二者气态氢化物稳定性的大小关系为 > (填微粒符号)。
(4)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出阳离子的电子式: ,该阳离子中存在的化学键有 。
(5)由C、E两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子里C、E两种原子最外层均达到8个电子的稳定结构。甲遇水蒸气可形成一种常见的漂白性物质。则甲的结构式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 下列有关碱土金属锶(Sr)元素单质及其化合物的叙述中,正确的是( )
A. 锶能与水反应,但反应缓慢
B. 硝酸锶是离子化合物,不溶于水
C. 氢氧化锶碱性弱于氢氧化镁的碱性
D. 金属锶单质银白色,导电性良好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)为原料制备MgCO3·3H2O。实验过程如下:

(1)酸溶过程中主要反应的热化学方程式为
MgCO3(s)+2H+(aq)===Mg2+(aq)+CO2(g)+H2O(l) ΔH=-50.4 kJ·mol-1
Mg2SiO4(s)+4H+(aq)===2 Mg2+(aq)+H2SiO3(s)+H2O(l) ΔH=-225.4 kJ·mol-1
酸溶需加热的目的是______;所加H2SO4不宜过量太多的原因是_______。
(2)加入H2O2氧化时发生发应的离子方程式为___________。
(3)用下图所示的实验装置进行萃取分液,以除去溶液中的Fe3+。
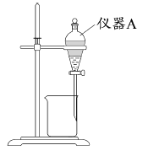
①实验装置图中仪器A的名称为_______。
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有机萃取剂,______、静置、分液,并重复多次。
(4)请补充完整由萃取后得到的水溶液制备MgCO3·3H2O的实验方案:边搅拌边向溶液中滴加氨水,______,过滤、用水洗涤固体2~3次,在50℃下干燥,得到MgCO3·3H2O。
[已知该溶液中pH=8.5时Mg(OH)2开始沉淀;pH=5.0时Al(OH)3沉淀完全]。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com