
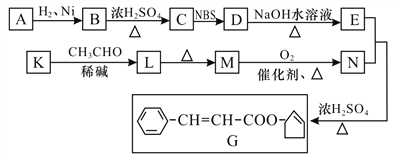
����Ŀ�����л���ѧ����������G��һ�ֺϳɹ�������ͼ��ʾ��
�˴Ź���������ʾA�����ַ壬�ҷ����֮��Ϊ1��1���Ҳ���C=C��
��֪��CH3CH2CH==CH2![]() CH3CHBrCH==CH2
CH3CHBrCH==CH2
CH3CHO��CH3CHO![]() CH3CHOHCH2CHO
CH3CHOHCH2CHO
CH3CHOHCH2CHO![]() CH3CH==CHCHO��H2O
CH3CH==CHCHO��H2O
��ش�
��1��A�Ľ��ʽΪ_______________��G�г�����������ŵ�����Ϊ___________________��
��2������M����ȫת��ΪN��ʵ������������ǣ�_______________����M����ȫת��ΪN��
��3����ѧ�����飬��M��N��ת����KMnO4(H��)����O2����ʦ��Ϊ��������ԭ����_____________��
��4��K��L�Ļ�ѧ����ʽΪ___________________________����Ӧ����Ϊ______________��
��5��F��M��ͬϵ���M��һ��̼ԭ�ӡ���������������F��ͬ���칹����________��(�����������칹)�����ܷ���������Ӧ��������������Ȼ�̼��Һ�ӳɣ��۱�������2��ȡ��������Щͬ���칹���У����в�������̼ԭ���ڱ�������ԳƷֲ���ͬ���칹��Ľṹ��ʽΪ__________________��
��6���Ա�ϩ��NBS�Լ�Ϊԭ���Ʊ�����(������)������ƺϳ�·��(������ԭ����ѡ)��__________���������·�ʽ��ʾ��A![]() B��
B��![]() Ŀ������
Ŀ������
���𰸡� ![]() ̼̼˫�������� ȡ����ת�������Թ��У��μ�ŨNaOH����Һ�ʼ��ԣ��ټ����Ƶ�Cu(OH)2���ȣ���û��ש��ɫ����������M��ת����ȫ KMnO4(H��)������ȩ����ͬʱ����������̼̼˫��
̼̼˫�������� ȡ����ת�������Թ��У��μ�ŨNaOH����Һ�ʼ��ԣ��ټ����Ƶ�Cu(OH)2���ȣ���û��ש��ɫ����������M��ת����ȫ KMnO4(H��)������ȩ����ͬʱ����������̼̼˫�� 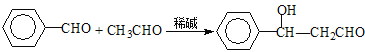 �ӳɷ�Ӧ 18
�ӳɷ�Ӧ 18 ![]() CH2==CH��CH3
CH2==CH��CH3![]() CH2==CH��CH2��Br
CH2==CH��CH2��Br![]()
![]()
![]()
![]()
�������������������������ͼ�������Ϣ��֪��E��N��Ũ����Ĵ��·���������Ӧ������G����G���������ѣ���EΪ3-�ǻ�����ϩ��NΪ����ϩ�ᣬD��NaOH��Һ�м�������E����DΪ3-�强ϩ��������Ϣ1��֪CΪ��ϩ��B��Ũ������ȵ�����������C����BΪ����������AΪ����ͪ��������֪2��3��֪KΪ����ȩ��LΪ![]() ��MΪ����ϩȩ��M�������������������¼�������N(����ϩ��)��
��MΪ����ϩȩ��M�������������������¼�������N(����ϩ��)��
��1����������������AΪ����ͪ���˴Ź���������ʾA�����ַ壬��ǿ��֮��Ϊ1: 1��������ṹ��ʽΪ![]() ��G�й����ŵ�����Ϊ̼̼˫����������
��G�й����ŵ�����Ϊ̼̼˫����������
��2������M����ȫת��ΪN��ʵ�����Ǽ���M����ȩ����ʵ�������ȡ����ת�������Թ��У��μ�ŨNaOH����Һ�ʼ��ԣ��ټ����Ƶ�Cu(OH)2���ȣ���û��ש��ɫ����������M��ת����ȫ��
��3��KMnO4(H��)��Һ����ǿ�����ԣ��ܽ�ȩ����̼̼˫�����������Բ��ܽ�M�� N��ת����KMnO4(H��)����O2��ԭ����KMnO4(H��)������ȩ����ͬʱ������������̼̼˫����
��4��K��L�Ļ�ѧ��ӦΪ�� �����ݷ�Ӧ�ص㣬�÷�Ӧ�Ǽӳɷ�Ӧ��
�����ݷ�Ӧ�ص㣬�÷�Ӧ�Ǽӳɷ�Ӧ��
��5��F��M(����ϩȩ)��ͬϵ���M��һ��̼ԭ�ӣ�˵����10��̼ԭ�ӵķ����廯������ܷ���������Ӧ��˵����ȩ����������������Ȼ�̼��Һ�ӳɣ�˵����̼̼˫�����۱�������2��ȡ����������ͬ���칹�������ȡ�����ֱ���һ��ȡ����Ϊ������һ��ȡ����������������һ������ϩ������һ������ȩ����һ����ȡ����Ϊȩ������һ����ϩ��3��������ȡ�������칹����6�֣�����ȡ���������ڡ��䡢������λ�ù�ϵ����18��ͬ���칹�����в�������̼ԭ���ڱ�������ԳƷֲ���ͬ���칹��Ľṹ��ʽΪ![]() ��
��
��6���Ա�ϩ��NBS�Լ�Ϊԭ���Ƹ�����(������)���ϳ�·��Ϊ��CH2==CH��CH3![]() CH2==CH��CH2��Br
CH2==CH��CH2��Br![]()
![]()
![]()
![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ҹ��Ƽ��ɹ����漰���ʵ�Ӧ���У�������������ѧ�仯����
|
|
|
|
A���״���������������������Դ���� | B��뮡������������̫�����˾۱�ȼ�� | C��ƫ�����������������칬�������Ļ��ȼ�� | D�����ɿ�ȼ����������Ϊ��Դʹ�� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������Է�Һ�к���Fe3+��Al3+��Fe2+��SO42-���Ը÷�ҺΪԭ���Ʊ�Fe2O3�Ĺ�����������(���ֲ�����������)��
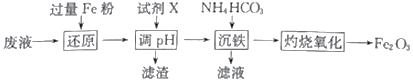
��֪����NH4HCO3����ˮ�л�ֽ⡣
�ڳ����£���Һ�в�ͬ�����������������������ʱ��pH���±���
��������(0.1mol��L-l) | Fe3+ | Fe2+ | Al3+ |
��ʼ����ʱ��pH | 2.4 | 7.6 | 3.4 |
��ȫ����ʱ��pH | 3.7 | 9.6 | 4.8 |
�ش��������⣺
��1��д������ԭ�������з�Ӧ�����ӷ���ʽ��_________________________________��
��2���Լ�X��ѡ��_________����дһ�֣��ѧʽ����������������Ҫ�ɷ���_________________��
��3������̼����狀���ˣ�������Һ��Ȼ���ǣ����ܵ�ԭ����_________________________����90����ˮϴ��FeCO3������Ŀ����______________________________________��
��4������ʵ����������FeCO3Ӧ��_____________(����������)�н��У������������������Ļ�ѧ����ʽΪ__________________________________��
��5������ҵ����������174.0��FeCO3�õ�117.6�ֲ�Ʒ����ò�Ʒ��Fe2O3�Ĵ���Ϊ___________ (���Ʒ������ֻ��FeO������һλС��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1mol/LNaOH��Һ�ζ�10 mL 0.1 mol/LH2A��Һ����Һ��pH��NaOH��Һ�������ϵ��ͼ��ʾ������˵������ȷ����
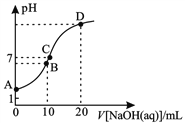
A. A����Һ�м�������ˮ��![]() ����
����
B. B�㣺c( HA -)>c(H+)>c(A2һ)>c(H2A)
C. ˮ���������c(OH -)��B��>D��
D. C�㣺c(Na+) =c(HA-)+2c( A2-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʽṹ�����ʡ�����BP����һ���ܹ�ע����ĥͿ����ϣ�����Ϊ�ѵȽ�������ı�����Ĥ��
��1�����廯������廯������ڸ�����������H2��Ӧ�����Ƶ�BP��
��������Ӧ�Ļ�ѧ����ʽΪ________________________��
����ԭ���д���_____�ֲ�ͬ�����ĵ��ӣ�����ռ�ݵ�����ܲ����Ϊ_______��
�۳����£����廯���ǵ���ɫ����Һ�壬�����ڱ�ͪ�����Ȼ�̼�У�����������______���壨������ͣ���
��2����֪��������ǿ�ᣬ���������pKa= -lgKa��
���л��������ǿ�����ڽ�̼��ȡ��ԭ�ӵ�Ӱ��,�����ԣ�BrCH2COOH >CH3COOH���ݴ��Ʋ⣬pKa��AtCH2COOH____ClCH2COOH���>������<������=����
����������Ԫ�ᣬд��������PO43-������ͬ�ռ乹�ͺͼ�����ʽ�ķ��ӻ�����_________________��
��������һԪ�ᣬ����ˮ�б��ֳ����������ԣ�������������������������£�����ˮ������B(OH)3��ϣ�����һ��������ӣ��������ӵĽṹʽΪ��_________����������λ�������ü�ͷ�������
��3�������մɲ���Si3N4�ijɼ���ʽ��ͼ1��ʾ���ṹ��N��Si��N�ļ��DZ�Si��N��Si�ļ��Ǵ���ԭ����_____________________________________��
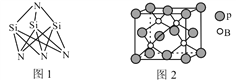
��4������ľ���ṹ��ͼ2��ʾ��������Pԭ�ӵĶѻ���ʽΪ________��������������������������������������ܡ����ѻ������þ��������ڽ�������Pԭ��֮��ľ���Ϊa nm�������ܶ�Ϊ__________g��cm-3��ֻ���г�����ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��̽�������Ҵ������ʣ�ijͬѧ��Ʋ�����������ʵ�顣
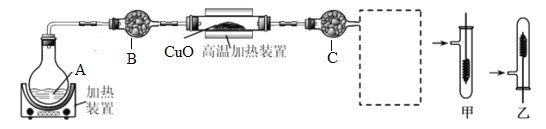
��ش�
(1)����B������Ϊ_____________��
(2)Ϊ�����Ʊ�������A��Ӧ������Լ�Ϊ______��B��Ӧ������Լ�Ϊ_______��
(3)��A�м����Ҵ���B�м�����ʯ�ң�C�м�����ˮ����ͭ����Ӧһ��ʱ���C�е�����Ϊ_________������ⷴӦ�м���������ȩ�����������������ᡣ��д���Ҵ�������ͭ��Ӧ������ȩ�Ļ�ѧ����ʽ_____________________��
(4)��(3)��ʵ���ijͬѧΪ����β�����Ƿ����Ҵ������߿���ѡ���װ����______(��ס����ҡ�)��ʵ��ʱӦ�Ƚ�����״ͭ˿���ȣ���ں��ٳ���Ѹ�������Թ��У��۲쵽ͭ˿�ɺڽ�����죬�ɴ˿ɵó��Ľ�����____________________��(������������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ͪ��C3H6O��ͨ������ɫҺ�壬������ˮ���ܶ�С��1 gmL��1 �� �е�ԼΪ55�森Ҫ��ˮ���ͪ�Ļ�����н���ͪ������������з�������Ϊ�������ǣ� ��
A.����
B.��Һ
C.����
D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������̼����ȼ�ϵ��ԭ��ʾ����ͼ�������йظõ�ص�˵����ȷ���ǣ�������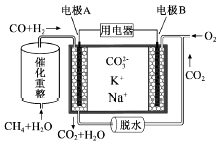
A.�缫B�Ϸ����ĵ缫��ӦΪ��O2+2CO2+4e��=2CO32��
B.�缫A��H2����ĵ缫��ӦΪ��H2+2OH����2e��=2H2O
C.��ع���ʱ��CO32����缫B�ƶ�
D.��ӦCH4+H2O ![]() 3H2+CO��ÿ����1molCH4ת��12mol ����
3H2+CO��ÿ����1molCH4ת��12mol ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com