
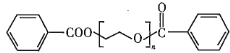
【题目】有机化合物F可作为内燃机的润滑油,聚合物![]() (
(![]() )用于制备水凝胶,它们的合成路线如下:
)用于制备水凝胶,它们的合成路线如下:
已知:![]() +(n-1)H2O
+(n-1)H2O
nCH2=CH2+nCH2=CHCH3![]()
![]()
(1)![]() 的分子式为
的分子式为![]() ,
,![]() 的化学名称是_________。红外光谱测定结果显示,
的化学名称是_________。红外光谱测定结果显示,![]() 中不含羟基。
中不含羟基。![]() 的反应类型是_____________。
的反应类型是_____________。
(2)![]() 的化学方程式是__________________。
的化学方程式是__________________。
(3)反应![]() 的另一种产物是
的另一种产物是![]() ,其相对分子质量是60,
,其相对分子质量是60,![]() 均能与
均能与![]() 溶液反应产生
溶液反应产生![]() 。
。
①![]() 的结构简式是_______________________。
的结构简式是_______________________。
②![]() 的化学方程式是________________________。
的化学方程式是________________________。
(4)下列说法正确的是_________________。
a.![]() 中均含有酯基
中均含有酯基
b.![]() 中所有碳原子一定在同一平面上
中所有碳原子一定在同一平面上
c.![]() 的同分异构体中能使
的同分异构体中能使![]() 溶液显色的共有1l种
溶液显色的共有1l种
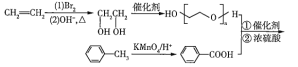
(5)写出由乙烯和甲苯合成![]() 的路线:______________(其他试剂任选)。
的路线:______________(其他试剂任选)。
【答案】邻羟基苯甲酸(或![]() 羟基苯甲酸) 酯化反应或取代反应 2
羟基苯甲酸) 酯化反应或取代反应 2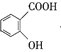 +HCHO
+HCHO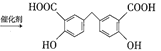 +H2O
+H2O ![]()
 +H2O
+H2O 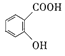 +CH3COOH
+CH3COOH ![]()
【解析】
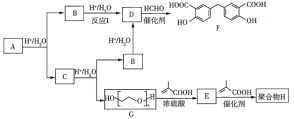
(1)结合D的分子式为C7H6O3,根据D→F的转化关系及F的结构简式可知![]() 的结构简式是
的结构简式是![]() ;
;
(2)结合D、F以及HCHO的结构特征,写出![]() 的化学方程式;
的化学方程式;
(3)①由于反应Ⅰ的另一种产物M能与NaHCO3溶液反应产生CO2,则M结构中含有羧基,并且相对分子质量为60,M为乙酸,又因为B能与NaHCO3溶液反应产生CO2,则B结构中含有羧基,B为![]() ;
;
(4)由乙烯和甲苯合成![]() ,乙烯与溴水中的Br2发生加成反应生成BrCH2CH2Br,BrCH2CH2Br在氢氧化钠溶液中,在加热条件下生成乙二醇,然后在结合题中的信息并利用题中的信息去设计合成路线。
,乙烯与溴水中的Br2发生加成反应生成BrCH2CH2Br,BrCH2CH2Br在氢氧化钠溶液中,在加热条件下生成乙二醇,然后在结合题中的信息并利用题中的信息去设计合成路线。
(1)D的分子式为![]() ,根据D→F的转化关系及F的结构简式可知
,根据D→F的转化关系及F的结构简式可知![]() 的结构简式是
的结构简式是![]() ,名称为
,名称为![]() 羟基苯甲酸;由
羟基苯甲酸;由![]() 的转化关系及
的转化关系及![]() 的结构简式可知该反应为酯化反应;
的结构简式可知该反应为酯化反应;
(2)根据D、F的结构简式可知,2个D分子与1个甲醛分子发生反应生成F和H2O,则![]() 的化学方程式是2
的化学方程式是2  +HCHO
+HCHO +H2O ;
+H2O ;
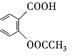
(3)①由于反应Ⅰ的另一种产物M能与NaHCO3溶液反应产生CO2,则M结构中含有羧基,结合M的相对分子质量可以得M为乙酸,结构简式是CH3COOH,B为![]() ;②
;②![]() 在酸性条件下发生水解反应产生邻羟基苯甲酸和乙酸,反应的化学方程式是
在酸性条件下发生水解反应产生邻羟基苯甲酸和乙酸,反应的化学方程式是![]() +H2O
+H2O![]()
 +CH3COOH;
+CH3COOH;
(4)a.D是![]() ,分子中无酯基,a错误;
,分子中无酯基,a错误;
b.由于乙烯中所有原子均在同一平面上,故![]() 中所有碳原子共平面,b正确;
中所有碳原子共平面,b正确;
c.D的同分异构体能使![]() 溶液显色,说明其结构中含有酚羟基,当苯环上的取代基为
溶液显色,说明其结构中含有酚羟基,当苯环上的取代基为![]() 和
和![]() 时,二者在苯环上有邻、间、对3种位置关系,当苯环上的取代基为
时,二者在苯环上有邻、间、对3种位置关系,当苯环上的取代基为![]() 和
和![]() 时,二者在苯环上有邻、间、对3种位置关系,当苯环上的取代基为2个
时,二者在苯环上有邻、间、对3种位置关系,当苯环上的取代基为2个![]() 和1个
和1个![]() 时,三者在苯环上有6种位置关系,故除D外,符合题意的
时,三者在苯环上有6种位置关系,故除D外,符合题意的![]() 的同分异构体有11种,c正确。
的同分异构体有11种,c正确。
答案选bc;
(5)结合题中的信息和所学知识,乙烯和甲苯合成![]() 的路线:
的路线:



 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】利用如图实验装置进行相关实验,能得出相应实验结论的是( )
a | b | c | 实验结论 |
| |
A | 浓醋酸 | CaCO3 | C6H5ONa溶液 | 酸性:碳酸>苯酚 | |
B | Br2的苯溶液 | 铁屑 | AgNO3溶液 | 苯和液溴发生取代反应 | |
C | 浓盐酸 | 酸性KMnO4溶液 | 碘化钾溶液 | 氧化性:Cl2>I2 | |
D | 饱和食盐水 | 电石 | 酸性KMnO4溶液 | 乙炔具有还原性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )

A.该反应的化学方程式为3B+2D![]() 6A+4C
6A+4C
B.反应进行到1s时,v(A)=3v(D)
C.反应进行到6s时,各物质的反应速率相等
D.反应进行到6s时,B的平均反应速率为0.05mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图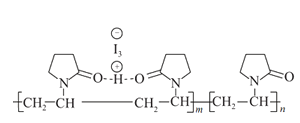 ,下列说法不正确的是( )
,下列说法不正确的是( )
A.聚维酮的单体是![]() B.聚维酮分子由(m+n)个单体聚合而成
B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质D.聚维酮在一定条件下能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素及其化合物的应用研究是目前科学研究的前沿之一。试回答下列问题:
(1)二氧化钛(![]() )作光催化剂,能将污染物如甲醛(
)作光催化剂,能将污染物如甲醛(![]() )、苯等有害气体转化为二氧化碳和水。水分子的中心原子的价电子对数为__________;甲醛的价电子对互斥理论模型为__________;二氧化碳分子中碳原子的杂化类型为____________________。
)、苯等有害气体转化为二氧化碳和水。水分子的中心原子的价电子对数为__________;甲醛的价电子对互斥理论模型为__________;二氧化碳分子中碳原子的杂化类型为____________________。
(2)写出下列分子或离子的空间构型:![]() __________;
__________;![]() __________。
__________。
(3)![]() 可与
可与![]() 形成H3O+,H3O+中O原子采取杂化_________。H3O+中键角比H2O中键角大,原因是______________________________。
形成H3O+,H3O+中O原子采取杂化_________。H3O+中键角比H2O中键角大,原因是______________________________。
(4)原子序数小于36的过渡元素A和B,在元素周期表中位于同一族,且原子序数B比A多1,基态B原子中含有三个未成对电子。则B在元素周期表中的位置为__________,属于__________区元素,基态B原子的电子排布式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰气的化学式为![]() ,结构式为
,结构式为![]() ,性质与卤素相似,下列有关叙述正确的是( )
,性质与卤素相似,下列有关叙述正确的是( )
A.氰气分子中既有极性键,又有非极性键
B.氰气分子中![]() 键的键长大于
键的键长大于![]() 键的键长
键的键长
C.氰气分子中含有2个![]() 键和4个
键和4个![]() 键
键
D.氰气不能和氢氧化钠溶液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
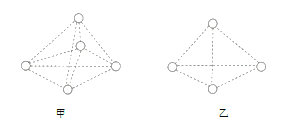
【题目】如图所示是甲烷和白磷![]() 分子的空间结构示意图,请你把认为是化学键的改为实线(在图上改即可)。把碳原子涂成实心小圆球_____。甲烷分子的空间结构是__________(填“甲”或“乙”)图。从图中可看出,每个甲烷分子中有__________对共用电子对,而白磷分子中形成__________个共价键。
分子的空间结构示意图,请你把认为是化学键的改为实线(在图上改即可)。把碳原子涂成实心小圆球_____。甲烷分子的空间结构是__________(填“甲”或“乙”)图。从图中可看出,每个甲烷分子中有__________对共用电子对,而白磷分子中形成__________个共价键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列四种晶体的晶胞示意图回答问题:
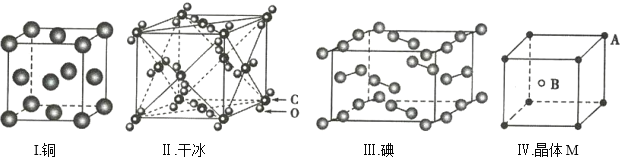
(1)根据图I分析,铜晶胞平均含有的铜原子数是___________。
(2)根据图Ⅱ分析,干冰晶胞平均含有的CO2分子数是___________。
(3)根据图Ⅲ分析,碘晶体中碘分子的排列有种不同的方向_________种不同的方向。
(4)根据图Ⅳ分析,晶体M的化学式可能是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中一定量混合气体发生反应:2 A(g)+2B(g)![]() xC(g),达到平衡时测得A的浓度为0.5mol/L,在温度不变的条件下,将容器中的容积扩大到原来2倍,再达平衡时,测得A的浓度为0.3mol/L,下列有关判断正确的是( )
xC(g),达到平衡时测得A的浓度为0.5mol/L,在温度不变的条件下,将容器中的容积扩大到原来2倍,再达平衡时,测得A的浓度为0.3mol/L,下列有关判断正确的是( )
A.x=4B.平衡向正反应方向移动
C.B的转化率降低D.C的体积分数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com