
【题目】爱迪生电池在充电和放电时发生反应:Fe+ NiO2+2H2O![]() Fe(OH)2+Ni(OH)2,下列该蓄电池推断错误的是
Fe(OH)2+Ni(OH)2,下列该蓄电池推断错误的是
①放电时,电解质溶液中的阴离子向正极方向移动
②放电时,Fe参与负极反应,NiO2参与正极反应
③放电时,负极上的电极反应式为:Fe + 2H2O- 2e- = Fe(OH)2 + 2H+
④充电时,阴极上的电极反应式为:Fe(OH)2 + 2e- = Fe + 2OH-
⑤蓄电池的电极必须浸入某种碱性电解质溶液中
A.③⑤ B.③④ C. ①③ D.①⑤
科目:高中化学 来源: 题型:
【题目】无水AlCl3易升华,可用作有机合成的催化剂等。工业上以铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
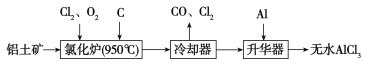
(1)为促进反应的进行,实际生产中需加入焦炭,其原因是
______________________________________________。
(2)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,此反应的离子方程式为
_______________________________________________。
(3)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】链型的不饱和油酸(C17H33COOH)与蔗糖反应可以制得非天然油脂,其反应示意图如图所示(图中的反应式不完整),则下列说法不正确的是( )
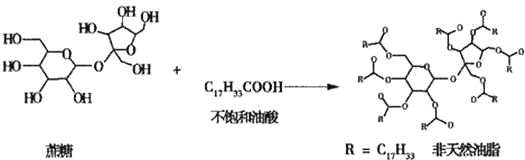
A. 该非天然油脂与氢氧化钠溶液共热,产物可与溴的四氯化碳溶液反应
B. 天然油脂、蔗糖、非天然油脂都能发生水解反应
C. 蔗糖、葡萄糖分别与银氨溶液水浴加热反应,有相同的实验现象
D. 植物油、非天然油脂都可以与H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的五种盐X、Y、Z、M、N,它们的阴离子可能是SO![]() 、Cl-、NO
、Cl-、NO![]() 、CO
、CO![]() ,阳离子可能是Ag+、NH
,阳离子可能是Ag+、NH![]() 、Na+、Al3+、Cu2+、Ba2+、Fe3+,已知:
、Na+、Al3+、Cu2+、Ba2+、Fe3+,已知:
①M的焰色反应呈黄色。
②五种盐均溶于水,水溶液均为无色。
③X的溶液呈中性,Y、Z、N的溶液呈酸性,M的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有X、Z的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,N和Z的溶液中生成沉淀,继续加氨水,Z中沉淀消失。
⑥把X的溶液分别加入到Y、Z、N的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,所含阴离子相同的两种盐的化学式是__________________
(2)M溶液显碱性的原因是(用离子方程式表示)______________________
(3)X和Z的溶液反应的离子方程式是_______________________
(4)N和氨水反应的离子方程式是___________________________
(5)若要检验Y中所含的阳离子,正确的实验方法是____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件。该小组同学为探究中毒原因进行了如下实验。
(1)小组同学依据漂白液具有漂白消毒的性质推测,漂白液中ClO-具有氧化性。实验如下:
Ⅰ. 用pH试纸检验,漂白液pH>7,饱和![]() 溶液pH<7。
溶液pH<7。
Ⅱ. 取10 mL漂白液,依次加入Na2SO3溶液和BaCl2溶液,有白色沉淀生成,经检验白色沉淀不溶于盐酸。
Ⅲ. 另取10 mL,漂白液,加入品红溶液,溶液红色逐渐变浅,一段时间后褪为无色。
Ⅳ. 再取10 mL漂白液,加入品红溶液,加入少量稀硫酸酸化后,溶液红色立即变为无色。
①漂白液pH大于7的原因是(用离子方程式表示)__________。
②由实验Ⅱ得出ClO-具有氧化性,写出相应的离子方程式__________。
③对比实验Ⅲ和Ⅳ说明ClO-氧化性与溶液酸碱性的关系是__________。
(2)小组同学依据(1)中的实验,提出:漂白液在酸性溶液中有Cl2生成。用图所示的装置继续实验,探究漂白液在酸性溶液中是否能反应生成Cl2。
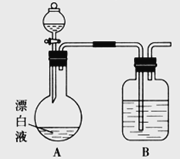
①装置B的作用是__________;盛放的药品是__________。
②若打开分液漏斗活塞向烧瓶中加入硫酸,不久烧瓶中有黄绿色气体产生。A中反应的离子方程式________。
③若打开分液漏斗活塞向烧瓶中加入饱和![]() 溶液,观察到产生大量的白色胶状沉淀,同时有黄绿色气体产生。A中加
溶液,观察到产生大量的白色胶状沉淀,同时有黄绿色气体产生。A中加![]() 溶液反应的离子方程式是__________。
溶液反应的离子方程式是__________。
(3)上述实验说明漂白液与酸性溶液混合会产生Cl2。若取10 mL漂白液与足量BaCl2溶液混合后,不断通入SO2至过量,在实验过程中可能的实验现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯的原子序数为17,37Cl和35Cl是氯的两种同位素,下列说法正确的是()
A. 35Cl原子所含质子数为18
B. ![]() mol的H35Cl分子所含中子数约为6.02×1023
mol的H35Cl分子所含中子数约为6.02×1023
C. 3.5 g的35Cl2气体的体积为2.24 L
D. 35Cl2气体的摩尔质量为70
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用下图装置探究氨的催化氧化。

(1)浓氨水中存在多种形式的氢键,用氢键表示式写出浓氨水中存在的所有氢键_________________。
(2)氨催化氧化的化学方程式为_____________________。
(3)加热玻璃管2一段时间后,挤压1中打气球鼓入空气,观察到2中物质呈红热状态;停止加热后仍能保持红热,该反应是_________反应(填“吸热”或“放热”)。
(4)三氧化二铬在反应中做催化剂。写出基态铬原子的核外电子排布式_________________;这样排布使整个体系能量最低,原因是 。
(5)若取消装置3,在装置4中仅观察到大量白烟,为保证在装置4中观察到红棕色气体,装置3应装入______________。
(6)为实现氨催化氧化,也可用装置5替换装置1,化合物X(一种)中存在的化学键类型________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com