
����Ŀ��ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W������Ԫ�ص�ԭ������֮��Ϊ32�������ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ�Y��Z�������ڣ�Z��Wλ��ͬ���壮�������ʵ�����X��Y�ĵ��ʳ���һ�ܱ������У����ʵ������ͺ��¡���ѹ�����·������淴Ӧ������˵���У���ȷ���ǣ� ��
A.�ﵽ��ѧƽ��ʱ������Ӧ�������淴Ӧ���ʲ����
B.��Ӧ�����У�Y�ĵ��ʵ��������ʼ��Ϊ50%
C.�ﵽ��ѧƽ��ʱ��X��Y�����ֵ����ڻ�������е����ʵ���֮��Ϊ1��1
D.�ﵽ��ѧƽ��Ĺ����У��������ƽ����Է���������С
���𰸡�B
���������⣺ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W�������ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ���XΪHԪ�أ�Z��Wλ��ͬ���壬��Z��ԭ������Ϊx����W��ԭ������Ϊx+8��Y��Z�������ڣ�Y��ԭ������Ϊx��1��������Ԫ�ص�ԭ������֮��Ϊ32����1+��x��1��+x+��x+8��=32�����x=8����YΪNԪ�أ�ZΪOԪ�أ�WΪSԪ�أ��÷�ӦΪN2+3H2 ![]() 2NH3 �� A�����ݻ�ѧƽ���������֪���ﵽ��ѧƽ��ʱ������Ӧ�������淴Ӧ������ȣ���A����
2NH3 �� A�����ݻ�ѧƽ���������֪���ﵽ��ѧƽ��ʱ������Ӧ�������淴Ӧ������ȣ���A����
B����������ʵ�����Y��Z���ֵ��ʷ�Ӧ�����Ϊn����������ʽ��
N2 + | 3H2 |
| 2NH3 | |
��ʼ���� | n | n | 0 | |
��ʼ���� | x | 3x | 2x | |
ijʱ�̣� | n��x | n��3x | 2x |
��Y���ʵ��������Ϊ ![]() ��100%=50%����B��ȷ��
��100%=50%����B��ȷ��
C��Y��Z��1��3�������ת������ﵽ��ѧƽ��ʱ��Y��Z���ֵ����ڻ�������е����ʵ���֮�Ȳ���Ϊ1��1����C����
D���������غ��֪���������䣬����Ӧ����������ʵ�����С������M= ![]() ��֪�ﵽ��ѧƽ��Ĺ���������ƽ����Է�����������D����
��֪�ﵽ��ѧƽ��Ĺ���������ƽ����Է�����������D����
���Դ��ǣ�B
�����㾫����������Ĺؼ��������⻯ѧƽ��ļ�������֪ʶ�����շ�Ӧ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������
��1����2L�ܱ������ڣ�800��ʱ������Ӧ��2NO��g��+O2��g��2NO2��g��������ϵ�У�n��NO����ʱ��ı仯�����
ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
NO�����ʵ�����mol�� | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��i��������Ӧ�ڵ�5sʱ��NO��ת����Ϊ ��
��ii����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v��O2��= ��
��iii����˵���÷�Ӧ�Ѵﵽƽ��״̬���� ��
a��v��NO2��=2v��O2�� b��������ѹǿ���ֲ���
c��v����NO��=2v����O2�� d�������������ܶȱ��ֲ���
��2���±��е��������ƻ�1mol�����еĻ�ѧ�������ĵ�������
���� | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
������kJ�� | 243 | 193 | 151 | 431 | 366 | 298 | 436 |
�����������ݻش��������⣺
��i���������ʱ������е�������͵��� ��
A��H2 B��Cl2 C��Br2 D��I2
��ii�������⻯�������ȶ����� ��
A��HCl B��HBr C��HI
��iii��X2+H2=2HX��X����Cl��Br��I���ķ�Ӧ�����ȷ�Ӧ���Ƿ��ȷ�Ӧ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л��ﺬC��H��O��N����Ԫ�أ����������ֱ�Ϊ32%��6.66%��42.67%��67%�����л��������������������ܶ�Ϊ37.5��ͨ������ȷ����
��1���л���ķ���ʽ��
��2���л�����ܵĽṹ��ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����Ȼ�ѧ����ʽ��
Zn��s��+ ![]() O2��g���TZnO��s����H1=��351.1kJ/mol
O2��g���TZnO��s����H1=��351.1kJ/mol
Hg��l��+ ![]() O2��g���THgO��s����H2=��90.7kJ/mol
O2��g���THgO��s����H2=��90.7kJ/mol
�ɴ˿�֪Zn��s��+HgO��s���TZnO��s��+Hg��l���ġ�H3 �� ���С�H3��ֵ�ǣ� ��
A.��441.8 kJ/mol
B.��254.6 kJ/mol
C.��438.9 kJ/mol
D.��260.4 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ص����ʳ��������Ա仯�ĸ���ԭ����
A. Ԫ�ص����ԭ������������ B. ��������Ų����������Ա仯
C. ԭ�Ӱ뾶���������Ա仯 D. Ԫ�ػ��ϼ۳��������Ա仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���Ӧ�У���һ����Ӧ������������Ӧ�ķ�Ӧ���Ͳ�ͬ���ǣ� ��
A.CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
B.2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
C.CH3CH2Br+NaOH ![]() CH3CH2OH+NaBr
CH3CH2OH+NaBr
D.![]() +Br2
+Br2 ![]()
![]() +HBr
+HBr
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.������KI��Һ��FeCl3��Һ��Ӧ����CCl4��ȡ���е�I2 �� ��Һ����ˮ��Һ�еμ�KSCN��Һ�Գ�Ѫ��ɫ��˵���÷�Ӧ��һ������
B.��һ�������£�һ��˫��ˮ��Ʒ����2h��H2O2��Ũ�ȴ�0.05molL��1�½���0.03 molL��1 �� ��˫��ˮ����2h�зֽ��ƽ����Ӧ����ԼΪ0.015 molL��1h��1
C.����������ͬʱ����Ӧ�¶����ߣ��������ȷ�Ӧ����Ӧ���ʼӿ죬���ڷ��ȷ�Ӧ����Ӧ���ʼ���
D.һ�������£��̶�����������з�����ӦA��g��+B��g��2C��g������������A��B��C��Ũ��֮��Ϊ1��1��2ʱ���÷�Ӧһ������ƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪһ������ȼ�ϵ�ؽṹʾ��ͼ�����ڸõ��������ȷ���ǣ� ��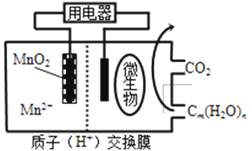
A.�������ΪCm��H2O��n������һ��������
B.�������ڵ缫���ŵ�ʱ������ԭ��Ӧ
C.�ŵ�����У�H+��������������
D.������ӦʽΪ��MnO2+4H++2e���TMn2++2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������������Ű�ҹ��ж������������У�����β����ȼúβ������ɿ�����Ⱦ��ԭ��֮һ��
��1������β����������Ҫԭ��Ϊ��2NO��g��+2CO��g�� ![]() 2CO2��g��+N2��g�������ܱ������з����÷�Ӧʱ��c��CO2�����¶ȣ�T���������ı������S����ʱ�䣨t���ı仯���ߣ���1ͼ��ʾ���ݴ��жϣ�
2CO2��g��+N2��g�������ܱ������з����÷�Ӧʱ��c��CO2�����¶ȣ�T���������ı������S����ʱ�䣨t���ı仯���ߣ���1ͼ��ʾ���ݴ��жϣ� 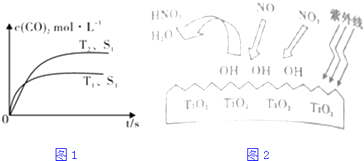
�ٸ÷�Ӧ�ġ�H0��ѡ�����������������
�ڵ��������������һ��ʱ�����������������ѧ��Ӧ���ʣ��������ı����S1��S2 �� ��ͼ�л���c��CO2����T2��S2�����´ﵽƽ������еı仯���� ��
���о������������������£�����TiO2�Ĵ����ã������е�ijЩ���ʻ����OH���ɻ�����ͼ2��ʾ��OH��NO2��ӦΪNO2+OH=HNO3 �� д��NO��OH��Ӧ�Ļ�ѧ����ʽ
��2��ֱ���ŷ�úȼ�ղ������������������صĻ������⣮
��úȼ�ղ����������������������CH4����ԭNOx�������������������Ⱦ��
���磺
CH4��g��+2NO2��g��=N2��g��+CO2��g��+2H2O��g����H=��867kJ/mol
2NO2��g��N2O4��g����H=��56.9kJ/mol
H2O��g��=H2O��l����H=��44kJ/mol
д��CH4��g������ԭN2O4��g������N2��g����CO2��g����H2O��l�����Ȼ�ѧ����ʽ�� ��
�ڽ�úȼ�ղ����Ķ�����̼�������ã��ɴﵽ��̼�ŷŵ�Ŀ�ģ�NH3��CO2��120�棬���������·�Ӧ�������أ�CO2��g��+2NH3��g����NH2��2CO��s��+H2O��g�����ֽ����ʵ���Ϊ1��1��NH3��CO2������ܱչ��������з�Ӧ��ƽ���NH3���������Ϊ20%����NH3��ƽ��ת����Ϊ ��
��25��ʱ����amolL��1�İ�ˮ��b molL��1����������ϣ���Ӧ����Һǡ�������ԣ���a��b��ʾNH3H2O�ĵ���ƽ�ⳣ��Ϊ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com