
【题目】下列物质中存在顺反异构体的是( )
A. 2-氯丙烯 B. 丙烯 C. 2-丁烯 D. 1-丁烯
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】在元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6 , 与其同周期的A、B、C、D四种元素,它们的原子最外层电子数依次为2、2、1、7,其中A、C两元素原子的次外层电子数为8,B、D两元素原子的次外层电子数为18,E、D两元素处于同族,且在该族元素中,E的气态氢化物的沸点最高.
(1)B元素在周期表中的位置;D元素基态原子电子排布式为 .
(2)E的气态氢化物在同族元素中沸点最高的原因是: .
(3)A、C两元素第一电离能> . (填元素符号)
(4)B元素能形成多种配合物.元素之间形成配合物的条件是:一方是能够提供孤对电子的原子,另一方是的原子.
(5)A元素可与氢元素形成离子化合物,电子式为;这种离子化合物可与水反应,化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A的结构简式如图所示,下列有关叙述中正确的是( ) 
A.有机物A与浓硫酸混合加热,可以发生消去反应
B.1 molA 与足量的H2发生加成反应,最多可以消耗4mol H2
C.1 molA 与足量的NaOH 溶液充分反应,最多可以消耗4 mol NaOH
D.有机物A 的同分异构体中能在稀硫酸存在下水解生成二苯酚的有6 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物在氧气中充分燃烧,生成等物质的量的水和二氧化碳,则该有机物必须满足的条件是()
A. 分子中的C、H、O的个数比为1:2:3 B. 分子中C、H个数比为1:2
C. 该有机物的相对分子质量为14 D. 该分子中肯定不含氧元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOHCH3COO﹣+H+ , 要使溶液中 ![]() 值增大,可以采取的措施是( )
值增大,可以采取的措施是( )
A.加少量烧碱溶液
B.降低温度
C.加少量冰醋酸
D.加水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我们可以将SiO2的晶体结构想象为在晶体硅的Si—Si键之间插入O原子。根据SiO2晶体结构图,下列说法不正确的是( )
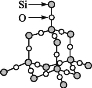
A.石英晶体中每个Si原子通过Si—O极性键与4个O原子作用
B.每个O原子也通过Si—O极性键与2个Si原子作用
C.石英晶体中Si原子与O原子的原子个数比为1∶2,可用“SiO2”来表示石英的组成
D.在晶体中存在石英分子,故能叫分子式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中有错误的是
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B. 实验室制取蒸馏水的装置中,温度计水银球应与蒸馏烧瓶的支管口在同一水平线
C. 用淘洗的方法从沙里淘金
D. 用蒸发方法使NaCl从溶液中析出时,应边加热边搅拌直至溶液蒸干
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)常温下,0.1mol/LHCl溶液的pH=;0.005mol/LBa(OH)2溶液的pH=;
(2)常温下,pH=13的Ba(OH)2溶液aL与pH=3的H2SO4溶液bL混合(混合后溶液体积变化忽略不计)
①若所得混合溶液呈中性,则a:b=;
②若所得混合溶液pH=12,则a:b= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“一带一路”将为中国化工企业开辟新的国际市场,其中,能源、资源整合和环境治理是保驾护航的基础.
(1)下面是不同过程的热化学方程式,请写出FeO(s)被CO还原成Fe和CO2的热化学方程式 已知:Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H1=﹣25kJmol﹣1①
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H2=﹣47kJmol﹣1②
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H3=+19kJmol﹣1③
(2)贵金属的冶炼中往往会产生有毒气体,先进技术使用NaBH4为诱导剂,可使Co2+与肼(N2H4)在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体. ①写出该反应的离子方程式: .
②在纳米钴的催化作用下,肼可以发生分解反应3N2H4(g) ![]() N2(g)+4NH3(g)
N2(g)+4NH3(g)
保持温度不变,向容积固定的容器中充入一定量的肼,下列描述能够说明体系处于平衡状态的是
a.容器内压强不随时间改变
b.单位时间内生成amol N2的同时,生成4molNH3
c.N2H4和NH3的物质的量之比保持不变的状态
d.混合气体的平均摩尔质量保持不变的状态
若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图1所示,其中曲线b表示的是(物质的化学式)的体积分数随温度的变化情况,为抑制肼的分解,可采取的合理措施有(任写一种).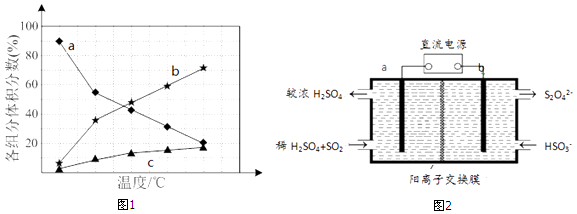
(3)大气污染气的主要成分是SO2和NO2 . 利用图2所示装置(电极均为惰性电极)可以吸收SO2 , 还可以用阴极排出的溶液吸收NO2 . ①a极为(填“阴”“阳”) b极的电极反应式为 .
②简述该装置能吸收SO2的原理: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com