
| A、5种 | B、6种 |
| C、7种 | D、8 种 |


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
| A、H2、I2、HI的浓度相等 |
| B、1个I-I键断裂的同时,有2个H-I键断裂 |
| C、混合气体的质量不再改变 |
| D、混合气体密度恒定不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素的非金属性:X<Y<Z |
| B、在元素周期表中它们依次处于第ⅦA族、第ⅥA族、第ⅤA族 |
| C、酸性:H3ZO4>H2YO4>HXO4 |
| D、气态氢化物的稳定性:HX>H2Y>ZH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾能起催化剂作用 |
| B、明矾更易使碳酸氢钠发生分解反应 |
| C、明矾受热分解放出气体 |
| D、明矾在水中能起到酸的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
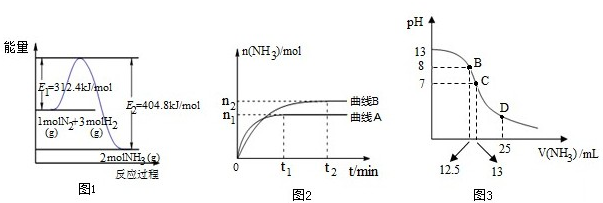
| n1 |
| 4t1 |
| 7 |
| 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学生为了验证苯酚、醋酸、碳酸的酸性强弱,设计了如图实验装置,请回答下列问题:
某学生为了验证苯酚、醋酸、碳酸的酸性强弱,设计了如图实验装置,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com