
| A、澄清的石灰水与稀盐酸反应Ca(OH)2+2H+═Ca2++2H2O | ||||
| B、钠与水的反应Na+2H2O═Na++2OH-+H2↑ | ||||
| C、硫酸氢钠溶液与少量氢氧化钡溶液混合:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | ||||
D、向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O
|
| ||


科目:高中化学 来源: 题型:
| A、分液时,分液漏斗中下层液体从下口放出后,换个洁净的烧杯,将上层液体从上口放入烧杯中 |
| B、蒸馏时,应使温度计水银球位于蒸馏烧瓶支管口处 |
| C、用酒精萃取溴水溶液中的溴 |
| D、称量时,将称量物体放在称量纸或烧杯中,置于托盘天平的左盘,砝码放在托盘天平的右盘 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、H+、I-、MnO4- |
| B、Fe3+、Fe2+、SO42-、NO3- |
| C、Al3+、Na+、SO42-、CO32- |
| D、Fe3+、H+、SO42-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol氢气完全燃烧吸热246.8 kJ |
| B、1mol水蒸气和1mol硫化氢的能量相差221.7 kJ |
| C、由①②知,水的热稳定性小于硫化氢 |
| D、若反应②中改用固态硫,放热将小于20.1 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在水中形成的分散系属于悬浊液 |
| B、分子直径比Na+小 |
| C、“钴酞菁”分子不能透过滤纸 |
| D、在水中形成的分散系具有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
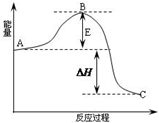 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.请回答下列问题:
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
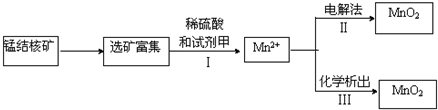
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com