
【题目】将Na2O2逐渐加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入的Na2O2物质的量(mol)的关系如图所示,则原溶液中的Mg2+、Al3+、NH4+物质的量分别( ) 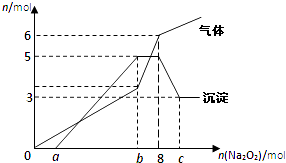
A.2 mol、3 mol、6 mol
B.3 mol、2 mol、6mol
C.2 mol、3 mol、4 mol
D.3 mol、2 mol、2 mol
 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:
【题目】t℃时,某NaOH稀溶液中,c(H+)=10﹣amol/L,c(OH﹣)=10﹣bmol/L,已知a+b=12.
(1)该温度下,水的离子积常数Kw= .
(2)在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH= , 此时该溶液中由水电离的c(OH﹣)= .
(3)该温度下,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在密闭容器中进行SO2的催化氧化反应.若起始时c(SO2)=c(O2)=6mol/L,平衡时测得c(O2)=4.5mol/L,则下列叙述中正确的是( )
A.SO2的转化率为60%
B.SO3的产率为60%
C.平衡时总压强与起始压强之比为7:8
D.平衡时V(SO2):V(O2):V(SO3)=3:3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍是重要的有色金属之一,但粗镍中一般含有Fe、Cu及难与酸、碱溶液反应的不溶性杂质而影响使用.现对粗镍进行提纯,具体的反应流程如下: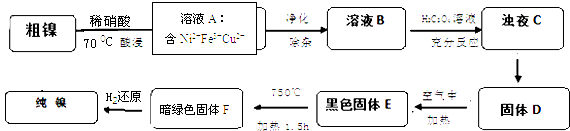
已知:
①2Ni2O3(黑色) ![]() 4NiO(黑色)+O2↑
4NiO(黑色)+O2↑
②
物质 | CuS | Cu(OH)2 | Ni(OH)2 | NiS |
Ksp | 8.8×10﹣38 | 2.2×10﹣20 | 5.48×10﹣18 | 3.2×1018 |
根据信息回答:
(1)28Ni在周期表中的第周期;镍与稀硝酸反应的离子方程式为 . 实验表明镍的浸出率与温度有关,随着温度升高镍的浸出率增大,但当温度高于70℃时,镍的浸出率又降低,浸出渣中Ni(OH)2含量增大,其原因为;
(2)在溶液A的净化除杂中,先调节PH=5.5,加热煮沸5min,静置一段时间后,过滤出Fe(OH)3 . 为了得到纯净的溶液B还需要加入以下物质进行除杂(填正确答案标号).
A.NaOH
B.Na2S
C.H2S
D.NH3﹒H2O
(3)已知以下三种物质的溶解度关系:NiC2O4>NiC2O4H2O>NiC2O42H2O.由浊液C得到固体D的操作包括过滤、、(填操作名称); D生成E的化学方程式为
(4)1molE经上述流程得到纯镍,理论上参加反应的氢气为 mol.
(5)测定样品中的镍含量的基本思路是将Ni2+转化为沉淀,通过测量沉淀的质量进一步推算Ni含量.已知Ni2+能与CO32﹣ , C2O42﹣、S2﹣等离子形成沉淀,但测定时常选用丁二酮肟(C4H8N2O2)作沉淀剂,生成分子式为C8H14N4O4Ni的鲜红色沉淀.从实验误差角度分析主要原因为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1L的密闭容器中,加入1.0mol A和2.2mol B进行如下反应:A(g)+2B(g)C(g)+D(g),在800℃时,D的物质的量n(D)和时间t的关系如图. 
(1)800℃时,0~5min内,以B表示的平均反应速率为 .
(2)利用图中数据计算在800℃时的平衡常数的数值为 .
(3)若700℃,反应达平衡时,A的浓度为0.55mol/L,则该反应为反应(填“吸热”或“放热”).
(4)800℃时,某时刻测得体系中物质的量浓度如下:c(A)=0.06molL﹣1 , c(B)=0.50molL﹣1 , c(C)=0.20molL﹣1 , c(D)=0.018molL﹣1 , 则此时该反应(填“向正方向进行”、“向逆方向进行”或“处于平衡状态”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如下图所示(部分产物及反应条件已略去).已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀. 
请回答下列问题:
(1)B中所含元素位于周期表中第周期,族.
(2)A在B中燃烧的现象是 .
(3)D+E→B的反应中,被氧化与被还原的物质的物质的量比是 .
(4)G+J→M的离子方程式是 .
(5)Y受热分解的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷和红磷均能在空气中燃烧,且燃烧产物相同,但二者的燃烧热不同,通过实验可测得这两个反应的反应热. ① ![]() P4(s,白磷)+
P4(s,白磷)+ ![]() O2(g)═
O2(g)═ ![]() P4O10(s)△H1=﹣745.8kJmol﹣1
P4O10(s)△H1=﹣745.8kJmol﹣1
②4P(s,红橉)+5O2(g)═P4O10(s)△H2=﹣2954kJmol﹣1
(1)白磷和红磷的关系是 . a.同一种物质 b.同位素 c.同分异构体 D.同素异形体
(2)红磷的燃烧热是kJmol﹣1 , 白磷的燃烧热比红磷的燃烧热(填“大”或“小”).
(3)白磷转化为红磷的热化学方程式为P4(s,白磷)═4P(s,红磷)△H=﹣29.2kJmol﹣1 . 在相同的条件下,能量较低的是(填“白磷”或“红磷”),白磷的稳定性比红磷(填“高”或“低”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com