
����Ŀ���������糧�ͷų���������������(NOx)��SO2��CO2���������ɻ������⡣��ȼú���������������������̼�ȴ�������ʵ����ɫ���������ܼ��š��������õ�Ŀ�ġ�
(1)���������ü������ԭNOx��
CH4(g)�� 4NO2(g)��4NO(g)�� CO2(g)�� 2H2O(g) ��H1����574 kJ/mol
CH4(g)�� 4NO(g)��2N2(g)�� CO2(g)�� 2H2O(g) ��H2����1160 kJ/mol
����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ__________________________��
(2)��̼����CO2ת��Ϊ�״���CO2(g)��3H2(g)![]() CH3OH(g)��H2O(g)��H3
CH3OH(g)��H2O(g)��H3
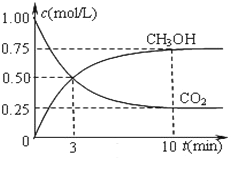
��һ���º����ܱ������г���1 mol CO2��3 mol H2���з�Ӧ�����CO2��CH3OH(g)Ũ����ʱ��仯��ͼ��ʾ���ش�0��10 min�ڣ�������ƽ����Ӧ����Ϊ___mol/(L��S)����10 min�����¶Ȳ��䣬����ܱ��������ٳ���1 mol CO2(g)��1 mol H2O(g)����ƽ��_________(����������������������������)�ƶ���
������ͼ��ʾC��D��E��F��X��Y���Ƕ��Ե缫������Դ��ͨ����(��)�е����̪��Һ����F�������Ժ�ɫ��
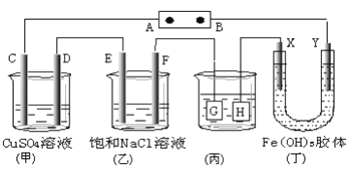
(1)���ü״�������ȼ�ϵ������Դ�������ΪKOH��Һ����A���ĵ缫��ӦʽΪ_________________________
(2)����(��)װ�ø�ͭ��������Ӧ���� _____�缫(��G��H)
(3)(��)װ����Y���������ɫ��_______(�����dz)
(4)ͨ��һ��ʱ���C��D��E��F�缫���е������ɣ������ʵ���֮��Ϊ_____________
���𰸡�CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)��H��-867 kJ/mol 0.00375 ���� O2 + 4e- + 2H2O = 4OH- G �� 1:2:2:2
��������
���ݻ�ѧƽ�������ʽ���м�������ʵ�Ũ�Ⱥ�ƽ�ⳣ��������Ũ���̺�ƽ�ⳣ���Ĺ�ϵ������Ӧ���еķ����ݵ��ԭ�������������еĵ缫��Ӧ������
(1)���ݸ�˹���ɷ������� CH4(g)�� 4NO2(g)��4NO(g)�� CO2(g)�� 2H2O(g) ��H1����574 kJ/mol����CH4(g)�� 4NO(g)��2N2(g)�� CO2(g)�� 2H2O(g) ��H2����1160 kJ/mol
��+�ڿɵ��Ȼ�ѧ����ʽΪCH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)��H����1160��574 =-867 kJ/mol��
(2).���ݷ���ʽ����
CO2(g)��3H2(g)![]() CH3OH(g)��H2O(g)
CH3OH(g)��H2O(g)
��ʼŨ��1.0 3.0 0 0
�ı�Ũ�� 0.75 2.25 0.75 0.75
ƽ��Ũ��0.25 0.75 0.75 0.75
0��10 min�ڣ�������ƽ����Ӧ����Ϊ2.25mol/L��600s=0.00375mol/(L��s)��ƽ�ⳣ��Ϊ![]() ����10 min�����¶Ȳ��䣬����ܱ��������ٳ���1 mol CO2(g)��1 mol H2O(g)����Qc=
����10 min�����¶Ȳ��䣬����ܱ��������ٳ���1 mol CO2(g)��1 mol H2O(g)����Qc=![]() <K��ƽ��������С�
<K��ƽ��������С�
����(��)�е����̪��Һ����F�������Ժ�ɫ��˵��F��Ϊ�����ӷ�Ӧ������������Һ��ʣ�����������ӣ�����FΪ��������Ӧ��BΪ������AΪ������ (1) ���ü״�������ȼ�ϵ������Դ�������ΪKOH��Һ��A Ϊ�������缫��ӦΪO2 + 4e- + 2H2O = 4OH- ��
(2) ����(��)װ�ø�ͭ��������Ӧ������������ΪG����
(3)��Ϊ������������ĵ�Ӿ����Ϊ��������������������ɣ�����������Y�������ɫ���
(4)ͨ��һ��ʱ���C������������D�ϲ���ͭ��E�ϲ���������F�ϲ������������ݵ����غ�������缫�ϵIJ�������ʵ�����Ϊ1:2:2:2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����ȡ�������Ҫ��Ӧ��SiCl4 + 2H2 ![]() Si + 4HCl���÷�Ӧ�У�����ԭ��������______(�ѧʽ)����Ϊ��ԭ����������______(�ѧʽ)������Ӧ��������1 mol Si��������H2 ______mol��
Si + 4HCl���÷�Ӧ�У�����ԭ��������______(�ѧʽ)����Ϊ��ԭ����������______(�ѧʽ)������Ӧ��������1 mol Si��������H2 ______mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܱ������зֱ����N2��H2��O2�������壬���¸��������������ȷ���ǣ� ��
A. �����ǵ��¶Ⱥ�ѹǿ����ͬʱ������������ܶȣ�����H2��������N2��������O2��
B. �����ǵ��¶Ⱥ��ܶȶ���ͬʱ�����������ѹǿ��p��H2����p��N2����p��O2��
C. �����ǵ��������¶ȡ�ѹǿ����ͬʱ����������������V��O2����V��N2����V��H2��
D. �����ǵ�ѹǿ��������¶Ⱦ���ͬʱ�����������������m��H2����m��N2����m��O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ�������ӽ���Ĥȼ�ϵ�ؽ���ѧ��ת��ɵ��ܵ�ͬʱ��ʵ���������ᡢ���硢������λһ��Ľ�ϣ���ԭ����ͼ��ʾ������˵���������

A. �����ĵ缫��ӦʽΪSO2+2H2O��2e��=SO42��+4H+
B. ��Ӧ��ʽΪ2SO2+O2+2H2O=2H2SO4
C. ���ӵ��ƶ�����Ϊ�ӵ缫B���缫A
D. SO2�����ٶȵĴ�С����Ӱ���صĵ綯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
������E(��������)������CT��顢��������Ӱ�ȣ���һ�ֺϳ�·�����£�

(1)A�к��еĺ���������Ϊ___________���١����в�����ȡ����Ӧ����___________��
(2)C�Ľṹ��ʽΪ___________��ҩƷ�е�������ĺ���ͨ�����òⶨҩƷ�е����ķ�������ⶨ������Ҫ�õ����Լ�Ϊ______________________��
(3)B�ж���ͬ���칹�壬��������������ͬ���칹��Ľṹ��ʽΪ___________��
�ٱ����������ȡ���� ��lmol����2 molNaHCO3������Ӧ
���ܷ���������Ӧ �ܺ˴Ź�������ֻ��4����ֵ
(4)��֪���ٱ���(![]() )�ױ�����
)�ױ�����
![]()

���Լױ���(CH3CO)2OΪԭ���Ʊ� ��д����Ӧ�ĺϳ�·������ͼ___________(���Լ���ѡ���ϳ�·������ͼʾ�����������)��
��д����Ӧ�ĺϳ�·������ͼ___________(���Լ���ѡ���ϳ�·������ͼʾ�����������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʹҩ��![]() �ĺϳɷ������£�
�ĺϳɷ������£�

��֪��
(1)![]() ������Ϊ_________________���ڵķ�Ӧ����Ϊ_________________��Ӧ��
������Ϊ_________________���ڵķ�Ӧ����Ϊ_________________��Ӧ��
(2)![]() �Ľṹ��ʽΪ_________________.
�Ľṹ��ʽΪ_________________.![]() �к��������ŵ�����Ϊ_________________.
�к��������ŵ�����Ϊ_________________.
(3)�۵Ļ�ѧ����ʽΪ__________________________________��
(4)�л���![]() ������ɱ�
������ɱ�![]() ��������ԭ�ӣ���������Ҫ���
��������ԭ�ӣ���������Ҫ���![]() ��ͬ���칹����_________�֡�
��ͬ���칹����_________�֡�
A ��![]() ����ɫ B ������������ȡ����
����ɫ B ������������ȡ����
(5)��֪����һ���ķ�Ӧ�ȣ���Ӧ����ʱ�������(![]() �������л���)�����
�������л���)�����![]() �IJ��ʣ�ԭ����___________________________________________________��
�IJ��ʣ�ԭ����___________________________________________________��
(6) ����һ����Ҫ�Ļ����м��塣�Ի�����(
����һ����Ҫ�Ļ����м��塣�Ի�����(![]() )���Ҵ�Ϊ��ʼԭ�ϣ���ϼ�֪��Ϣѡ���Ҫ�����Լ���д��
)���Ҵ�Ϊ��ʼԭ�ϣ���ϼ�֪��Ϣѡ���Ҫ�����Լ���д�� �ĺϳ�·�ߡ�
�ĺϳ�·�ߡ�
(��֪��![]()
![]() ��
��![]() Ϊ�������ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ����)________________________________
Ϊ�������ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ����)________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����![]() ��
��![]() ��Ӧ����ȡ������
��Ӧ����ȡ������![]() ����˵����ȷ����
����˵����ȷ����
A. �÷�Ӧ��������ֻ��![]() B.
B. ![]() �ĵ���ʽΪ
�ĵ���ʽΪ
C. ![]() ��ϡ���������ӦD. �÷�Ӧ��ÿ����
��ϡ���������ӦD. �÷�Ӧ��ÿ����![]() ,ת�Ƶĵ�����Ϊ
,ת�Ƶĵ�����Ϊ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���ʵ����Ԫ�����ڱ��IJ��ֱ߽磬�����ϱ߽粢δ��ʵ�߱����

������Ϣ�ش��������⡣
��1�����ڱ��л�̬Gaԭ�ӵ����������Ų�ʽΪ ��
��2��FeԪ��λ�����ڱ��� ����Fe��CO���γ������Fe(CO)5����Fe(CO)5�����Ļ��ϼ�Ϊ ����֪��ԭ����Ŀ�͵�������(��۵�������)��ͬ������Ϊ�ȵ����壬�ȵ�����������ƵĽṹ��������CO���ӻ�Ϊ�ȵ�����ķ��Ӻ����ӷֱ�Ϊ �� (�ѧʽ)��
��3����CH4��CO2��CH3OH�У�̼ԭ�Ӳ�ȡsp3�ӻ��ķ����� ��
��4������VSEPR����Ԥ��ED4-���ӵĿռ乹��Ϊ ��B��C��D��Eԭ��������γɵķ����У�����ԭ�Ӷ����������8�����ȶ��ṹ�ķ��ӵĵ���ʽΪ (д2��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ��д��ȷ����(��H�ľ���ֵ����ȷ)
A. C2H5OH(l)+3O2(g)![]() 2CO2(g)+3H2O(g)����H=1 367.0 kJ/mol(ȼ����)
2CO2(g)+3H2O(g)����H=1 367.0 kJ/mol(ȼ����)
B. NaOH(aq)+HCl(aq)![]() NaCl(aq)+H2O(l)����H=+57.3 kJ/mol(���)
NaCl(aq)+H2O(l)����H=+57.3 kJ/mol(���)
C. S(s)+O2(g)![]() SO2(g)����H=296.8 kJ/mol(��Ӧ��)
SO2(g)����H=296.8 kJ/mol(��Ӧ��)
D. 2NO2![]() O2+2NO����H=+116.2 kJ/mol(��Ӧ��)
O2+2NO����H=+116.2 kJ/mol(��Ӧ��)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com