
【题目】下列有关晶体的叙述中,不正确的是( )
A.氯化钠和氯化铯晶体中,阳离子的配位数均为6
B.金刚石为三维网状结构,由碳原子以sp3杂化轨道形成共价键
C.金属钠的晶体采用体心立方堆积,每个晶胞含2个原子,配位数为8
D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
【答案】A
【解析】解:A、氯化钠晶体中氯离子配位数为6、氯化铯晶体中氯离子的配位数为8,则氯化钠和氯化铯晶体中氯离子的配位数不相同,故A错误;
B、金刚石为三维网状结构,一个碳与四个碳原子形成共价键,所以碳原子以sp3杂化,故B正确;
C、金属钠的晶体采用体心立方堆积,所以每个晶胞含1+8× ![]() 个原子,每个钠原子周围距离最近的钠原子有8个,所以配位数为8,故C正确;
个原子,每个钠原子周围距离最近的钠原子有8个,所以配位数为8,故C正确;
D.采用沿X、Y、Z三轴切割的方法判断二氧化碳分子的个数为12,所以在CO2晶体中,与每个CO2分子周围紧邻的有12个CO2分子,故D正确;
故选A.
【考点精析】通过灵活运用离子晶体和原子晶体,掌握离子间通过离子键结合而成的晶体叫作离子晶体;相邻原子间以共价键相结合而形成空间网状结构的晶体叫原子晶体即可以解答此题.


科目:高中化学 来源: 题型:
【题目】三室式电渗析祛处理废液(HCl和FeCl2混合溶液)的原理如图所示,其中X、Y均为离子交换膜。在直流电场的作用下,中间室得到盐酸,阴极区可回收铁。下列说法正确的是
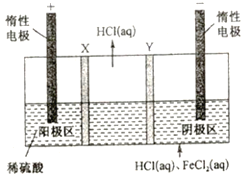
A. X、Y依次是阴离子透过膜和阳离子透过膜
B. 通电后,阴极区溶液的pH不断减小
C. 阳极反应式为2H2O-4e-==4H++O2↑
D. 中间室得到1L2mol/L盐酸时,电路中通过1mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应A(g)+B(g)![]() 2C(g)+D(s)△H>0,向1L绝热容器中加入1molA和1molB发生反应,下列叙述不能作为该反应达到平衡状态的标志的是( )
2C(g)+D(s)△H>0,向1L绝热容器中加入1molA和1molB发生反应,下列叙述不能作为该反应达到平衡状态的标志的是( )
①单位时间内消耗amolA,同时生成2amolC
②混合气体的总压强不再变化
③混合气体的密度不再变化
④A、B、C的分子数之比为1∶1∶2
⑤反应容器中温度不变
⑥A的转化率与B的转化率相等时
A. ①②④⑥ B. ②④⑥ C. ①④⑥ D. ①②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茉酚是一种重要的有机化工原料。利用苯酚合成已二醛[OHC(CH2)4CHO]和尼龙6(![]() )的合成路线如下:
)的合成路线如下:

已知:I.  ;
;
II.  。
。
回答下列问题:
(1)由A制取B的反应类型为_______;C的化学名称为___________。
(2)E的结构简式为____________。
(3)上述流程中合成尼龙6的化学方程式为_____________________。
(4)已二醛与银氨溶液反应的化学方程式为___________________。
(5)已二醛的同分异构休中既含五元环结构,又含“ ” 结构的有_____种(不考虑立体异构);其中核磁共振氢谱有三组峰的结构简式有_________________。
” 结构的有_____种(不考虑立体异构);其中核磁共振氢谱有三组峰的结构简式有_________________。
(6)写出以溴乙烷为原料(其他试剂任选)制备甲醛的合成跻线:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用标准NaOH溶液滴定充满HCl的烧瓶(标况下)做完喷泉实验后得到的稀盐酸,以测定它的准确浓度,请你回答下列问题:
(1)理论计算该盐酸的物质的量浓度为:________________________________。
(2)若用甲基橙作指示剂,达到满定终点时的现象是___________________________。
(3)现有三种浓度的标准NaOH溶液,你认为最合适的是下列第__________种。
①5.00mol·L-1 ②0.500mol·L-1 ③0.0500mol·L-1
(4)若采用上述最合适浓度的标准NaOH溶液满定,滴定时实验数据列表如下:
实验次数编号 | 待测盐酸体积(mL) | 滴入NaOH溶液体积(mL) |
1 | 10.00 | 8.48 |
2 | 10.00 | 8.52 |
3 | 10.00 | 8.00 |
求这种待测稀盐酸的物质的量浓度c(HCl)=___________________。
(5)在滴定操作过程中,以下各项操作使测定值偏高的有:_______________
①滴定管用蒸馏水洗净后,未用已知浓度的标准溶液润洗
②滴定管(装标准溶液)在滴定前尖嘴处有气泡,滴定终了无气泡
③滴定前平视,滴定终了俯视
④看到颜色变化后立即读数
⑤洗涤锥形瓶时,误把稀食盐水当做蒸馏水进行洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3是一种重要的化工原料。
(1)不同温度、压强下.合成该平衡体系NH3的物质的量分数如图 (N2和H2的起始物质的量之比为1:3)。
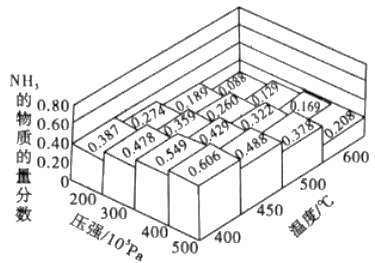
①分析图中数据,升高温度,该反应的平衡常数K值____(填“增大”“减小”或“不变”)。
②如果开始时向密闭容器中投入1.0mol N2 和3.0mol H2,则在500℃、3×107Pa条件下达到平衡时N2 的平衡转化率=_______。(保留两位有效数字)
③液氨和水颇为相像,它能溶解多种无机及有机分子,其电离方程式可表示为2NH3 ![]() NH4++ NH2一(某温度下其离子积常数为10-30)。液氨中的pNH4与水中的pH相似,则该温度下液氨的pNH4=____。
NH4++ NH2一(某温度下其离子积常数为10-30)。液氨中的pNH4与水中的pH相似,则该温度下液氨的pNH4=____。
(2)以氨气代替氢气研发氨清洁燃料电池是当前科研的一个热点。氨燃料电池使用的电解质溶液是KOH溶液。该电池负极的电极反应式为_________________。
(3)NH3也是造成水体富营养化的重要因素之一,用次氯酸钠水解生成的次氯酸将水中的NH3转化为氮气除去,其相关反应的热化学方程式如下:
反应I: NH3 (aq)+HClO(aq)=NH2Cl(aq)+H2O(l) △H1=akJ/mol;
反应II :NH2Cl(aq)+HClO(aq)=NHCl2(aq) +H2O(l) △H2=bkJ/mol;
反应III: 2NHCl2(aq) +H2O(l)=N2(g)+HClO( aq)+3HCl( aq) △H3=ckJ/mol。
①2NH3(aq)+3HClO(aq)==N2 (g)+3HCl(aq)+3H2O(l) △H=________kJ/mol
②已知在水溶液中NH2Cl较稳定,NHCl2不稳定易转化为氮气。在其他条件不变的情况下,改变![]() 对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量)的影响如图所示。a点之前溶液中发生的主要反应为_______(填序号)。
对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量)的影响如图所示。a点之前溶液中发生的主要反应为_______(填序号)。
A.反应I、I I B.反应I

③除氨氮过程中最佳的![]() 值约为______________。
值约为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中可以大量共存,加OH-产生沉淀,加H+生成气体的一组离子是( )
A.Na+、Cu2+、CO32-、Cl-
B.Na+、 Cl-、 HCO3-、Mg2+
C.Cl-、NO3-、K+、 Ca2+
D.NH4+、 K+、 H+、 SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A(g)+B(g)C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 900 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= , △H0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003molL﹣1s﹣1 . ,则6s时c(A)= molL﹣1 , C的物质的量为mol;若反应经一段时间后,达到平衡时A的转化率为 , 如果这时向该密闭容器中再充入1mol氩气,平衡时A的转化率为;
(3)判断该反应是否达到平衡的依据为(填正确选项前的字母): a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时问改变 d.单位时间里生成c和D的物质的量相等
(4)1200℃时反应C(g)+D(g)A(g)+B(g)的平衡常数的值为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com