
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是
A.标准状况下,22.4 L H2O含有的分子数为NA
B.常温常压下,1.06 g Na2CO3含有的Na+离子数为0.02NA
C.通常状况下,NA个CO2分子占有的体积为22.4 L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为1
科目:高中化学 来源: 题型:
【题目】下列变化不能用勒夏特列原理解释的是
A. 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率
B. H2、I2(g)混合气体加压后颜色变深
C. 红棕色的NO2加压后颜色先变深再变浅
D. 实验室用排饱和食盐水的方法收集氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.将0.10 mol·L-1氨水加水稀释后,溶液中c(![]() )·c(OH-)变大
)·c(OH-)变大
B.为确定某酸H2A是强酸还是弱酸,可测H2A溶液与H2SO4溶液的导电性。若导电性比硫酸弱,则H2A是弱酸。
C.将CH3COOH溶液加水稀释后,溶液中 变大
变大
D.用0.200 0 mol·L-1NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合溶液中两种酸的浓度均为0.1 mol·L-1),至中性时,溶液中的酸未被完全中和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。
Ⅰ.(1)有机物![]() 的名称为________, 其与Br2加成时(物质的量之比为1:1),所得产物有______种。
的名称为________, 其与Br2加成时(物质的量之比为1:1),所得产物有______种。
(2)分子式为C9H12属于芳香烃的同分异构体共有________种,其中___________(填结构简式)的一溴代物只有两种。
(3)有机物A的结构简式为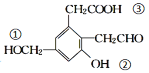 ,若取等质量的A分别与足量的Na、NaOH、H2充分反应,理论上消耗这三种物质的物质的量之比为_________,有机物A中标有序号①、②、③处羟基上氢原子的活泼性由强到弱顺序为___________。
,若取等质量的A分别与足量的Na、NaOH、H2充分反应,理论上消耗这三种物质的物质的量之比为_________,有机物A中标有序号①、②、③处羟基上氢原子的活泼性由强到弱顺序为___________。
Ⅱ.根据下面的反应路线及所给信息填空。
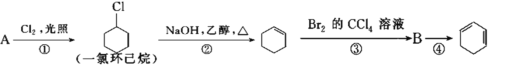
(4)A的结构简式是________。
(5)①、③的反应类型分别是_________、________。
(6)反应④的化学方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1mol·L-1NaOH溶液滴定新配制的25.0mL0.02 mol·L-1FeSO4溶液,应用手持技术测定溶液的pH与时间(t)的关系,结果如右图所示。下列说法错误的是
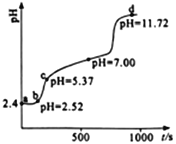
A. ab段,溶液中发生的主要反应:H++OH-=H2O
B. bc段,溶液中c(Fe2+) > (Fe3+) >c(H+)>c(OH-)
C. d点,溶液中的离子主要有Na+、SO42-、OH-
D. 滴定过程发生了复分解反应和氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为常温下![]() 溶液逐滴加入到
溶液逐滴加入到![]() 溶液中pH的变化曲线,下列说法 不正确的是
溶液中pH的变化曲线,下列说法 不正确的是

A.在![]() 区间内某点,两溶液恰好完全反应
区间内某点,两溶液恰好完全反应
B.反应过程中溶液中阴、阳离子总数:b点小于c点
C.![]() 区间内
区间内![]() 不包含a、c两点
不包含a、c两点![]() 可能存在:
可能存在:![]()
D.d点时溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时, H3A 水溶液(一种酸溶液)中含 A 的各种粒子的分布分数(平衡时某种粒子的浓度占各种粒子浓度之和的分数(α)与 pH 的关系如图所示。下列叙述正确的是( )
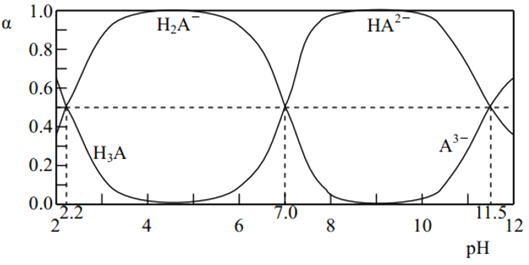
A. 根据图,可得 Ka1(H3A )≈10-7
B. 将等物质的量的 NaH2A 和 Na2HA 混合物溶于水,所得的溶液中 α(H2Aˉ)=α(HA2-)
C. 以酚酞为指示剂(变色范围 pH 8.2~10.0),将 NaOH 溶液逐滴加入到 H3A 溶液中,当溶液由无色变为浅红色时停止滴加,则生成 NaH2A
D. 在上述含 A 的各种粒子的体系中,若 c(H2Aˉ)+5c(A3ˉ)+c(OHˉ)=c(H+),则溶液pH为11.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的叙述正确的是( )
A.糖类、油脂、蛋白质都是有机高分子化合物
B.乙醇可以和金属钠反应很缓慢地放出氢气,说明乙醇的酸性很弱
C.有机物![]() 可以发生消去反应和催化氧化
可以发生消去反应和催化氧化
D.福尔马林可用作食品防腐剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓硝酸、浓硫酸反应生成SeO2以回收Se。在回收过程中涉及如下化学反应:①SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O;②Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;③Se+4HNO3(浓)=SeO2+4NO2↑+2H2O;
下列有关叙述正确的是( )
A.氧化性由强到弱的顺序是H2SO4(浓)>SeO2>I2
B.反应①中Se是氧化产物,I2是还原产物
C.反应①中生成0.6molI2,转移的电子数目为2.4NA
D.反应②③中等量的Se消耗浓硫酸和浓硝酸中溶质的物质的量之比为2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com