
【题目】图为常温下![]() 溶液逐滴加入到
溶液逐滴加入到![]() 溶液中pH的变化曲线,下列说法 不正确的是
溶液中pH的变化曲线,下列说法 不正确的是

A.在![]() 区间内某点,两溶液恰好完全反应
区间内某点,两溶液恰好完全反应
B.反应过程中溶液中阴、阳离子总数:b点小于c点
C.![]() 区间内
区间内![]() 不包含a、c两点
不包含a、c两点![]() 可能存在:
可能存在:![]()
D.d点时溶液中:![]()
【答案】A
【解析】
A. c点溶液的pH=7,若两溶液恰好完全反应生成醋酸钠,溶液呈碱性,则要想使pH=7,醋酸要过量,则C点时两溶液已经完全反应且醋酸过量,在![]() 区间内某点,两溶液恰好完全反应,故A错误;
区间内某点,两溶液恰好完全反应,故A错误;
B.氢氧化钠是强电解质,溶液中钠离子数目不变,c点为中性,b点为碱性,加入的醋酸越多,溶液中阴阳离子数目越多,则反应过程中溶液中阴、阳离子总数:b点小于c点,故B正确;
C. a点溶质为氢氧化钠,加入醋酸,氢氧化钠的量大于醋酸的量,且溶液呈碱性,则![]() 区间内
区间内![]() 不包含a、c两点
不包含a、c两点![]() 可能存在:
可能存在:![]() ,故 C正确;
,故 C正确;
D. d点加入25mL0.2000molL1CH3COOH溶液时,反应后溶质为0.0500mol/L的醋酸和醋酸钠;则根据电荷守恒和物料守恒:![]()
![]() ,故D正确;
,故D正确;
答案选A。


 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】以乙炔为主要原料可以合成聚氯乙烯、聚丙烯腈和氯丁橡胶,有关合成路线图如下:
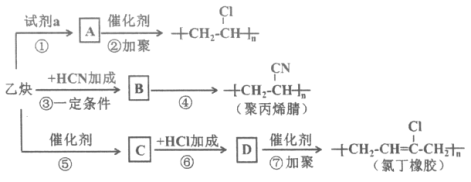
已知: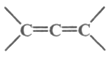 不稳定
不稳定
(1)乙炔中官能团的名称是__________。
(2)试剂a是__________。
(3)写出物质B的结构简式__________。
(4)④的反应类型是__________。
(5)写出下列反应的化学方程式:反应⑤_______;反应⑦_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D四种短周期元素,它们的核电荷数依次增大,A与C原子的基态电子排布中L能层都有两个未成对电子,C、D同主族,E、F都是第四周期元素,E原子的基态电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)基态D原子中,电子占据的最高能层符号 ______ ,该能层具有的原子轨道数为 ______。
(2)E2+离子的价层电子排布图是 ______ ,F原子的电子排布式是 ______ 。
(3)A元素的最高价氧化物对应的水化物中心原子采取的轨道杂化方式为 ______ ,B元素的气态氢化物的VSEPR模型为 ______ 。
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,它们结构相似,DAB-的电子式为 ______ 。
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6,甲的水溶液可以用于实验室中E2+离子的定性检验,检验E2+离子的离子方程式为 ______ 。
(6)某种化合物由D,E,F三种元素组成,其晶胞如图所示,则其化学式为 ______,该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度d= ______ g/cm3(列出计算式,无需计算)。
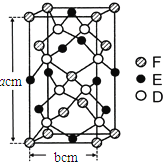
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,![]() 和
和![]() 的电离常数分别为
的电离常数分别为![]() 和
和![]() 。将
。将![]() 和体积均相同的两种酸溶液分别稀释,其
和体积均相同的两种酸溶液分别稀释,其![]() 随加水体积的变化如图所示。下列叙述正确的是( )
随加水体积的变化如图所示。下列叙述正确的是( )

A. 曲线Ⅰ代表![]() 溶液
溶液
B. 溶液中水的电离程度:b点>c点
C. 从c点到d点,溶液中 保持不变(其中
保持不变(其中![]() 、
、![]() 分别代表相应的酸和酸根离子)
分别代表相应的酸和酸根离子)
D. 相同体积a点的两溶液分别与![]() 恰好中和后,溶液中
恰好中和后,溶液中![]() 相同
相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是
A.标准状况下,22.4 L H2O含有的分子数为NA
B.常温常压下,1.06 g Na2CO3含有的Na+离子数为0.02NA
C.通常状况下,NA个CO2分子占有的体积为22.4 L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置中有机物样品在电炉中充分燃烧,通过测定生成的CO2和H2O的质量来确定有机物组成。
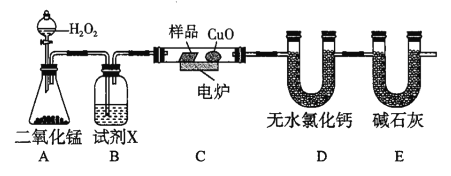
请回答下列问题:
(1)A装置是提供实验所需的O2,写出有关反应的化学方程式__________;B装置中试剂X可选用_________。
(2)若准确称取0.44g样品(只含C、H、O三种元素中的两种或三种),充分反应后,D管质量增加0.36g,E管质量增加0.88g,则该有机物的实验式为________。
(3)要确定该有机物的分子式,还需知道该有机物的_____________,经测定其蒸气密度是相同条件下H2的22倍,则其分子式为___________。
(4)若该有机物的核磁共振氢谱如图所示,则其结构简式为_____________;
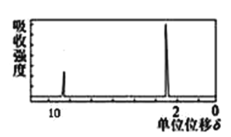
若该有机物只有一种化学环境的氢原子,则其结构简式为___________。
(5)某同学认为E和空气相通,会影响测定结果准确性,应在E后再增加一个E装置,其主要目的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物与悬浮在大气中海盐粒子的相互反应:4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+ Cl2(g),ΔH。在恒温条件下,向2 L恒容密闭容器中加入0.4mol NO2和0.2 mol NaCl,10 min反应达到平衡时n(NaNO3)= 0.1mol,NO2的转化率为α。下列叙述中正确的是
2NaNO3(s)+2NO(g)+ Cl2(g),ΔH。在恒温条件下,向2 L恒容密闭容器中加入0.4mol NO2和0.2 mol NaCl,10 min反应达到平衡时n(NaNO3)= 0.1mol,NO2的转化率为α。下列叙述中正确的是
A.10min内NO浓度变化表示的速率v(NO)=0.01 mol·L-1·min-1
B.若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于α
C.若升高温度,平衡逆向移动,则该反应的ΔH>0
D.若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述正确的是( )
A.铁屑、溴水、苯混合加热就能制取溴苯
B.用苯、浓硫酸、浓硝酸制取硝基苯时,温度越高反应越快,得到的硝基苯越多
C.乙醇与乙酸混合加热即能发生酯化反应生成有香味的酯
D.![]() 过程中反应①、②分别是取代反应、加成反应
过程中反应①、②分别是取代反应、加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液滴入某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如图所示[已知:![]() ]。下列叙述不正确的是
]。下列叙述不正确的是

A. Ka(HA)的数量级为10-5
B. 滴加NaOH溶液的过程中,![]() 保持不变
保持不变
C. m点所示溶液中:c(H+)+c(Na+)=c(HA)+c(OH-)
D. n点所示溶液中:c(Na+)=c(A-)+c(HA)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com