
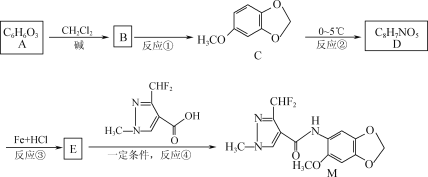
【题目】据报道,化合物M对番茄灰霉菌有较好的抑菌活性,其合成路线如下图所示。
已知:
![]()
回答下列问题:
(1)化合物C中的含氧官能团为____________,反应④的反应类型为____________。
(2)写出E的结构简式:________________________。
(3)写出反应②的化学方程式:_____________________________________________。
(4)写出化合物C满足下列条件的一种同分异构体的结构简式:_________________。
① 含苯环结构,能在碱性条件下发生水解;
② 能与FeCl3发生显色反应;
③ 分子中含有4种不同化学环境的氢。
(5)已知CH3CH2CN![]() CH3CH2COOH。请以
CH3CH2COOH。请以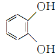 、CH2==CHCN和乙醇为原料合成化合物
、CH2==CHCN和乙醇为原料合成化合物 ![]() ,写出制备的合成路线流程图(无机试剂任用)_____。
,写出制备的合成路线流程图(无机试剂任用)_____。
【答案】醚键 取代反应 ![]()
![]()
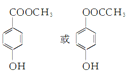
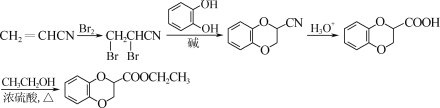
【解析】
由框图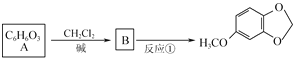 知A为
知A为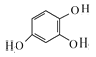 ,
,
由C的结构简式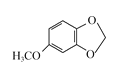 知含氧官能团为“一O-”为醚键;E+
知含氧官能团为“一O-”为醚键;E+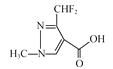
![]() M,M中生成了肽键,则为取代反应。(2)由M逆推,知E的结构筒式为
M,M中生成了肽键,则为取代反应。(2)由M逆推,知E的结构筒式为![]() 。逆推D的结构筒式为
。逆推D的结构筒式为![]() ,C与D比较知,D比C比了“一NO2",则应为C发生硝化反应所得。(4)碱性条件能水解,则含有酯基,与FeCl3能发生显色反应,则说明含有酚羟基,且酚羟基与酯基互为对位关系。
,C与D比较知,D比C比了“一NO2",则应为C发生硝化反应所得。(4)碱性条件能水解,则含有酯基,与FeCl3能发生显色反应,则说明含有酚羟基,且酚羟基与酯基互为对位关系。
(5)由合成产物逆推,产物可以由![]() 与乙醇酯化得到,羧基可以由“-CN”水解获得,
与乙醇酯化得到,羧基可以由“-CN”水解获得,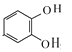 和CH2=CHCN相连,可以先将CH2=CHCN与Br2发生加成反应生成卤代物,再发生类似于流程中A-→B的反应.
和CH2=CHCN相连,可以先将CH2=CHCN与Br2发生加成反应生成卤代物,再发生类似于流程中A-→B的反应.
(1)由C的结构简式 知化合物C中的含氧官能团为醚键,反应④为
知化合物C中的含氧官能团为醚键,反应④为![]() +
+
![]()
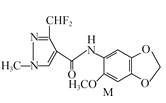 ,其反应类型为取代反应。答案:醚键 ;取代反应。
,其反应类型为取代反应。答案:醚键 ;取代反应。
(2)根据分析知E的结构简式为:![]() ;答案:
;答案:![]() 。
。
(3)反应②是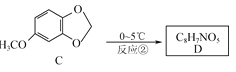 的反应。其化学方程式:
的反应。其化学方程式:![]() ;答案:
;答案:![]() 。
。
(4)①碱性条件能水解,则含有酯基,与FeCl3能发生显色反应,则说明含有酚羟基,③ 分子中含有4种不同化学环境的氢,酚羟基与酯基互为对位关系。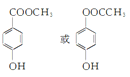 ;答案:
;答案: 。
。
(5)已知CH3CH2CN![]() CH3CH2COOH。以
CH3CH2COOH。以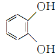 、CH2==CHCN和乙醇为原料合成化合物
、CH2==CHCN和乙醇为原料合成化合物 ![]() 的合成路线流程图为:
的合成路线流程图为: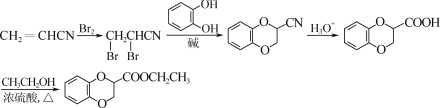 。
。


科目:高中化学 来源: 题型:
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高综合效益,而且还能防止环境污染,生产流程如下:

已知石油列解已成为生产H的重要方法,E的溶液能发生银镜反应,G是具有香味的液体,试填空。
(1)A的名称______;G的名称______。
(2)B的结构简式_______;H的结构简式____________。
(3)写出H发生加聚反应的方程式:_____________。
(4)D→E的化学方程式:_____________。
(5)E→F的化学方程式:_____________。
(6)F→G的化学方程式:_____________。
(7)写出G的同分异构体中与CH3COOH互为同系物的结构简式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表达式正确的是( )
A. 0.5mol 稀 H2 SO 4与0.5mol 稀 Ba (OH )2溶液反应放出akJ热量,则中和热为 akJ/ mol
B. 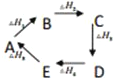 则热量变化关系式: △H1+△H3+△H5=-(△H2+△H4)
则热量变化关系式: △H1+△H3+△H5=-(△H2+△H4)
C. △H与反应方程式中的化学计量数,物质的状态和可逆反应均有关
D. 同温同压下, H2( g)+ Cl 2(g)= 2HCl (g)在光照和点燃条件下的△H不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CO(g)+O2(g)=2CO2(g) △H=﹣566kJ/mol
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=﹣452kJ/mol

根据以上热化学方程式,下列判断不正确的是( )
A. 上图可表示由CO生成CO2的反应过程和能量关系
B. CO的燃烧热为283kJ/mol
C. 2 Na2O2(s)+2 CO2(s)=2 Na2CO3(s)+O2(g)△H>﹣452kJ/mol
D. CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的储存及处理方法错误的是
A.常温时液氯用钢瓶储存B.未用完的钠、钾放回原试剂瓶
C.尾气中氯气用烧碱溶液吸收D.氧化性和还原性废弃物混合后直接排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有如图所示的铜-锌原电池,其电解质溶液为硫酸铜溶液。下列关于该电池的说法错误的是
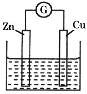
A. 锌电极为负极,发生氧化反应
B. 电子从锌电极经过硫酸铜溶液流向铜电极
C. 铜电极上发生的反应为Cu2++2e-=Cu
D. 电解质溶液中的SO42-向锌电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差l;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法不正确的是( )
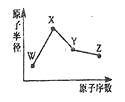
A. 对应简单离子半径:W>X
B. 对应气态氢化物的稳定性:Y<Z
C. 化合物XZW既含离子键,又含极性共价键
D. Z的氢化物和X的最高价氧化物对应水化物的溶液均能与Y的氧化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t ℃时,将一定量的混合气体在密闭容器中发生反应:aA(g)+bB(g) ![]() cC(g)+dD(g),平衡后测得B气体的浓度为0.6 mol·L-1。恒温下,将密闭容器的容积扩大1倍,重新达到平衡后,测得B气体的浓度为0.4 mol·L-1。下列叙述中正确的是
cC(g)+dD(g),平衡后测得B气体的浓度为0.6 mol·L-1。恒温下,将密闭容器的容积扩大1倍,重新达到平衡后,测得B气体的浓度为0.4 mol·L-1。下列叙述中正确的是
A. 重新达到平衡时,D的体积分数减小 B. a+b<c+d
C. 重新达到平衡时,A气体的浓度增大 D. 平衡向右移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com