
【题目】有如图所示的铜-锌原电池,其电解质溶液为硫酸铜溶液。下列关于该电池的说法错误的是
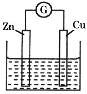
A. 锌电极为负极,发生氧化反应
B. 电子从锌电极经过硫酸铜溶液流向铜电极
C. 铜电极上发生的反应为Cu2++2e-=Cu
D. 电解质溶液中的SO42-向锌电极移动
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】某工厂,在山坡坑道的仓库里贮有氯气钢瓶。一天一只贮有氯气的钢瓶损坏,造成氯气泄漏,在场工人采取的措施正确的是
A.把钢瓶推到坡下的小河里B.把钢瓶扔到农田中
C.把钢瓶丢到深坑里,用石灰填埋D.钢瓶处理后,工人应转移到坡上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关燃烧热、中和反应反应热的叙述正确的是 ( )
①S(s)+3/2O2(g)===SO3(g) ΔH=-315 kJ·mol-1(燃烧热)(ΔH的数值正确)
②NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1(中和反应反应热)(ΔH的数值正确)
③已知CH3OH(l)的燃烧热为238.6 kJ·mol-1,则CH3OH(l)+![]() O2(g)===CO2(g)+2H2O(g) ΔH=-238.6 kJ·mol-1
O2(g)===CO2(g)+2H2O(g) ΔH=-238.6 kJ·mol-1
④燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+![]() O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1
O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1
⑤已知稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,则稀醋酸与稀氢氧化钠溶液反应生成1 mol水时放出57.3 kJ的热量
⑥葡萄糖的燃烧热是2 800 kJ·mol-1,
则1/2C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l) ΔH=-1 400 kJ·mol-1
A. ①② B. ②⑥ C. ②④ D. ④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法错误的是
A.Na2CO3用于制胃酸中和剂B.FeSO4用于制补铁剂
C.硬铝合金用于制造飞机和宇宙飞船D.14C用于测定文物年代
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,化合物M对番茄灰霉菌有较好的抑菌活性,其合成路线如下图所示。
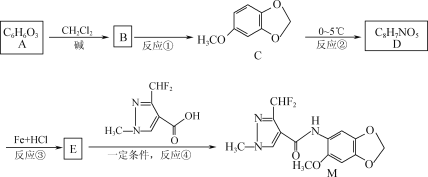
已知:
![]()
回答下列问题:
(1)化合物C中的含氧官能团为____________,反应④的反应类型为____________。
(2)写出E的结构简式:________________________。
(3)写出反应②的化学方程式:_____________________________________________。
(4)写出化合物C满足下列条件的一种同分异构体的结构简式:_________________。
① 含苯环结构,能在碱性条件下发生水解;
② 能与FeCl3发生显色反应;
③ 分子中含有4种不同化学环境的氢。
(5)已知CH3CH2CN![]() CH3CH2COOH。请以
CH3CH2COOH。请以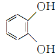 、CH2==CHCN和乙醇为原料合成化合物
、CH2==CHCN和乙醇为原料合成化合物 ![]() ,写出制备的合成路线流程图(无机试剂任用)_____。
,写出制备的合成路线流程图(无机试剂任用)_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废气中的SO2经如图中的两个循环可分别得到S和H2SO4。下列说法正确的是
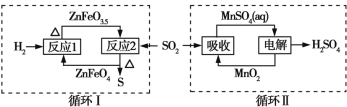
A. 循环Ⅰ中,反应1中的氧化产物为ZnFeO3.5
B. 循环Ⅰ中,反应2中的还原产物为ZnFeO4
C. Mn可作为循环Ⅱ中电解过程中的阳极材料
D. 循环Ⅰ和循环Ⅱ中消耗同质量的SO2,理论上得到S和H2SO4的质量之比为16∶49
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铁铵aFe2(SO4) 3·b(NH4) 2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。
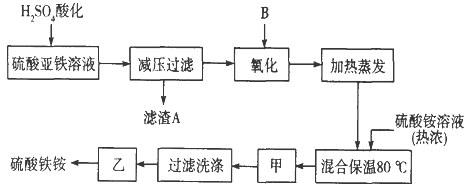
请回答下列问题:
(1)滤渣A的主要成分是__________________。
(2)下列物质中最适合的氧化剂B是________;反应的离子方程式__________________。
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲、乙的名称分别是:甲______________,乙___________________。
(4)上述流程中,氧化之后和加热蒸发之前,需取少量溶液检验Fe2+是否已全部被氧化,所加试剂能否用酸性的KMnO4溶液?____(填“能”或“不能”)理由是: ________________________。(可用语言或方程式说明)
(5)检验硫酸铁铵中NH4+的方法是________________________________________。
(6)称取14.00 g样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入0.05 mol Ba (NO3) 2溶液,恰好完全反应。则该硫酸铁铵的化学式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将15.2 g 铜和镁组成的混合物加入250 mL4.0 mol L-1的稀硝酸中,固体完全溶解,生成的气体只有NO。向所得溶液中加入1.0 L NaOH溶液,此时金属离子恰好沉淀完全,沉淀质量为25.4 g,下列说法不正确的是
A. 原固体混合物中,Cu和Mg的物质的量之比为2:1
B. 氢氧化钠溶液的浓度为0.8 mol·L-1
C. 固体溶解后的溶液中硝酸的物质的量为0.1mol
D. 生成的NO气体在标况下的体积为4.48L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列制备符合工业生产实际的是
A. 用电解熔融氯化镁制单质镁
B. 用电解熔融氯化铝制单质铝
C. 用电解饱和食盐水制氯气
D. 用二氧化硅与焦炭在高温下反应制得高纯度的硅
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com