
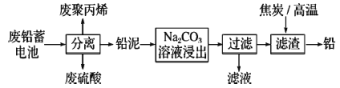
【题目】废铅蓄电池的一种回收利用工艺流程如图所示:
部分难溶电解质的性质如下表:

请回答下列问题:
(1)铅蓄电池在生产、生活中使用广泛,铅蓄电池的缺点有___(写一条)。
(2)利用废铅蓄电池中的废硫酸与氟磷灰石[Ca5(PO4)3F]反应,可以制化肥-过磷酸钙[有效成分是Ca(H2PO4)2],写出该反应的化学方程式:___。
(3)Na2CO3溶液浸出时发生的反应为CO32-(aq)十PbSO4(s)![]() PbCO3(s)+SO42-(aq),计算该反应的平衡常数K=___。以滤渣PbCO3和焦炭为原料可制备金属铅,用化学方程式表示制备过程:___。
PbCO3(s)+SO42-(aq),计算该反应的平衡常数K=___。以滤渣PbCO3和焦炭为原料可制备金属铅,用化学方程式表示制备过程:___。
(4)利用铅泥中PbSO4制取PbO2的方法:PbSO4溶于CH3COONa溶液生成弱电解质(CH3COO)2Pb,(CH3COO)2Pb与KClO在强碱性条件下反应制取PbO2,写出生成PbO2的离子方程式:___。
(5)已知Pb(OH)2是既能溶于稀硝酸又能溶于KOH溶液的两性氢氧化物。设计实验区别PbCrO4和BaCrO4:___。
【答案】比能量低(或笨重或废弃电池污染环境等) 2Ca5(PO4)3F+7H2SO4=7CaSO4+3Ca(H2PO4)2+2HF 1.2×105 PbCO3![]() PbO+CO2↑、2PbO+C
PbO+CO2↑、2PbO+C![]() 2Pb+CO2↑ (CH3COO)2Pb+ClO+2OH=PbO2↓+Cl+2CH3COO+H2O 取少量待测物于两支试管中,分别向两支盛有黄色沉淀的试管中加入过量KOH溶液,振荡,沉淀溶解的是PbCrO4,沉淀不溶解的是BaCrO4
2Pb+CO2↑ (CH3COO)2Pb+ClO+2OH=PbO2↓+Cl+2CH3COO+H2O 取少量待测物于两支试管中,分别向两支盛有黄色沉淀的试管中加入过量KOH溶液,振荡,沉淀溶解的是PbCrO4,沉淀不溶解的是BaCrO4
【解析】
废铅蓄电池经分离得到铅泥,加入碳酸钠溶液可生成碳酸铅,过滤后加入碳高温可生成铅;
(1)铅蓄电池较为笨重,且可引起重金属污染;
(2)结合反应原理及原子守恒写出生成过磷酸钙的化学方程式;
(3)写出反应CO32-(aq)+PbSO4(s)PbCO3(s)+SO42-(aq)的平衡常数表达式,结合Ksp(PbSO4)、Ksp(PbCO3)计算K的值;类比PbCO3和CaCO3的化学性质,写出制备Pb的化学方程式;
(4)根据题给信息推测(CH3COO)2Pb的性质,结合守恒规律写出(CH3COO)2Pb与KClO反应的离子方程式;
(5)结合两性氢氧化物的性质及表中Ksp的数值,设计合理实验方案。
废铅蓄电池经分离得到铅泥,加入碳酸钠溶液可生成碳酸铅,过滤后加入碳高温可生成铅;
(1)铅蓄电池较为笨重,且可引起重金属污染,比能量低;
(2)利用废铅蓄电池中的废硫酸与氟磷灰石[Ca5(PO4)3F]反应,可以制化肥过磷酸钙[有效成分是Ca(H2PO4)2],该反应的化学方程式为:2Ca5(PO4)3F+7H2SO4=7CaSO4+3Ca(H2PO4)2+2HF;
(3)反应CO32-(aq)+PbSO4(s)PbCO3(s)+SO42-(aq)的平衡常数K= =
= ×
×![]() =
=![]() =1.2×105,以滤渣PbCO3和焦炭为原料可制备金属铅,涉及反应为PbCO3
=1.2×105,以滤渣PbCO3和焦炭为原料可制备金属铅,涉及反应为PbCO3![]() PbO+CO2↑、2PbO+C
PbO+CO2↑、2PbO+C![]() 2Pb+CO2↑;
2Pb+CO2↑;
(4)(CH3COO)2Pb溶液与KClO在强碱性条件下反应制取PbO2,同时生成氯离子、CH3COO,反应的离子方程式为:(CH3COO)2Pb+ClO+2OH=PbO2↓+Cl+2CH3COO+H2O;
(5)Pb(OH)2是既能溶于稀硝酸,又能溶于KOH溶液的两性氢氧化物,则可加入过量KOH溶液鉴别,能溶解的为PbCrO4,操作方法为:取少量待测物于两支试管中,分别向两支盛有黄色沉淀的试管中加入过量KOH溶液,振荡,沉淀溶解的是PbCrO4,沉淀不溶解的是BaCrO4。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】根据系统命名法,天然橡胶应称为聚![]() 甲基
甲基![]() ,
,![]() 丁二烯,其结构简式为
丁二烯,其结构简式为![]() ,单体为
,单体为![]() 甲基
甲基![]() ,
,![]() 丁二烯。该反应的化学方程式为
丁二烯。该反应的化学方程式为![]() 。合成橡胶就是根据以上原理制成的。
。合成橡胶就是根据以上原理制成的。
(1)以![]() 为单体可生成氯丁橡胶,试写出该反应的化学方程式:_________________。
为单体可生成氯丁橡胶,试写出该反应的化学方程式:_________________。
(2)丁腈橡胶的结构简式为![]() ,形成该橡胶的单体为________。
,形成该橡胶的单体为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种![]() 工程树脂由丙烯腈(
工程树脂由丙烯腈(![]() ,用
,用![]() 表示)、1,
表示)、1,![]() 丁二烯(
丁二烯(![]() ,用
,用![]() 表示)和苯乙烯(
表示)和苯乙烯(![]() ,用
,用![]() 表示)按一定比例共聚而得。
表示)按一定比例共聚而得。
(1)![]() 和
和![]() 三种单体中,
三种单体中,![]() 原子个数比的比值最小的单体是___________(填物质名称)。
原子个数比的比值最小的单体是___________(填物质名称)。
(2)经元素分析可知,该![]() 工程树脂的组成为
工程树脂的组成为![]() (
(![]() 为正整数),则原料中
为正整数),则原料中![]() 和
和![]() 的物质的量之比是____________(用
的物质的量之比是____________(用![]() 表示)。
表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气作为清洁能源有着广泛的应用前景,采用天然气制备氢气的流程如下。
![]()
请回答下列问题:
Ⅰ.蒸汽转化:在催化剂的作用下,水蒸气将CH4氧化,结合图表信息回答问题。
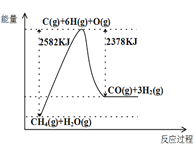
(1)该过程的热化学方程式是__________。
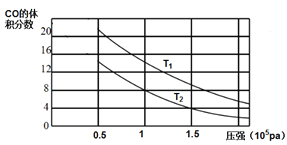
(2)平衡混合物中CO的体积分数与压强的关系如图所示,判断T1和T2的大小关系:T1_______T2(填“>”“<”或“=”),并说明理由__________。
(3)一定温度下,在1L恒容的密闭容器中充入1mol CH4和1mol水蒸气充分反应达平衡后,测得反应前后容器中气体的物质的量之比是3:4,计算该条件下反应的平衡常数为______________。
Ⅱ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅲ.模拟H2提纯工艺:将CO2和H2分离得到H2的过程如下:
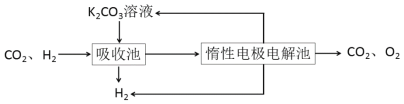
依据图示信息回答:
(4)吸收池中发生反应的离子方程式是_________。
(5)写出电解池中阳极发生的电极反应式________;结合化学用语说明K2CO3溶液再生的原因_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中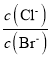 增大
增大
B.在0.1 mol/LCH3COONa溶液中:c(OH﹣)+0.1mol/L>c(CH3COOH)+c(H+)+c(Na+)
C.在10mL 0.1 mol/L的AgNO3溶液中加入6mL等浓度的NaCl溶液,有白色沉淀产生,再加入6 mL等浓度的Na2S溶液,溶液中又有黑色沉淀生成,说明Ksp(Ag2S)< Ksp(AgCl)
D.常温下,10 mL 0.02 mol/L HCl溶液与10 mL 0.02 mol/LBa(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通电解精炼铜的方法所制备的铜中仍含杂质,利用如图中的双膜(阴离子交换膜和过滤膜)电解装置可制备高纯度的Cu。下列有关叙述正确的是( )
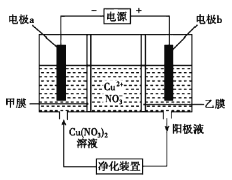
A.电极a为粗铜
B.甲膜为过滤膜,可阻止阳极泥及漂浮物杂质进入阴极区
C.乙膜为阴离子交换膜,可阻止杂质阳离子进入阴极区
D.当电路中通过1mol电子时,可生成32g精铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A. 分子式为C8H8O2的芳香族化合物中属于羧酸的同分异构体有3种
B. 麦芽糖的水解产物有两种,且互为同分异构体
C. 等质量的苯和苯乙烯(![]() )完全燃烧,消耗氧气的体积相同
)完全燃烧,消耗氧气的体积相同
D. 分子式为C4H8Cl2且含有两个甲基的有机物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热某纯净的小苏打(NaHCO3)样品至固体质量不再变化,得到固体(Na2CO3)质量31.8g,将该固体溶于水配制成500mL溶液,计算:
(1)产生的气体冷却至标准状况下,其体积为多少升?______________
(2)求所得溶液中Na+的物质的量浓度?_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类推的思维方法在化学学习与研究中常会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否。下列几种类推结论中,正确的是( )
A.由2Cu + O2 = 2CuO可推出同族的硫也有Cu + S = CuS
B.Fe3O4可表示为FeO·Fe2O3,则Pb3O4可表示为PbO·Pb2O3
C.Mg能在CO2中燃烧,所以Na也能在CO2中燃烧
D.CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应只生成Na2SO3和O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com