
【题目】对于三种气态烃甲烷、乙烷、乙烯,请回答下列问题:
(1)等质量的三种烃在相同状况下体积最大的是________。
(2)等质量的三种烃完全燃烧时消耗氧气最多的是________。
(3)等质量的三种烃完全燃烧生成二氧化碳最多的是________,生成水最多的是________。
(4)在120 ℃、1.01×105Pa条件下,与足量的氧气混合点燃,完全燃烧前后气体体积没有变化的烃是________。
【答案】 CH4 CH4 C2H4 CH4 CH4、C2H4
【解析】(1)CH4、C2H6、C2H4的相对分子质量大小为:CH4<C2H4<C2H6,根据n=![]() ,V=nVm可知,相同条件下,质量相同时,气体的相对分子质量越小,气体所占体积越大,故质量相同时,在相同状况下体积最大的是CH4;(2)CH4、C2H6、C2H4的H%大小为:CH4>C2H6>C2H4,质量相同时,分子中H元素的质量分数越大,完全燃烧时消耗O2越多,故完全燃烧时消耗O2的量最多的是CH4;(3)CH4、C2H6、C2H4的C%大小为:CH4<C2H6<C2H4,质量相同时,分子中C元素的质量分数越大,完全燃烧时生成的CO2越多,故完全燃烧生成的CO2最多的是C2H4;CH4、C2H6、C2H4的H%大小为:CH4>C2H6>C2H4,质量相同时,分子中H元素的质量分数越大,完全燃烧时生成H2O越多,故生成水最多的是CH4;(3)120℃条件下水为气体,燃烧通式CxHy+(x+
,V=nVm可知,相同条件下,质量相同时,气体的相对分子质量越小,气体所占体积越大,故质量相同时,在相同状况下体积最大的是CH4;(2)CH4、C2H6、C2H4的H%大小为:CH4>C2H6>C2H4,质量相同时,分子中H元素的质量分数越大,完全燃烧时消耗O2越多,故完全燃烧时消耗O2的量最多的是CH4;(3)CH4、C2H6、C2H4的C%大小为:CH4<C2H6<C2H4,质量相同时,分子中C元素的质量分数越大,完全燃烧时生成的CO2越多,故完全燃烧生成的CO2最多的是C2H4;CH4、C2H6、C2H4的H%大小为:CH4>C2H6>C2H4,质量相同时,分子中H元素的质量分数越大,完全燃烧时生成H2O越多,故生成水最多的是CH4;(3)120℃条件下水为气体,燃烧通式CxHy+(x+![]() )O2
)O2![]() xCO2+
xCO2+![]() H2O(g),完全燃烧前后气体体积没有变化,则1+(x+
H2O(g),完全燃烧前后气体体积没有变化,则1+(x+![]() )=x+
)=x+![]() ,故y=4,即CH4、C2H4完全燃烧后体积不变。
,故y=4,即CH4、C2H4完全燃烧后体积不变。


科目:高中化学 来源: 题型:
【题目】野外被蚊虫叮咬会出现红肿,这是由甲酸(HCOOH)造成的。请完成下列探究。
I . HCOOH 酸性探究
(1)下列酸属于二元酸的有___________。
a.HCOOH b.H2CO3 c.H2C2O4 d.CH3CHOHCH2COOH
(2)下列实验事实能证明甲酸为弱酸的是___________。
a.HCOONH4溶液呈酸性
b.将甲酸滴入![]() 溶液中有气体生成
溶液中有气体生成
C.常温下,0.1mol·L-1的甲酸溶液的pH约为3
d.等浓度的盐酸与甲酸溶液。前者的导电能力更强
(3)可用小苏打溶液处理蚊虫叮咬造成的红肿,请用离子方程式表示其原理_________。
Ⅱ甲酸制备甲酸铜探究
相关原理和化学方程式如下:
先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,然后碱式碳酸铜再与甲酸反应制得四水甲酸铜![]() 晶体:
晶体:
![]()
![]()
实验步骤如下:
(4)碱式碳酸铜的制备:
![]()
①步骤ⅰ是将一定量![]() 晶体和
晶体和![]() 固体一起放到研钵中研细并混合均匀。
固体一起放到研钵中研细并混合均匀。
②步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃-80℃,温度不能过高的原因是________________________________。
③步骤ⅱ的后续操作有过滤、洗涤等。检验沉淀是否已洗涤干净的方法为________。
(5)甲酸铜晶体的制备:
将Cu(OH)2CuCO3固体放入烧杯中,加入一定量的热蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质。在通风橱中蒸发滤液至原体积的三分之一时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体 2~3 次,晾干,得到产品。
①“趁热过滤”中,必须“趁热”的原因是_________________。
②用乙醇洗涤晶体的目的是________________________________。
③若该实验所取原料 CuSO45H2O 晶体和 NaHCO3 固体的质量分别为12.5 g 和9.5 g,实验结 束后,最终称量所得的产品为 7.91 g,则产率为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系

据此判断下列说法中正确的是( )
A. 石墨转变为金刚石是吸热反应
B. 白磷比红磷稳定
C. ①S(g)+O2(g)=SO2(g);②S(s)+O2(g)=SO2(g);放出热量:①②
D. CO(g)+H2O(g)=CO2(g)+ H2 (g);该反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是周期表中的一部分,根据A-I在周期表中的位置,第(2) ~ (3)小题用元素符号或化学式回答,(4)~(6)小题按题目要求回答。
族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | O |
1 | A | |||||||
2 | D | E | G | |||||
3 | B | C | F | H | I |
(1)表中元素,化学性质最不活泼的原子结构示意图是___________,非金属性最强的元素在周期表中的位置是__________________________,
(2)最高价氧化物的水化物中碱性最强的是_________,酸性最强的是___________,
(3)A分别与D、E、G形成的最简单化合物中,最不稳定的_______________,
(4)A和E组成最简单化合物的电子______________
(5)在B、C、F、G的简单离子中,离子半径由大到小的顺序是__________________,
(6)由A的单质与O2构成的燃料电池中,在E的最高价氧化物对应水化物的条件下进行,写出正极的电极反应式______________________________________。
(7)当B的最高价氧化物的水化物与C的最高价氧化物反应后,向所得溶液中通入过量D的最高价氧化物的离子方程式___________________________________,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用Fe2(SO4)3酸性溶液处理SO2废气的工艺流程如下,下列说法不正确的是)

A.溶液的pH:①>②>③
B.整个过程中Fe2(SO4)3溶液可以循环利用
C.溶液②转化为溶液③发生反应的离子方程式为4H++4Fe2++O2=4Fe3++2H2O
D.向②溶液中滴加KSCN溶液,溶液可能变为血红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取a g样品,向其中加入足量的氢氧化钠溶液,测得生成的气体为b L(标况)。反应的离子方程式为_______________,样品中铝的物质的量为_____________(用含b的代数式表示)。
(2)若取a g样品,在高温下能恰好完全反应,该反应的化学方程式为________________,样品中氧化铁与铝的质量比为_________________(用含a 、b的代数式表示)。
(3)待(2)中反应产物冷却后,往其中加入足量的盐酸,测得生成的气体体积为c L(标况),则该气体与(1)中所得的气体的体积比c∶b=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用质量分数为98%的浓硫酸(ρ=1.84 g·cm-3)配制240 mL 1.84 mol·L-1稀硫酸,下列操作正确的是( )
A. 将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B. 必需的定量仪器有100 mL量筒、250 mL容量瓶和托盘天平
C. 量取浓硫酸的体积为25.0 mL
D. 先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲用98%的浓H2SO4(ρ=1.84g/cm3)配制500mL 0.5molL﹣1的稀H2SO4。
(1)填写下列操作步骤:
①所需浓H2SO4的体积为______。
②如果实验室有10mL、20mL、50mL量筒,应选用______mL量筒量取。
③将量取的浓H2SO4沿内壁慢慢注入盛有约100m 水的烧杯里,并不断搅拌,目的是______。
④立即将上述溶液沿玻璃棒注入______中,并用50mL蒸馏水洗涤烧杯2~3次,并将洗涤液注入其中,并不时轻轻振荡。
⑤加水至距刻度线______处,改用______加水,使溶液的凹液面最低点正好跟刻度线相平。盖上瓶塞,上下颠倒数次,摇匀。
(2)请指出上述操作中一处明显错误______。
(3)误差请分析以下错误操作对所配制的溶液浓度的影响(填“偏高”“偏低”或“无影响”)。
①若进行操作⑤定容时,眼睛俯视,则所配制溶液的浓度将______。
②问题(2)的错误操作将导致所配制溶液的浓度______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—股淡淡清香能给人心旷神怡的感觉,主要由香精、酒精和水构成的香水备受爱美人士的青睐。香精里面含有酯类物质,工业上以A为主要原料来合成乙酸乙酯,其合成路线如下图所示,其中A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平。又知2CH3CHO+O2![]() 2CH3COOH。请回答下列问题:
2CH3COOH。请回答下列问题:
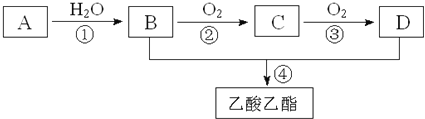
(1)写出A的电子式__________;
(2)B、D分子内含有的官能团分别是__________、__________(填名称);
(3)写出下列反应的反应类型:①______________,④______________;
(4)写出下列反应的化学方程式:
①__________________________________________________;
②__________________________________________________;
④__________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com