
【题目】蔗糖与浓硫酸反应的实验改进装置如图所示,下列说法错误的是
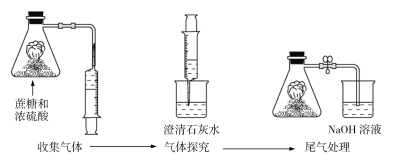
A.改进装置后,有毒气体被碱液吸收,实现了绿色环保
B.浓硫酸在实验过程中体现了脱水性和强氧化性
C.产生的气体能使澄清石灰水变浑浊,说明产生了CO2
D.该反应比较剧烈、危险,实验各物质的用量应按要求规范操作
科目:高中化学 来源: 题型:
【题目】室温下,向圆底烧瓶中加入1 molC2H5OH和含1molHBr的氢溴酸,溶液中发生反应;C2H5OH+HBr![]() C2H5Br+H2O,充分反应后达到平衡。已知常压下,C2H5Br和C2H5OH的沸点分别为38.4℃和78.5℃。下列有关叙述错误的是
C2H5Br+H2O,充分反应后达到平衡。已知常压下,C2H5Br和C2H5OH的沸点分别为38.4℃和78.5℃。下列有关叙述错误的是
A. 加入NaOH,可增大乙醇的物质的量
B. 增大HBr浓度,有利于生成C2H5Br
C. 若反应物增大至2 mol,则两种反应物平衡转化率之比不变
D. 若起始温度提高至60℃,可缩短反应达到平衡的时间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25C时,有关弱酸的电离平衡常数如下表:
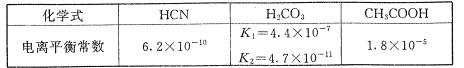
下列有关微粒浓度的说法正确的是( )
A.pH均为8的NaCN溶液、Na2CO3溶液、CH3COONa溶液:c(Na2CO3)>c(NaCN)>c(CH3COONa)
B.浓度均为0.1mol/LNaHCO3和Na2CO3混合溶液中:2c(Na+)=3c(HCO3-)+3c(CO32-)+3c(H2CO3)
C.0.2mol/LHCN溶液与0.lmol/LNaOH溶液等体积混合所得溶液中:c(HCN)>c(Na+)>c(CN-)>c(OH-)
D.浓度均为0lmol/LCH3COOH和CH3COONa混合溶液中:c(CH3COOH)+c(H+)>c(CH3COO-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是合成心脏病治疗药法西多曲的中间体,其合成路线流程图如图:
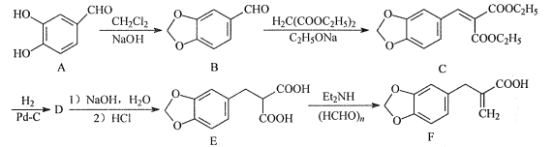
(1)C中的含氧官能团名称为___和___。
(2)A-B的反应类型为___。
(3)D的分子式为C15H18O6,写出D的结构简式:___。
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:___。
①能与FeCl3溶液发生显色反应,不能发生银镜反应;
②苯环上有4个取代基,分子中只有4种不同化学环境的氢。
(5)请写出以H2C=CH2、H2C(COOC2H5)2、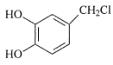 为原料制备
为原料制备 的合成路线流程图___(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图___(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为短周期原子序数依次增大的主族元素,其原子序数之和为30,W与X、Y、Z都能形成共价化合物,Y、W形成的常见化合物溶于水显碱性,Z、W形成的化合物溶于水显酸性,四种元素形成的某种化合物的结构式为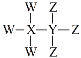 。下列说法错误的是
。下列说法错误的是
A.X为硼元素或碳元素
B.Y不属于第ⅣA族元素
C.W与Y、Z分别形成的常见化合物能反应生成盐
D.最高价氧化物对应的水化物的酸性:Z>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
氮原子可以形成 σ 键、π 键、大 π 键和配位键,成键的多样性使其形成了多种具有独特组成的物质。回答下 列问题:
(1)第一电离能:氮______氧(填“大于”或“小于”),基态氮原子价电子排布图不是![]() ,是因 为该排布方式违背了__________。
,是因 为该排布方式违背了__________。
(2)肼(H2NNH2)分子中孤电子对与 σ 键的数目之比为______,肼的相对分子质量与乙烯接近,但沸点远高于乙烯的原因是______。
( 3)硝酸的结构可表 示 为 ![]() ,硝酸与水分子可 形 成一水合二硝酸结晶 水 合物 (2HNO3 H2O) , 水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式______(氢键用“…”表示)。
,硝酸与水分子可 形 成一水合二硝酸结晶 水 合物 (2HNO3 H2O) , 水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式______(氢键用“…”表示)。
(4)正硝酸钠(Na3NO4)为白色晶体,是一种重要的化工原料。
①Na3NO4 阴离子的空间构型为______,其中心原子杂化方式为______。
②分别写出一种与 Na3NO4 的阴离子互为等电子体的阴离子和分子______(填化学式)。
③在 573 K 条件下,实验室中用 NaNO3 和 Na2O 在银皿中反应制得 Na3NO4,Na2O 的立方晶胞如图所 示。

图中“●”表示______(填“Na+”或“O2”),距离“●”最近且等距离的“○”有______个,Na2O 晶胞的参数为 a pm,则晶胞密度为_____gcm3。(列出计算式即可,NA 为阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是

A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是( )
COS(g)+H2(g) K=0.1反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是( )
A.通入CO后,正反应速率逐渐增大
B.升高温度,H2S浓度增加,表明该反应是吸热反应
C.CO的平衡转化率为80%
D.反应前H2S物质的量为7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多硫化钠Na2Sx(x≥2)在结构上与Na2O2、FeS2等有相似之处。Na2Sx在碱性溶液中与NaClO反应可生成Na2SO4,下列说法错误的是
A.NaClO是氧化剂
B.Na2SO4是氧化产物
C.若反应中Na2Sx与NaClO的物质的量之比为1:13,则x为5
D.若x=3,则反应的离子方程式为:S32-+10ClO-+4OH-=3SO42-+10Cl-+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com