
【题目】雾霾天气是一种大气污染状态,是对大气中各种悬浮颗粒物含量超标的笼统表述,尤其是PM2.5(空气动力学当量直径小于等于2.5微米的颗粒物)被认为是造成雾霾天气的“元凶”。雾霾的化学成分较为复杂,包含有下列物质,其中属于有机化合物的是( )
A. 臭氧 B. 碳氢化合物 C. 氮氧化物 D. 一氧化碳
科目:高中化学 来源: 题型:
【题目】以硅藻土为载体的五氧化二钒(V2O5)是接触法生产硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:

回答下列问题:
(1)“酸浸”时V2O5转化为VO![]() ,反应的离子方程式为______________,同时V2O4转化成VO2+。“废渣1”的主要成分是________。
,反应的离子方程式为______________,同时V2O4转化成VO2+。“废渣1”的主要成分是________。
(2)“氧化”中欲使3 mol的VO2+变为VO![]() ,则需要氧化剂KClO3至少为________mol。
,则需要氧化剂KClO3至少为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学帮助水质检测站配制490 mL 0.5 mol L-1NaOH溶液以备使用。
(1)该同学应选择_____mL的容量瓶。
(2)应用托盘天平准确称量_______g NaOH固体。
(3)配制过程如图乙所示,则图甲操作应在图乙中的______ (填字母)之间。
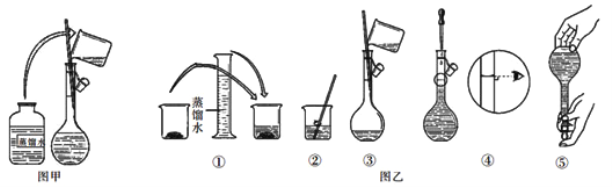
A.①与② B.②与③ C.③与④
(4)若在配制过程中出现下列情况,会使所配制NaOH溶液的浓度偏低的是______(填字母)。
A.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
B.定容时俯视
C.配制溶液所用的容量瓶洗净后没有烘干
D.NaOH固体在烧杯中溶解后,立即将溶液转移到容量瓶内,并接着进行后续操作
E.定容摇匀后,发现液面低于刻度线,再加入蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①热分解法、②热还原法、③电解法是工业上制取金属的三种常用方法。下列金属与冶炼方法相对应的是( )
A. Al、Na—③ B. Ca、Cu—② C. Fe、Mg—③ D. Al、Hg—①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空:
(1)碱金属元素原子最外层的电子都是________个,在化学反应中它们容易失去________个电子。
(2)碱金属元素中还原性最强的是________,原子半径最小的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pOH值指的是溶液的碱度,以溶液中OH-浓度来表示,与pH所表示的溶液酸度相对应,pOH等于OH-的浓度的负常用对数。下图分别表示的是在25℃和100℃下水的电离平衡曲线。下列说法中正确的是

A. 曲线B表示的是25°C时水的电离平衡曲线
B. 25°C时,向pH=1的稀硫酸中逐滴滴入pH=11的稀氨水至过量,反应过程中水的电离先促进后抑制
C. Q点对应的溶液中,可同时大量存在K+、Fe3+、NO3-、SO42-
D. 100°C时,将pH = 2的硫酸与pH=12的氧氧化钠溶液等体积混合,溶液显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去粗盐中的CaCl2、MgCl2、Na2SO4 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:
![]()
(1)判断BaCl2已过量的方法是______________。
(2)第⑥步中,相关的离子方程式是____________________。
(3)为检验精盐纯度,需配制230mL0.2mol/L NaCl(精盐)溶液,则需用托盘天平称取精盐固体的质量为_______,需要的玻璃仪器有量筒、 __________________。
(4)配制NaCl(精盐)溶液时,若出现下列操作,造成结果偏低的是__________。
A.称量时NaCl已潮解 B.天平的砝码已锈蚀
C.定容摇匀时,液面下降又加水 D.定容时仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由金属Na、Cu、C、N、B等元素组成的物质在生活和工业上有着广泛用途。
(1)基态Cu+的外围电子轨道式为_______。
(2)H3BNH3是储氢材料,其制备原理为:3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3,其中(HB=NH)3是一种六元环状化合物。化合物H3BNH3中B原子的杂化方式为_______;1个(HB=NH)3分子中含有 ___个σ键。
(3) B、C、N、O原子的第一电离能由大到小的顺序为_____________________。
(4)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为____(填字母)。
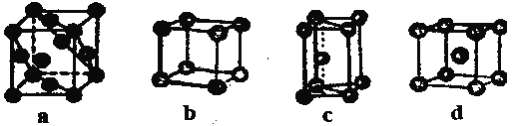
(5)已知NaCl的摩尔质量为Mg·mol-1,密度为pg·㎝-3,阿伏加德罗常数为NA mol-1,在NaCl晶体中,两个距离最近的Cl-中心间的距离为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com