
【题目】铅蓄电池的工作原理为:Pb+PbO2+2H2SO=2PbSO4+2H2O

研读右图,下列判断不正确的是
A.K闭合时,d电极反应式:PbSO4+2H2O-2e-=PbO2+4H++SO42-
B.当电路中转移0.2 mol电子时,Ⅰ中消耗的![]() 为0.2mol
为0.2mol
C.K闭合时,Ⅱ中![]() 向c电极迁移
向c电极迁移
D.K闭合一段时间后,Ⅱ可单独作为原电池,d电极为正极
【答案】C
【解析】
根据铅蓄电池的工作原理,可知左边是原电池,右边是电解池。
A.d连的是原电池的正极,所以为电解池的阳极,电极反应式:PbSO4+2H2O-2e-=PbO2+4H++SO42-,正确;
B.根据Pb+PbO2+2H2SO=2PbSO4+2H2O,转移2mol电子,则消耗2mol硫酸,所以当电路中转移0.2 mol电子时,Ⅰ中消耗的![]() 为0.2mol,正确;
为0.2mol,正确;
C.K闭合时,Ⅱ是电解池,阴离子移向阳极,d是阳极,所以![]() 向d电极迁移,错误;
向d电极迁移,错误;
D.K闭合一段时间后,Ⅱ中发生了充电反应:2PbSO4+2H2O = Pb+PbO2+2H2SO,c、d电极上的PbSO4分别转化为Pb和PbO2,所以可单独作为原电池,d电极上附着PbO2,放电时得到电子,为正极,正确;
故选C。


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】碘酸钾(![]() )是重要的微量元素碘添加剂。实验室设计下列实验流程制取并测定产品中
)是重要的微量元素碘添加剂。实验室设计下列实验流程制取并测定产品中![]() 的纯度:
的纯度:
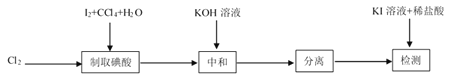
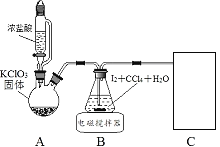
其中制取碘酸(![]() )的实验装置见图,有关物质的性质列于表中
)的实验装置见图,有关物质的性质列于表中
物质 | 性质 |
HIO3 | 白色固体,能溶于水,难溶于CCl4 |
KIO3 | ①白色固体,能溶于水,难溶于乙醇 ②碱性条件下易发生氧化反应:ClO-+IO3-=IO4-+Cl- |
回答下列问题
(1)装置A中参加反应的盐酸所表现的化学性质为______________。
(2)装置B中反应的化学方程式为___________________ 。B中所加CCl4的作用是_________从而加快反应速率。
(3)分离出B中制得的![]() 水溶液的操作为____________;中和之前,需将HIO3溶液煮沸至接近于无色,其目的是____________,避免降低
水溶液的操作为____________;中和之前,需将HIO3溶液煮沸至接近于无色,其目的是____________,避免降低![]() 的产率。
的产率。
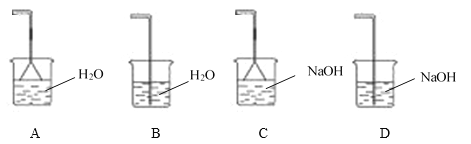
(4)为充分吸收尾气,保护环境,C处应选用最合适的实验装置是____________(填序号)。
(5)为促使![]() 晶体析出,应往中和所得的
晶体析出,应往中和所得的![]() 溶液中加入适量的___________。
溶液中加入适量的___________。
(6)取1.000g![]() 产品配成200.00mL溶液,每次精确量取20.00mL溶液置于锥形瓶中,加入足量KI溶液和稀盐酸,加入淀粉作指示剂,用0.1004mol/L
产品配成200.00mL溶液,每次精确量取20.00mL溶液置于锥形瓶中,加入足量KI溶液和稀盐酸,加入淀粉作指示剂,用0.1004mol/L![]() 溶液滴定。滴定至终点时蓝色消失(
溶液滴定。滴定至终点时蓝色消失(![]() ),测得每次平均消耗
),测得每次平均消耗![]() 溶液25.00mL。则产品中
溶液25.00mL。则产品中![]() 的质量分数为___(结果保留三位有效数字)。
的质量分数为___(结果保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1840年,Devil用干燥的氯气通过干燥的硝酸银制得了N2O5。
(1)F.DanielS等曾利用测压法在刚性反应器中研究了特定条件下N2O5(g)分解反应:
已知:2N2O5(g)=2N2O4(g)+O2(g) ΔH1=-4.4kJmol-1
2NO2(g)=N2O4(g) ΔH2=-55.3kJmol-1
则反应N2O5(g)=2NO2(g)+![]() O2(g)的ΔH=__kJmol-1。
O2(g)的ΔH=__kJmol-1。
(2)查阅资料得知N2O5是硝酸的酸酐,常温呈无色柱状结晶体,微溶于冷水,可溶于热水生成硝酸,熔点32.5℃,受热易分解,很容易潮解,有毒。在通风橱中进行模拟实验制取N2O5的装置如图:
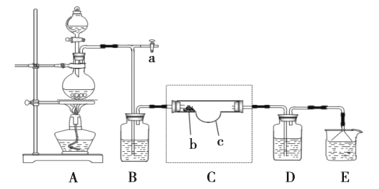
注:虚线框内为该组同学自制特殊仪器,硝酸银放置在b处。
请回答下列问题:
①实验开始前,需要打开a处活塞并鼓入空气,目的是__。
②经检验,氯气与硝酸银反应的产物之一为氧气,写出此反应的化学反应方程式__。
③实验时,装置C应保持在35℃,可用的方法是__。
④能证明实验成功制得N2O5的现象是__。
⑤装置D中的试剂是__,作用是__。
⑥装置E烧杯中的试剂为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用反应:Cu+2Fe3+=Cu2++2Fe2+设计的原电池实验装置如图。请回答下列问题:
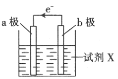
(1)b极发生___(填“氧化”或“还原”)反应,其电极材料为___,b电极反应式为:____。
(2)a极为____(填“正极”或“负极”),其电极材料可能为___,a极的电极反应式为____。
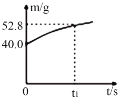
(3)该电池放电过程中,若测得电解质溶液的质量与时间的关系如图所示,则反应从开始至t1时,电路中转移电子的物质的量为_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定有机化合物中碳和氢的组成常用燃烧分析法,下图是德国化学家李比希测定有机物组成的装置,氧化铜作催化剂,在750°C左右使有机物在氧气流中全部氧化为CO2和H2O,用含有固体氢氧化钠和氯化钙的吸收管分别吸收CO2和H2O。

试回答下列问题:
(1)甲装置中盛放的是____________,甲、乙中的吸收剂能否颠倒?____________________,请说明理由:_______________________________。
(2)实验开始时,要先通入氧气一会儿,然后再加热,为什么?____________________________。
(3)将4.6 g有机物A进行实验,测得生成5.4 g H2O和8.8 g CO2,则该物质中各元素的原子个数比是________________。
(4)经测定,有机物A的核磁共振氢谱示意图如图,则A的结构简式为__________________。
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示的实验,能达到实验目的的是( )
A. 验证化学能转化为电能
验证化学能转化为电能
B. 证明温度对平衡移动的影响
证明温度对平衡移动的影响
C. 验证铁发生析氢腐蚀
验证铁发生析氢腐蚀
D. 验证AgCl溶解度大于Ag2S
验证AgCl溶解度大于Ag2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B为单质,C为化合物。能实现上述转化关系的是( )
A+B![]() C
C![]() C溶液
C溶液![]() A+B
A+B
①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液遇Na2CO3放出CO2气体,则A可能是H2
③若C溶液中滴加KSCN溶液显血红色,则B可能为Fe
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A.①②B.③④C.①③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如下,下列有关该有机物的叙述中不正确的是
![]()
A. 其分子式为 C9H10O
B. 能使酸性高锰酸钾溶液褪色
C. 一定条件下,1mol 该有机物理论上最多能与 4mol H2 发生加成反应
D. 一定条件下,1mol 该有机物理论上最多能与 4mol Br2 发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行SO2的性质实验。在点滴板a、b、c、d处分别滴有不同的试剂,再向Na2SO3固体上滴加数滴浓H2SO4后,在整个点滴板上盖上培养皿,一段时间后观察到的实验现象如表所示。下列说法正确的是( )
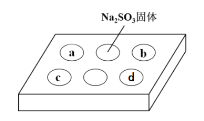
序号 | 试剂 | 实验现象 |
a | 品红溶液 | 红色褪去 |
b | 酸性KMnO4溶液 | 紫色褪去 |
c | NaOH溶液(含2滴酚酞) | 红色褪去 |
d | H2S溶液 | 黄色浑浊 |
A.在浓硫酸与Na2SO3固体反应中,浓硫酸表现的强氧化性
B.a、b均表明SO2具有漂白性
C.c中只可能发生反应:SO2+2OH-=SO32-+H2O
D.d中表明SO2具有氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com