
����Ŀ��25��ʱ���������ˮ�зֱ�����������������ʣ�����ʵ�������±���ʾ��
�������� | HCl(aq) | FeCl3 | NaOH | HCOONa | C2H5OH |
��Һ��pH | 3 | 4 | 10 | 11 | δ�ⶨ |
ˮ�ĵ���̶� | ��1 | ��2 | ��3 | ��4 | ��5 |
�������ʺ�ˮ�ĵ���̶��ɴ�С����˳����ȷ����
A����3����1����5����2����4 B����4����2����5����1����3
C����4����2����5����3����1 D����1����3����5����2����4
���𰸡�C
��������
�����������ˮ�д��ڵ���ƽ�⣺H2O ![]() H+ + OH-,����Ӽ������ˮ�ĵ��룬��������ˮ�������ٽ�ˮ�ĵ��룬������Ŀ��������pHֵ�����ݣ����Լ��������Һ����ˮ�����c(H+)����������PH =3������ˮ�����c(H+)=10-11mol/L������FeCl3ʹPH=4������ˮ�����c(H+)=10-4mol/L������NaOHʹpH=10,����ˮ�����c(H+)=10-10mol/L������HCOONaʹPH=11������ˮ�����c(H+)=10-3mol/L������C2H5OH����Ӱ��ˮ�ĵ��룬����ˮ�����c(H+)=10-7mol/L���ɴ˿�֪ˮ�ĵ���̶��ɴ�С��˳��Ϊ��4����2����5����3����1��ѡC��
H+ + OH-,����Ӽ������ˮ�ĵ��룬��������ˮ�������ٽ�ˮ�ĵ��룬������Ŀ��������pHֵ�����ݣ����Լ��������Һ����ˮ�����c(H+)����������PH =3������ˮ�����c(H+)=10-11mol/L������FeCl3ʹPH=4������ˮ�����c(H+)=10-4mol/L������NaOHʹpH=10,����ˮ�����c(H+)=10-10mol/L������HCOONaʹPH=11������ˮ�����c(H+)=10-3mol/L������C2H5OH����Ӱ��ˮ�ĵ��룬����ˮ�����c(H+)=10-7mol/L���ɴ˿�֪ˮ�ĵ���̶��ɴ�С��˳��Ϊ��4����2����5����3����1��ѡC��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A. �����£�C(s)��H2O(g)![]() CO(g)��H2(g) �����Է����У���÷�Ӧ����H��0
CO(g)��H2(g) �����Է����У���÷�Ӧ����H��0
B. ��pH��Ϊ2������ʹ���ֱ��к͵����ʵ�����NaOH�����Ĵ�����������
C. ��п��ϡ���ᷴӦ�������ȴ�п�죬����Ϊ��п�ȴ�п��ԭ��ǿ
D. �����£���0.1 mol/L��ˮ�У���������NH4Cl���壬��Һ��pH��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����顢��ϩ�ͱ������л���Ĺ�ͬ����
A. ����C��H����Ԫ�����
B. ����ʹ����KMnO4��Һ��ɫ
C. ���ܷ����ӳɷ�Ӧ��ȡ����Ӧ
D. ��O2����ȫȼ�ն�����CO2��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ����
A.���Ӿ����У�ֻ�������Ӽ�B.���������ڷ��Ӿ���
C.ԭ�Ӿ����У�ֻ���ڹ��ۼ�D.�����۵㣺���ʯ>ʳ��>��>�ɱ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C��D����ѧ��������������ᴿ�Ļ���װ�á�����ݻ���������ᴿ��ԭ�����ش�������ʵ������Ҫʹ������װ�á���A��B��C��D�����ʵ��Ŀո��С�

(1)��ȥCa(OH)2��Һ��������CaCO3_________________��
(2)�ӵ�ˮ��ȡ��______________��
(3)������ˮ��ȡ����ˮ_________________��
(4)����ֲ���ͺ�ˮ_____________��
(5)�뺣ˮɹ��ԭ���������_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������нϹ㷺�Ŀ������ã���ṹ��ʽ������ʾ
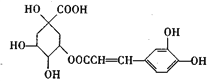
���ڿ��������������������ȷ����
A. ����ʽΪC16H18O9
B. ����̼ԭ�Ӳ����ܶ���ͬһƽ����
C. 1mol����������Ũ��ˮ��Ӧʱ��������5 molBr2
D. ��һ�������¿��Է���ȡ����Ӧ���ӳɷ�Ӧ����ȥ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������ܴﵽʵ��Ŀ�ĵ���(����)
��� | ʵ����� | ʵ��Ŀ�� |
�� | �μ����Ը��������Һ | ȷ�����л�����ȩ |
�� | ��ˮ����������Һ��ֱ�Ӽ�������������ͭ����Һ������ | ȷ�������Ƿ�ˮ�� |
�� | ����̼��������Һ | ȷ���Ҵ��л������� |
�� | �ӵ��� | ȷ��ʳ���к��е���� |
A. �٢� B. �ڢ� C. �٢� D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҷ����������ᣬij��ѧѧϰС���ͬѧ��̽���ⶨ���ᾧ�壨H2C2O4��xH2O����xֵ��ͨ���������ϸ�С��ͬѧͨ�������ѯ�ã�����������ˮ��ˮ��Һ����������KMnO4��Һ���еζ���2MnO4����5H2C2O4��6H�� 2Mn2����10CO2����8H2O
����ͬѧ����˵ζ��ķ����ⶨxֵ��

�� ��ȡ1.260 g�����ᾧ�壬�������Ƴ�100.00 mLˮ��ҺΪ����Һ��
�� ȡ25.00 mL����Һ������ƿ�У��ټ���������ϡH2SO4
�� ��Ũ��Ϊ0.1000 mol/L��KMnO4����Һ���еζ����ﵽ�յ�ʱ����10.00 mL��
��ش�
�� �ζ�ʱ����KMnO4��Һװ����ͼ�е� ����ס����ҡ����ζ����С�
�� ��ʵ��ζ��ﵽ�յ�ı�־������ ��
�� ͨ���������ݣ������x= ��
���ۣ������ζ��յ�ʱ���ӵζ��̶ܿȣ����ɴ˲�õ�xֵ�� ���ƫ����ƫС�����䡱����ͬ����
�����ζ�ʱ���õ�KMnO4��Һ����ö�����Ũ�ȱ�С�����ɴ˲�õ�xֵ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������и��仯�У���Ӧ��Ϊ�����µķ�Ӧ��A��C��D������Ԫ�أ���A����Ԫ�صĻ��ϼ۽���C��D֮�䣬E������Ϊ��ɫ��ζ��Һ�壬FΪ����ɫ��ĩ��GΪ��������ɫ���塣
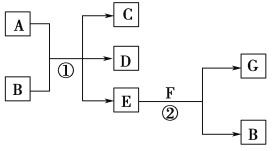
�ش��������⣺
��1��A��G�Ļ�ѧʽ�ֱ�Ϊ________��________��
��2��д����Ӧ�ڵĻ�ѧ����ʽ��___________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com