
【题目】在下列各变化中,反应①为常温下的反应,A、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,E常温下为无色无味的液体,F为淡黄色粉末,G为常见的无色气体。
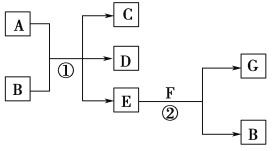
回答下列问题:
(1)A、G的化学式分别为________、________。
(2)写出反应②的化学方程式:___________________________________。
【答案】Cl2O22Na2O2+2H2O===4NaOH+O2↑
【解析】
E常温下为无色无味的液体,应为H2O,F为淡黄色粉末,应为Na2O2,则G为O2,B为NaOH,A、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,应为Cl2和NaOH的反应,生成NaCl和NaClO,结合物质的性质结合该题。
该题的突破口在于E和F的反应,E为常温下无色无味的液体,F为淡黄色粉末,则E为H2O,F为Na2O2,产生的无色气体G为氧气,B为NaOH,再结合A和B的反应,即可确定A为氯气。(1)由以上分析可知A为Cl2,G为O2;(2)反应②为过氧化钠与水反应生成氢氧化钠和氧气,反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑。


科目:高中化学 来源: 题型:
【题目】25℃时在五份蒸馏水中分别加入适量的下列物质,所得实验结果如下表所示:
加入物质 | HCl(aq) | FeCl3 | NaOH | HCOONa | C2H5OH |
溶液的pH | 3 | 4 | 10 | 11 | 未测定 |
水的电离程度 | α1 | α2 | α3 | α4 | α5 |
加入物质后水的电离程度由大到小排列顺序正确的是
A.α3>α1>α5>α2>α4 B.α4>α2>α5>α1>α3
C.α4>α2>α5>α3>α1 D.α1>α3>α5>α2>α4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇和乙酸是比较常见的有机物。
(1)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为_______________(不用写反应条件)。
(2)乙醇能够发生氧化反应:乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为_______。
(3)下列关于乙醇的说法正确的是______(选填字母)。
A.乙醇不能和酸性高锰酸钾溶液发生氧化还原反应
B.乙醇只能被氧化成乙醛
C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了
(4)当乙酸分子中的O都是18O时,乙醇分子中的O都是16O时,二者在一定条件下反应,生成物中水的相对分子质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝能提炼难熔金属和制成铝热剂,是因为铝( )
A.密度小,熔点较低
B.具有还原性,且生成氧化铝时放出大量热
C.在空气中燃烧,发出耀眼白光
D.是金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有0.1 mol/L的盐酸(a)、硫酸溶液(b)、醋酸溶液(c)各50 mL,试比较:
(1)三种酸的氢离子浓度由大到小的顺序是_________;三种酸的pH由大到小的顺序是______(填字母代号,下同)。
(2)三种酸跟足量的锌反应,开始时产生H2的速率由大到小的顺序是____________(不考虑Zn的纯度及表面积等问题)。
(3)三种酸跟足量的锌反应产生H2的体积由大到小的顺序是__________________。
(4)三种酸分别跟0.1 mol/L的NaOH溶液中和,消耗NaOH溶液的体积由大到小的顺序是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关图示分析正确的是( )
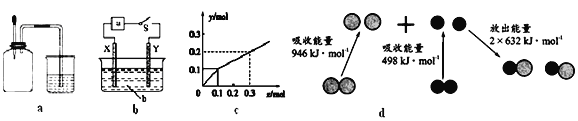
A. 如图a所示,集气瓶内充满Cl2和CH4的混合气体或NO2和O2的混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,并全部充满集气瓶
B. 如图b所示,X为铁棒,Y为铜棒,a为直流电源,当S闭合后,当b为NaOH溶液,X极附近产生白色沉淀时,电子从X极流入a
C. Pt为电极,电解含0.10 mol M+和0.1 mol N3+(M+、N3+均为金属阳离子)的溶液,阴极析出金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如图c,离子氧化能力M+>N3+>H+
D. 图d为N2(g)和O2(g)生成NO(g)过程中的能量变化,则N≡N的键能为946kJ/mol,热化学方程式为:N2(g)+O2(g)=2NO(g) ΔH=-180 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室需要0.5 mol·L-1硫酸溶液450 mL。根据溶液的配制情况回答下列问题:

(1)如图所示的仪器中配制溶液肯定不需要的是______(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(2)现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制450 mL、0.5 mol·L-1的稀硫酸。计算所需浓硫酸的体积为________ mL(保留1位小数),现有
①10 mL ②25 mL ③50 mL ④100 mL四种规格的量筒,你选用的量筒是________(填代号)。
(3)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是__________________________________________________________。
(4)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为:②→①→③→________→ ________→________→________→④(填序号)。_________
(5)在配制过程中,其他操作都准确,下列操作中错误的是________(填代号,下同),能引起误差偏高的有________。
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓硫酸直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓硫酸
④定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至刻度线
⑦定容时,俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在含有Fe3+、Fe2+、Cu2+的溶液中加入铁粉,充分反应后,固体残渣用盐酸处理有气体放出,则与铁粉反应后的溶液中最多的离子是( )
A.Fe3+
B.Fe2+
C.Cu2+
D.H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机化学反应属于加成反应的是
A.甲烷和氯气混合光照颜色逐渐变浅B.乙烯通入溴的四氯化碳溶液使其褪色
C.苯和液溴混合物中加入铁屑D.乙醇和金属钠反应产生氢气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com