
【题目】某化学实验室需要0.5 mol·L-1硫酸溶液450 mL。根据溶液的配制情况回答下列问题:

(1)如图所示的仪器中配制溶液肯定不需要的是______(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(2)现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制450 mL、0.5 mol·L-1的稀硫酸。计算所需浓硫酸的体积为________ mL(保留1位小数),现有
①10 mL ②25 mL ③50 mL ④100 mL四种规格的量筒,你选用的量筒是________(填代号)。
(3)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是__________________________________________________________。
(4)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为:②→①→③→________→ ________→________→________→④(填序号)。_________
(5)在配制过程中,其他操作都准确,下列操作中错误的是________(填代号,下同),能引起误差偏高的有________。
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓硫酸直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓硫酸
④定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至刻度线
⑦定容时,俯视刻度线
【答案】AD玻璃棒、胶头滴管13.6②将浓硫酸沿着烧杯壁(或玻璃棒)缓慢倒入水中,并不断用玻璃棒搅拌⑧ ⑤ ⑥ ⑦①②③④⑥⑦①②⑦
【解析】
(1)A为平底烧瓶、D为分液漏斗,在配制溶液过程中不会用到烧瓶和分液漏斗,答案选AD;配制一定浓度的溶液还缺少玻璃棒和胶头滴管;(2)质量分数为98%、密度为1.84 g·cm-3的浓硫酸的浓度为![]() mol·L-1=18.4 mol·L-1;实验室没有450 mL的容量瓶,实际上配制的是500 mL 0.5 mol·L-1的硫酸溶液,需要浓硫酸的体积为
mol·L-1=18.4 mol·L-1;实验室没有450 mL的容量瓶,实际上配制的是500 mL 0.5 mol·L-1的硫酸溶液,需要浓硫酸的体积为![]() ≈0.013 6 L=13.6 mL;(3)稀释浓硫酸时必须将浓硫酸加入水中,正确的操作方法为将浓硫酸沿着烧杯壁(或玻璃棒)缓慢倒入水中,并不断用玻璃棒搅拌;(4)配制一定物质的量浓度的溶液的步骤为计算、称量(量取)、溶解(稀释)、冷却、移液、洗涤、定容、摇匀,故正确的操作顺序为②→①→③→⑧→⑤→⑥→⑦→④;(5)①错误,原因:量筒不应洗涤,会引起浓度偏高;②错误,原因:温度偏高热胀冷缩,所以在定容时水加少了,导致配制的溶液的物质的量浓度偏高;③错误,原因:应该将浓硫酸缓慢加入水中,而不是将水加入浓硫酸中,这样会喷溅,有危险性;④错误,原因:水加多了,导致溶液的物质的量浓度偏小;⑥错误,原因:定容之后就不能加入水了;⑦错误,原因:应该视线与刻度线相平,俯视会导致加水偏少,浓度偏高。故操作中错误的是①②③④⑥⑦;能引起误差偏高的有①②⑦。
≈0.013 6 L=13.6 mL;(3)稀释浓硫酸时必须将浓硫酸加入水中,正确的操作方法为将浓硫酸沿着烧杯壁(或玻璃棒)缓慢倒入水中,并不断用玻璃棒搅拌;(4)配制一定物质的量浓度的溶液的步骤为计算、称量(量取)、溶解(稀释)、冷却、移液、洗涤、定容、摇匀,故正确的操作顺序为②→①→③→⑧→⑤→⑥→⑦→④;(5)①错误,原因:量筒不应洗涤,会引起浓度偏高;②错误,原因:温度偏高热胀冷缩,所以在定容时水加少了,导致配制的溶液的物质的量浓度偏高;③错误,原因:应该将浓硫酸缓慢加入水中,而不是将水加入浓硫酸中,这样会喷溅,有危险性;④错误,原因:水加多了,导致溶液的物质的量浓度偏小;⑥错误,原因:定容之后就不能加入水了;⑦错误,原因:应该视线与刻度线相平,俯视会导致加水偏少,浓度偏高。故操作中错误的是①②③④⑥⑦;能引起误差偏高的有①②⑦。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的的是( )
序号 | 实验操作 | 实验目的 |
① | 滴加酸性高锰酸钾溶液 | 确定苯中混有乙醛 |
② | 向水解后的蔗糖溶液中直接加入新制氢氧化铜悬浊液并加热 | 确定蔗糖是否水解 |
③ | 加入碳酸氢钠溶液 | 确定乙醇中混有乙酸 |
④ | 加淀粉 | 确定食盐中含有碘酸钾 |
A. ①② B. ②③ C. ①③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾在化学实验中是一种常用的氧化剂,某化学兴趣小组拟在实验室制备KMnO4并测定其纯度。
Ⅰ.KMnO4的制备
步骤1:利用下图所示装置制备K2MnO4
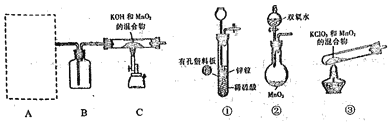
(1)装置A应选用_______( 填"①","②"或"③"),装置B中盛装的试剂是_______。
(2)装置C中反应生成K2MnO4的化学方程式为_________。
步骤2:由K2MnO4制备KMnO4
已知:①3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3
②相关物质的溶解度数据见下表:

实验流程如下:
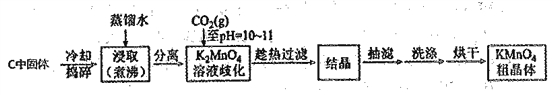
(3)结合相关物质的化学性质及溶解度,可以替代CO2的试剂是______________。
A.亚硫酸氢钾 B.稀硫酸 C.稀盐酸 D.稀醋酸
(4)当溶液pH达10~11时,停止通CO2;若CO2过量,会因生成____而使其和产品一起析出
(5)证明K2MnO4歧化完全的方法:取上层清液少许于试管中,通入CO2,若________,证明K2MnO4歧化完全。
Ⅱ.KMnO4纯度的测定
(6)通过用草酸(二元弱酸)滴定酸化后的KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数)。
①滴定过程中发生反应的离子方程式为__________________。
②称取 w g KMnO4粗产品配制100mL待测溶液,量取KMnO4待测液10.00mL于锥形瓶中进行实验,进行三次平行实验后测得平均消耗c mol/L草酸标准液V mL,则样品纯度的表达式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各变化中,反应①为常温下的反应,A、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,E常温下为无色无味的液体,F为淡黄色粉末,G为常见的无色气体。
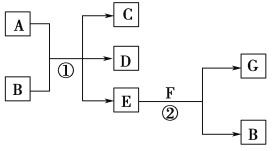
回答下列问题:
(1)A、G的化学式分别为________、________。
(2)写出反应②的化学方程式:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列①、②对应的试剂(或条件)不能完成实验目的的是 ( )
实验目的 | 试剂(或条件) |
| |
A | 温度对Na2S2O3与H2SO4反应速率的影响 | ①热水浴 ②冷水浴 | |
B | 用酸化的AgNO3溶液检验自来水中Cl-是否蒸馏除去 | ①自来水 ②蒸馏水 | |
C | 用Na块检验乙醇分子存在不同于烃分子里的氢原子 | ①乙醇 ②煤油 | |
D | 用溴水检验苯的同系物中取代基对苯基活性有影响 | ①苯 ②甲苯 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉煤气是炼铁厂排放的尾气,含有H2、N2、CO、CO2及O2,其中N2约为55%、CO约为25%、CO2约为15%、O2约为1.64% (均为体积分数)。某科研小组对尾气的应用展开研究:
Ⅰ.直接作燃料
己知:C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol, 2C(s)+O2(g)=2CO(g) △H=-221kJ/mol
(1)CO燃烧热的热化学方程式为__________________________________。
Ⅱ. 生产合成氨的原料
高炉煤气经过下列步骤可转化为合成氨的原料气:
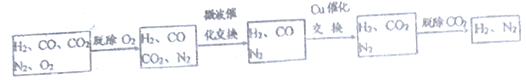
在脱氧过程中仅吸收了O2;交换过程中发生的反应如下,这两个反应均为吸热反应:
CO2+CH4![]() CO+H2 CO+H2O
CO+H2 CO+H2O![]() CO2+H2
CO2+H2
(2) 气体通过微波催化交换炉需要较高温度,试根据该反应特征,解释采用较高温度的原
因:________________________。
(3)通过铜催化交换炉后,所得气体中V(H2):V(N2)=______________________。
Ⅲ.合成氨后的气体应用研究
(4)氨气可用于生产硝酸,该过程中会产生大气污染物NOx。为了研究对NOx的治理,该研究小组在恒温条件下,向2L恒容密闭容器这加入0.2molNO和0.1molCl2,发生如下反应:2NO(g)+Cl2(g) ![]() 2ClNO(g) △H<0。10min 时反应达平衡,测得10min内v (ClNO)=7.5×10-3mol/(L·min),则平衡后n(Cl2)=___________mol。
2ClNO(g) △H<0。10min 时反应达平衡,测得10min内v (ClNO)=7.5×10-3mol/(L·min),则平衡后n(Cl2)=___________mol。
设此时NO的转化率为ɑ1,若其它条件不变,上述反应在恒压条件下进行,平衡时NO的转化率为ɑ2,则ɑ1_________ɑ2 (填“>”、“<”或“=”);平衡常数K_______(填“增大”“减小”或“不变”)
(5)氨气还可用于制备NCl3,NCl3发生水解产物之一具有强氧化性,该水解产物能将稀盐酸中的NaClO2氧化成ClO2,该反应的离子方程式为__________________________ 。
Ⅳ.一种用高岭土矿(主要成分为SiO2、Al2O3,含少量Fe2O3)为原料制备铝铵矾[NH4Al(SO4)2·12H2O]的工艺流程如图所示。回答下列问题:
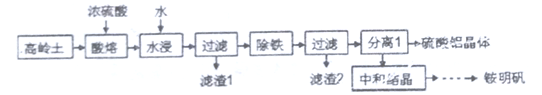
(6)当“酸溶”时间超过40min时,溶液中的Al2(SO4)3会与SiO2反应生成Al2O3·nSiO2,导致铝的溶出率降低,该反应的化学方程式为________________________。
(7)检验“除铁”过程中铁是否除尽的方法是_________________________。
(8)“中和”时,需控制条件为20℃和pH=2.8,其原因是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R、M、N是7种短周期元素,原子序数依次增大。已知X组成的单质是密度最小的气体,Y是形成化合物种类最多的元素,W原子最外层电子数是次外层电子数的3倍,R、M、N处于同一周期,R是该周期中金属性最强的元素,R与N能形成化合物RN,M与W同一主族。
请回答下列问题:
(1)Z在周期表中的位置是________________;N的原子结构示意图是____________。
(2)X、Y形成含碳量最小的有机物分子的空间构型是_____________。
(3)X、W、N按照原子个数比1∶1∶1形成的化合物的电子式为_____________。
(4)W与R形成的化合物R2W2可作供氧剂,该化合物含有的化学键类型有: _________,该化合物与YW2反应的化学方程式是__________________________________________________________。
(5)在一定条件下,往M的氢化物的水溶液中通入N的单质,出现混浊,则该反应的化学方程式是_________。此反应可证明单质氧化性M___________N(填“>”、“<”或“=”)。
(6)以上几种元素任意组合,可形成的酸性最强的物质是________________________,可形成的碱性最强的物质是_______________________(填写化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】基于CaSO4为载氧体的天然气燃烧是一种新型绿色的燃烧方式,CaSO4作为氧和热量的有效载体,能够髙效低能耗地实现CO2的分离和捕获其原理如下图所示:
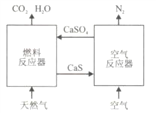
(1)已知在燃料反应器中发生如下反应:
i.CaSO4(g)+CH4(g)=4CaO(s)+CO2(g)+4SO2(g)+2H2O(g) ΔH1=akJ/mol
ii.CaSO4(s)+CH4(g)=CaS(s)+CO2(g)+2H2O(g) ΔH2=bkJ/mol
ⅲ. CaS(s)+3CaSO4(s)= 4CaO(s)+4SO2(g) ΔH3=ckJ/mol
①燃料反应器中主反应为_____________(填“i”“ ii”或“ⅲ”)。
②反应i和ii的平衡常数Kp与温度的关系如图1,则a_____________ 0(填“>”“ =” 或“<”);720℃时反应ⅲ的平衡常数Kp=_________________。
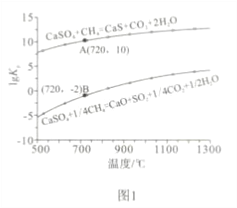

③下列措施可提高反应ii中甲烷平衡转化率的是______________ 。
A.增加CaSO4固体的投入量 B.将水蒸气冷凝
C.降温 D.增大甲烷流量
(2)如图2所示,该燃料反应器最佳温度范围为850℃-900℃之间,从化学反应原理的角度说明原因:
________________________。
(3)空气反应器中发生的反应为
CaS(s) +2O2(g)=CaSO4(s) ΔH4=dkJ/mol
①根据热化学原理推测该反应为 __________________(填“吸热”或“放热”) 反应。
(4)该原理总反应的热化学方程式为_____________________________。
(5)25℃时,用Na2S沉淀Cu2+、Sn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如右图所示,请回答:

25℃时向50mL的Sn2+、Cu2+浓度均为0.01 mol/L的混合溶液中逐滴加入Na2S溶液,当Na2S溶液加到150mL时开始生成SnS沉淀,则此时溶液中Cu2+浓度为___________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答问题:
(1)以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池中:
①H+向___________极移动(填“正”或“负”)。
②电子流动方向由____________极流向____________极(填:“正”、“负”)。
③若有1mol e- 流过导线,则理论上负极质量减少____________g。
④若将稀硫酸换成硫酸铜溶液,电极质量增加的是___________(填“锌极”或“铜极”),原因是_____________(用电极方程式表示)。
(2)一定温度下,在容积为2 L的密闭容器中进行反应:aN(g) ![]() bM(g) +cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
bM(g) +cP(g),M、N、P的物质的量随时间变化的曲线如图所示:

①反应化学方程式中各物质的系数比为a∶b∶c=_________。
②1 min到3 min这段时刻,以M的浓度变化表示的平均反应速率为:________________________。
③下列叙述中能说明上述反应达到平衡状态的是____________________________。
A.反应中当M与N的物质的量相等时
B.P的质量不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.单位时间内每消耗a mol N,同时消耗b mol M
E.混合气体的压强不随时间的变化而变化
F.M的物质的量浓度保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com