
����Ŀ��X��Y��Z��W��R��M��N��7�ֶ�����Ԫ�أ�ԭ����������������֪X��ɵĵ������ܶ���С�����壬Y���γɻ�������������Ԫ�أ�Wԭ�������������Ǵ�����������3����R��M��N����ͬһ���ڣ�R�Ǹ������н�������ǿ��Ԫ�أ�R��N���γɻ�����RN��M��Wͬһ���塣
��ش��������⣺
��1��Z�����ڱ��е�λ����________________��N��ԭ�ӽṹʾ��ͼ��____________��
��2��X��Y�γɺ�̼����С���л�����ӵĿռ乹����_____________��
��3��X��W��N����ԭ�Ӹ�����1��1��1�γɵĻ�����ĵ���ʽΪ_____________��
��4��W��R�γɵĻ�����R2W2�������������û����ﺬ�еĻ�ѧ�������У� _________���û�������YW2��Ӧ�Ļ�ѧ����ʽ��__________________________________________________________��
��5����һ�������£���M���⻯���ˮ��Һ��ͨ��N�ĵ��ʣ����ֻ��ǣ���÷�Ӧ�Ļ�ѧ����ʽ��_________���˷�Ӧ��֤������������M___________N�����������������������
��6�����ϼ���Ԫ��������ϣ����γɵ�������ǿ��������________________________�����γɵļ�����ǿ��������_______________________����д��ѧʽ��
���𰸡��ڶ����ڵ�VA�� 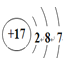 ��������
��������![]() ���Ӽ� ���ۼ���Ǽ��Թ��ۼ�2Na2O2��2CO2��2Na2CO3��O2Cl2��H2S��S����2HCl��HClO4NaOH
���Ӽ� ���ۼ���Ǽ��Թ��ۼ�2Na2O2��2CO2��2Na2CO3��O2Cl2��H2S��S����2HCl��HClO4NaOH
��������
X��ɵĵ������ܶ���С�����壬˵��XΪ��Ԫ�أ�Y���γɻ�������������Ԫ�أ�˵��Y��̼Ԫ�أ�Wԭ�������������Ǵ�����������3����˵��W����Ԫ�أ�R��M��N����ͬһ���ڣ�R�Ǹ������н�������ǿ��Ԫ�أ�˵��RΪ��Ԫ�أ�R��N���γɻ�����RN��˵��NΪ��Ԫ�أ�M��Wͬһ���壬˵��MΪ��Ԫ�أ�X��Y��Z��W��R��M��N��7�ֶ�����Ԫ�أ�ԭ��������������˵��ZΪ��Ԫ�أ��ݴ˷����ɵý��ۡ�
��1��ZΪ��Ԫ�أ�NΪ��Ԫ�أ��ʴ�Ϊ���ڶ����ڵ�VA�塢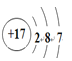 ��
��
��2��X��Y�γɺ�̼����С���л�������Ǽ�����ӣ���ռ乹��Ϊ�������壬�ʴ�Ϊ���������壻
��3��X��W��N����ԭ�Ӹ�����1��1��1�γɵĻ�����ΪHClO�������ʽΪ��![]() ����4��W��R�γɵĻ�����R2W2Ϊ�������ƣ��������Ӽ����ۼ����ʴ�Ϊ�����Ӽ������ۼ���Ǽ��Թ��ۼ��� 2Na2O2��2CO2��2Na2CO3��O2��
����4��W��R�γɵĻ�����R2W2Ϊ�������ƣ��������Ӽ����ۼ����ʴ�Ϊ�����Ӽ������ۼ���Ǽ��Թ��ۼ��� 2Na2O2��2CO2��2Na2CO3��O2��
��5��M���⻯���ˮ��Һ��ͨ��N�ĵ���Ϊ�û���Ӧ������ʵ˵���ȵķǽ�����ǿ���ʴ�Ϊ��Cl2��H2S��S����2HCl������
��6�����γɵ�������ǿ��������Ԫ�ص�����������Ӧ��ˮ�����HClO4�����γɵļ�����ǿ�����ʵ���Ԫ�ص�����������Ӧ��ˮ�����NaOH���ʴ�Ϊ��HClO4��NaOH��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ٵ��������ܹ��ڷֽ��л����ͬʱ�������ʲ������ܣ���ԭ������ͼ��ʾ���л���ΪC6H12O6)������˵����ȷ����

A. AΪ������H2PCA�ڸõ缫�Ϸ���������Ӧ
B. �ŵ�����У�������ӦΪ2H2O-4e=4H++O2��
C. ��1molO2����缫��Ӧ����2 mol H+�������ӽ���Ĥ��������
D. ����ܷ�ӦΪ:C6H12O6+6O2![]() 6CO2��+6H2O
6CO2��+6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.1 mol/L��������a����������Һ��b����������Һ��c����50 mL���ԱȽϣ�
��1���������������Ũ���ɴ�С��˳����_________���������pH�ɴ�С��˳����______������ĸ���ţ���ͬ����
��2���������������п��Ӧ����ʼʱ����H2�������ɴ�С��˳����____________��������Zn�Ĵ��ȼ����������������
��3���������������п��Ӧ����H2������ɴ�С��˳����__________________��
��4��������ֱ��0.1 mol/L��NaOH��Һ�кͣ�����NaOH��Һ������ɴ�С��˳����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧʵ������Ҫ0.5 mol��L��1������Һ450 mL��������Һ����������ش��������⣺

��1����ͼ��ʾ��������������Һ�϶�����Ҫ����______(�����)������������Һ�����õ��IJ���������________(����������)��
��2��������������Ϊ98%���ܶ�Ϊ1.84 g��cm��3��Ũ����������450 mL��0.5 mol��L��1��ϡ���ᡣ��������Ũ��������Ϊ________ mL(����1λС��)������
��10 mL����25 mL����50 mL����100 mL���ֹ�����Ͳ����ѡ�õ���Ͳ��________(�����)��
��3�����ƹ������������ձ��н�Ũ�������ϡ�ͣ�ϡ��ʱ����������__________________________________________________________��
��4������ʱ��һ��ɷ�Ϊ���¼������裺
����ȡ���ڼ��㡡��ϡ�͡���ҡ�ȡ���ת�ơ���ϴ�ӡ��߶��ݡ�����ȴ
����ȷ�IJ���˳��Ϊ��������������________�� ________��________��________����(�����)��_________
��5�������ƹ����У�����������ȷ�����в����д������________(����ţ���ͬ)�����������ƫ�ߵ���________��
��ϴ����ȡŨ��������Ͳ������ϴ��Һת�Ƶ�����ƿ��
��δ��ϡ�ͺ��H2SO4��Һ��ȴ�����¾�ת�Ƶ�����ƿ��
�۽�Ũ����ֱ�ӵ����ձ��������ձ���ע������ˮ��ϡ��Ũ����
�ܶ���ʱ��������ˮ�����̶��ߣ����ý�ͷ�ι�����
��ת��ǰ������ƿ�к�����������ˮ
����ҡ�Ⱥ���Һ����ڱ��ߣ����ý�ͷ�ιܼ�����ˮ���̶���
�߶���ʱ�����ӿ̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ�� X��Y��Z��W��ԭ������������������Ԫ���γɵĵ�������Ϊm��n��p��q��r��t��u ����ЩԪ����ɵĶ�Ԫ���������uΪ���Ѿ��е��־��ɷ֣�25 ����0.01 mol/L��v��Һ�У� 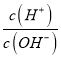 = 1.0��10-10���������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��
= 1.0��10-10���������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��
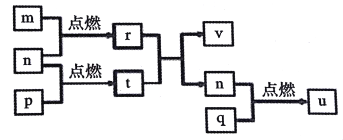
A. �����Ӱ뾶��W>Z>Y>X
B. W��Y�քe��XԪ���γɵļ�����ķе㣺 W> Y
C. Z2Y��ZX�д��ڵĻ�ѧ��������ͬ
D. v������ˮ�ĵ��룬u�ܴٽ�ˮ�ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں���Fe3+��Fe2+��Cu2+����Һ�м������ۣ���ַ�Ӧ������������ᴦ��������ų����������۷�Ӧ�����Һ�����������ǣ� ��
A.Fe3+
B.Fe2+
C.Cu2+
D.H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2(������Ԫ��Ϊ-2��)��һ������ɱ��Ч�ʸߡ�������ȾС��ˮ��������ʵ�����п�ͨ�����·�Ӧ�Ƶ�ClO2��2KClO3+H2C2O4+H2SO4![]() 2ClO2��+K2SO4+2CO2��+2H2O��
2ClO2��+K2SO4+2CO2��+2H2O��
(1)�÷�Ӧ����������__________��
(2)���ռ������������22.4Lʱ,��μӷ�Ӧ��H2C2O4���������ʵ���__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѧ�Dѡ��5���л���ѧ������
��̼������PC����һ��ǿ�͵���������֬���㷺���ڲ���װ��ҵ��������ҵ�����Ӻ͵�����ҵ��PC��һ�ֺϳ�·�����£�
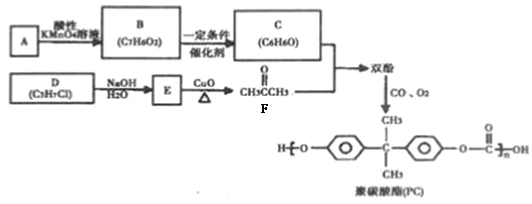
�ش��������⣺
��1����A ������ͼ���£���A �ķ���ʽΪ__________��
��2��D ������Ϊ_________��D��E�ķ�Ӧ����Ϊ_______��
��3��˫�ӵĽṹ��ʽΪ_______��
��4��B ��E �����γ�һ����������F��д��B + E��F��Ӧ�Ļ�ѧ����ʽ��_______��
��5��F��ͬ���칹���У���ͬʱ�������������Ĺ���______�֣������������칹����
�� ����������������
�� �ܷ���������Ӧ��
�� ��������Һ�е�ˮ�������FeC13 ��Һ����ɫ��
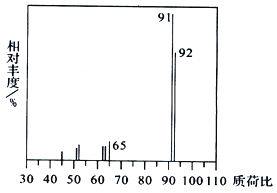
д�����к˴Ź���������ʾ5��壬�ҷ������Ϊ62:2:11���ַ��ӵĽṹ��ʽ��_______��
��6��д����D���Ӻϳɸ��ͣ����������ĺϳ�·��ͼ_______������֪��![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CO��H2Ϊԭ������������(CH3OCH3)��Ҫ��������������Ӧ

��1���ù��յ��ܷ�ӦΪ3CO(g)+3H2(g) ![]() CH3OCH3(g)+CO2(g)��H
CH3OCH3(g)+CO2(g)��H
�÷�Ӧ��H=_______________,��ѧƽ�ⳣ��K=__________(�ú�K1��K2��K3�Ĵ���ʽ��ʾ)��
��2��ij�¶���,��8.0molH2��4 molCO�����ݻ�Ϊ2L���ܱ�������,������Ӧ:4H2(g)+2CO(g) ![]() CH3OCH3(g)+H2O(g),5���Ӻ�Ӧ��ƽ��,��ö����ѵ��������Ϊ1/6,����CH3OCH3��Ũ�ȱ仯��ʾ�÷�Ӧ������Ϊ__________mol��L��1min��1,CO��ת����Ϊ_________��
CH3OCH3(g)+H2O(g),5���Ӻ�Ӧ��ƽ��,��ö����ѵ��������Ϊ1/6,����CH3OCH3��Ũ�ȱ仯��ʾ�÷�Ӧ������Ϊ__________mol��L��1min��1,CO��ת����Ϊ_________��
��3�����д�ʩ��,���ܼӿ췴Ӧ�����������CH3OCH3���ʵ���___________��
A.����������� B.�����¶� C.���ø�Ч���� D.����ѹǿ
��4���ù����з�Ӧ�۵ķ��������CH3OCH3�IJ���ԭ����_________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com