
【题目】镁与稀硝酸的反应为:4Mg+10HNO3(稀)=4Mg(NO3)2+NH4NO3+3H2O
(1)用“双线桥法”表示该反应中电子转移的方向和数目__________。
(2)该反应中,Mg发生了__________反应,氧化剂与还原剂的物质的量之比为__________________。
(3)还原产物是_________,HNO3表现了__________________。
(4)若反应过程中转移的电子数为1.505×1023,则参加反应的Mg的质量为________。
【答案】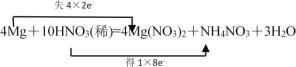 氧化 1∶4 NH4NO3 氧化性,酸性 3g
氧化 1∶4 NH4NO3 氧化性,酸性 3g
【解析】
氧化剂得电子化合价降低发生还原反应转化成还原产物,还原剂失去电子化合价升高发生氧化反应转化成氧化产物。
(1)反应中Mg是还原剂失去电子被氧化生成Mg(NO3)2,HNO3是氧化剂被还原生成NH4NO3,一个Mg失去2个电子,一共4个Mg参与反应,因此失去电子数为4×2e-;只有一个HNO3表现氧化性,失去8个电子。用双线桥表示如下:
(2)Mg是还原剂发生了氧化反应,根据化学方程式可知只有一个HNO3表现氧化性,因此氧化剂与还原剂的物质的量之比为1∶4。
(3)氧化剂对应还原产物,HNO3是氧化剂,还原产物是NH4NO3;HNO3表现了氧化性和酸性。
(4)1 mol Mg转移2 mol e-,当转移的电子数为1.505×1023时,Mg的物质的量n=![]() ×
×![]() =0.125mol,m=0.125×24=3 g。
=0.125mol,m=0.125×24=3 g。


科目:高中化学 来源: 题型:
【题目】某同学拟用氯化钙固体、碳酸钠溶液和稀硝酸等试剂,先制得碳酸钙,最终制得纯净的硝酸钙晶体。
(1)写出制取过程中反应的离子方程式:________________、________________________。
(2)请帮助该同学完成下列实验操作步骤(不要求回答使用的仪器)
①用蒸馏水完全溶解CaCl2后,加入________。
②将反应后的混合物过滤,并用适量蒸馏水洗涤沉淀至无Cl-。
③加入________________,使沉淀完全溶解。
④将所得溶液蒸发、结晶,得到纯净的硝酸钙晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,对于可逆反应M+3N![]() 2Q(g),平衡时Q的体积分数与温度和压强的关系如图所示,下列判断正确的是
2Q(g),平衡时Q的体积分数与温度和压强的关系如图所示,下列判断正确的是
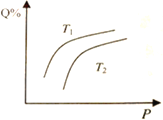
A. M和N不能都为气体
B. 由上图可知, N一定为气体
C. 若正反应方向ΔH>0,则T1<T2
D. 其它条件不变,压强增大,混合气体的平均相对分子质量减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液的物质的量浓度的计算正确的是
A. 标准状况下,a L NH3溶于1000 g水中,得到的溶液密度为b gcm-3,(考虑溶液体积变化)则该溶液的物质的量浓度为![]() molL-1
molL-1
B. 将100 mL 1.5 molL-1的NaCl溶液与200 mL 2.5 molL-1的NaCl溶液混合(忽略溶液体积变化),得到溶液的物质的量浓度为2 molL-1
C. V L Fe2(SO4)3溶液中含Fe3+m g,溶液中c(SO42-)是![]() molL-1
molL-1
D. 某温度时,饱和NaCl溶液的密度为ρ gcm-3,物质的量浓度为cmol/L,该溶液中NaCl的质量分数为![]() ×100%
×100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一只长滴管,深入液面下,向盛有FeCl2溶液的试管中滴加NaOH溶液,可观察到有白色沉淀生成.生成白色沉淀的离子方程式 , 在空气中放置的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的有机原料,在催化剂的作用下,CO和H2反应可生成甲醇 (CH3OH) 和副产物CH4,反应如下:
反应①CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.0kJ/mol
CH3OH(g) △H1=-90.0kJ/mol
反 应②CO(g)+3H2(g)![]() CH4(g) + H2O(g) △H2
CH4(g) + H2O(g) △H2
反应③ CH4(g)+2H2O(g)![]() CO2(g)+ 4H2(g) △H3=+125.0 kJ/mol
CO2(g)+ 4H2(g) △H3=+125.0 kJ/mol
反应④CO(g)+ H2O(g)![]() CO2(g) + H2(g) △H4=-25.0 kJ /mol
CO2(g) + H2(g) △H4=-25.0 kJ /mol
K1、K2、K3、K4分别表示反应①、②、③、④的平衡常数。
回答下列问题:
(1)反应②的平衡常数的表达式为K2=______________,K2与K3和K4的关系为K2=______________,△H2=____________kJ/mol。
(2)图1中能正确表示反应①的平衡常数(lgK1) 随温度变化的曲线为______________(填曲线字母),其判断理由为______________________________________________________________。

(3)恒温恒容的条件下,下列情况能说明反应①达到平衡状态的是__________________。
A.2v正 (H2)=v逆(CH3OH) B.混合气体的密度不再改变
C.混合气体的平均摩尔质量不再改变 D.混合气体的压强不再改变
(4)为探究不同催化剂对CO和H2生成CH3OH的选择性效果,某实验室控制CO和H2的初始投料比为1∶3进行实验,得到如下数据:
T/K | 时间/min | 催化剂种类 | 甲醇的含量(%) |
450 | 10 | CuO-ZnO | 78 |
450 | 10 | CuO-ZnO-ZrO2 | 88 |
450 | 10 | ZnO-ZrO2 | 46 |

①由表1可知,反应①的最佳催化剂为______________,图2中a、b、c、d四点是该温度下CO平衡转化率的是_________________________________。
②有利于提高CO转化为CH3OH的平衡转化率的措施有_________________。
A.使用催化剂CuO-ZnO-ZrO2 B.适当降低反应温度
C.增大CO和H2的初始投料比 D.恒容下,再充入a molCO和3a mol H2
(5)已知1000℃,反应CO(g)+ H2O(g)![]() CO2(g) + H2(g) K4=1.0。该温度下,在某时刻体系中CO、H2O、CO2、H2的浓度分别为3molL-1、1molL-1、4molL-1、2molL-1,则此时上述反应的v正(CO)_______v逆(CO) (填“>”、“<”或“=”)达到平衡时c(CO)=___________ molL-1。
CO2(g) + H2(g) K4=1.0。该温度下,在某时刻体系中CO、H2O、CO2、H2的浓度分别为3molL-1、1molL-1、4molL-1、2molL-1,则此时上述反应的v正(CO)_______v逆(CO) (填“>”、“<”或“=”)达到平衡时c(CO)=___________ molL-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某容积固定的密闭容器由可移动的活塞隔成 A、B 两室,向 A 中充入一定量 H2、O2 的混合气体,向 B 中充入 1 mol 空气,此时活塞的位置如图所示。

(1)A 室混合气体的物质的量为______,所含分子总数约______。
(2)实验测得 A 室混合气体的质量为 34 g,则该混合气体的密度是同温同压条件下氦气密度的______倍。
(3)若将 A 室 H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在______刻度,容器内气体压强与反应前气体压强之比为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com