
【题目】短周期主族元素X、Y、Z、W 的原子序数依次增大,X、Y 为有机物中常见元素,Y、Z、W 同周期,由四种元素形成的化合物甲的结构如图。下列说法正确的是
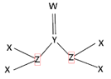
A.最高化合价:W>Z>Y>X
B.蛋白质中一定含有这四种元素
C.(YZ)2 与 X2W2 均为直线型分子
D.化合物甲的一种同分异构体可能既有离子键又有共价键
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料。粗盐中常含有少量泥沙及Ca2+、Mg2+、SO42-等杂质离子。为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:
![]()
(1)为除去Ca2+、Mg2+、SO42-,步骤②~④需加入以下三种溶液(用于沉淀的试剂稍过量);加入的顺序为_____________(填字母)。
A.Na2CO3 B.BaCl2 C.NaOH
(2)请写出步骤⑥中涉及反应的离子方程式: ______________________________________。
(3)粗盐提纯的整个操作过程中多处使用到玻璃棒,步骤⑦蒸发过程中使用玻璃棒的作用是_____________________________________。
(4)若先加盐酸再过滤,将对提纯效果产生影响,其原因是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将32.0g铜与60.0mL一定浓度的硝酸发生如下反应:Cu+4HNO3 = Cu(NO3)2+2NO2↑+2H2O;3Cu+8HNO3 = 3Cu(NO3)2+2NO↑+4H2O。铜完全溶解产生的混合气体体积为8.96L(标况)。请计算(各数据保留两位有效数字):
(1)NO的体积为______
(2)该混合气体的平均摩尔质量约为______
(3)待产生的气体全部释放后,向溶液加入100mL 2.0mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科研人员利用Cu/ZnO作催化剂,在光照条件下实现了CO2和H2合成CH3OH,该反应历程示意图如下。
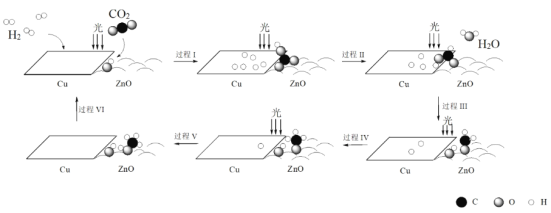
下列说法不正确的是
A.过程I中ZnO表面上进行CO2的吸附与转化
B.过程II中存在极性键的断裂与形成
C.过程V中生成CH3OH时吸收能量
D.总反应的化学方程式是CO2 + 3H2![]() CH3OH + H2O
CH3OH + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的制备、性质、收集说法正确的是( )
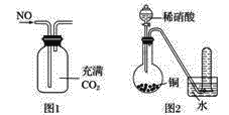
A.汽车尾气中有NOx,主要是汽车打火时氮气和氧气反应引起的
B.可以用图1所示装置收集到干燥的NO气体
C.根据图2装置收集到的气体为无色能够验证铜和稀硝酸反应的产物中气态物质只有NO
D.可以用湿润的淀粉碘化钾试纸鉴别红棕色气体NO2和溴蒸气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019 年的化学诺贝尔奖颁给了为锂电池研究作出贡献的三位科学家,其研究的是两种常见锂电池:一种是采用镍钴锰酸锂Li(NiCoMn)O2或镍钴铝酸锂为正极的“三元材料锂电池”;另一种是采用磷酸铁锂(LiFePO4)为正极的电池。请回答下列问题:
(1)Mn位于元素周期表的_____区(填“s”或“p”或“d”或“ds”或“f”),基态钴原子的未成对电子数为_____,1mol [Co(NH3)5Cl]Cl2中含σ键数目为___ NA。
(2)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是______________。![]() 的空间构型是________________,HPO3中心原子的杂化方式是_________________。
的空间构型是________________,HPO3中心原子的杂化方式是_________________。
(3)PH3是_____分子(填“极性”或“非极性”),其在水中的溶解性比NH3小,原因是____。
(4)硫化锂Li2S(摩尔质量Mgmol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如下图。S2-的配位数是______;若硫化锂晶体的密度为a g·cm -3,则距离最近的两个S2-的距离是_____nm。(用含 a、M、NA的计算式表示)。
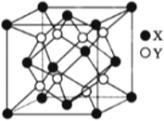
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关溶液中离子存在和转化的表达合理的是( )
A.中性溶液中可能大量存在Fe3+、K+、Cl-、SO![]()
B.离子方程式2Ca2++3HCO![]() +3OH-═2CaCO3↓+CO
+3OH-═2CaCO3↓+CO![]() +3H2O可以表示NH4HCO3与澄清石灰水反应
+3H2O可以表示NH4HCO3与澄清石灰水反应
C.由水电离出的c(H+)=1×10-12mol/L的溶液中可能大量存在K+、I-、Mg2+、NO![]()
D.n[NH4Al(SO4)2]:n[Ba(OH)2]=2:5时发生的反应为NH![]() +Al3++2SO
+Al3++2SO![]() +2Ba2++5OH-═NH3H2O+AlO
+2Ba2++5OH-═NH3H2O+AlO![]() +2H2O+2BaSO4↓
+2H2O+2BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应![]() 达到平衡,正反应速率随时间变化的示意图如下所示。
达到平衡,正反应速率随时间变化的示意图如下所示。
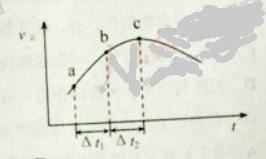
A. 反应在c 点达到平衡状态
B. 反应物浓度:![]() 点小于
点小于![]() 点
点
C. 反应物的总能量低于生成物的总能量
D. ![]() 时,SO2的转化率:
时,SO2的转化率:![]() 段小于
段小于![]() 段
段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将以下4份溶液分别置于如图的装置中,其他条件相同时,灯泡最亮的是( )
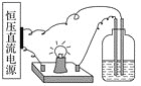
A. 100 mL 1 mol·L-1的盐酸
B. 100 mL 2 mol·L-1的蔗糖溶液
C. 100 mL 1 mol·L-1的氯化钠溶液
D. 30 mL 1 mol·L-1的氯化钙溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com