
����Ŀ��K4[Fe(CN)6]�������������ᡢҩ��ȡ�
(1)Fe2+�ĺ�������Ų�ʽΪ_____��
(2)CN����Cԭ�ӹ�����ӻ�����Ϊ_____����CN����Ϊ�ȵ������һ�ַ��ӵĽṹʽΪ_____��
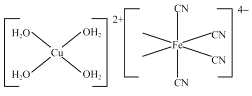
(3)[Cu(H2O)4]2+�ṹʾ��ͼ��ͼ��ʾ��[Fe(CN)6]4���ṹʾ��ͼ��ͼ��ʾ������ͼ����Ӧλ�ò�������_________��
(4)��֪3K4Fe(CN)6![]() 12KCN+Fe3C+3C+(CN)2��+2N2����(CN)2��������������������Ŀ��n(��)��n(��)��_____��
12KCN+Fe3C+3C+(CN)2��+2N2����(CN)2��������������������Ŀ��n(��)��n(��)��_____��
(5)����ý�Ǻϳɰ���Ӧ�Ĵ������������ڵ�ԭ�ӡ���ԭ�����������ϵĵ��㸽�žֲ�ʾ����ͼ��ʾ�����������ϵ�ԭ������ԭ�ӵ���Ŀ��Ϊ_____��

���𰸡�[Ar]3d6��1s22s22p63s23p63d6 sp N��N��C��O 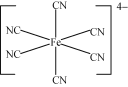 3��4 1��2
3��4 1��2
��������
��1����������ԭ������ع�����д���������Ų�ʽ��
��2������ԭ�ӵ��ӻ������ж����ӻ����ͣ��ٽ�ϵȵ�����ԭ�������ҳ���ȵ����壻
��3��������������ۣ��������ṩ�µ��ӶԵ�ԭ��ΪC�����[Cu(H2O)4]2���ṹʾ��ͼ���ɣ�
��4������C��Nԭ������8�����ȶ��ṹ����ȷ��д��ṹʽ�����ݹ��ۼ������ҵ���������������������Ŀ��
��5���þ�����ÿ��Nԭ����Χ��4��Feԭ�ӡ�ÿ��Feԭ����Χ��2��Nԭ�ӣ����þ�̯������������������Fe��Nԭ�����ı�ֵ��
��1��Fe��ԭ������Ϊ26��Fe2���ĺ��������Ϊ24��Fe2���ĺ�������Ų�ʽΪ[Ar]3d6��1s22s22p63s23p63d6��
�ʴ�Ϊ��[Ar]3d6��1s22s22p63s23p63d6��
��2��CN�����ӻ������Ϊ2��δ�ӻ���2��p����γ�2���������������sp�ӻ���ʽ��N2��CO������CN-��ԭ������Ϊ2���۲��������Ϊ10����Ϊ�ȵ����壬����CN����Ϊ�ȵ������һ�ַ��ӵĽṹʽΪN��N��C��O��
�ʴ�Ϊ��sp��N��N��C��O��
��3��[Fe(CN)6]4������λ��Ϊ6����ͼ�п��Կ����������е�Cԭ���ṩ�¶Ե�������������Fe2+�γ���λ��������ṹʾ��ͼ�ɱ�ʾΪ��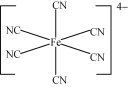 ��
��
�ʴ�Ϊ�� ��
��
��4��(CN)2���ӵĽṹʽΪN��C-C��N������һ�����۵���Ϊһ��������һ����������Ϊһ��������2��������֪����÷����ڷ�����������3����������4������CN)2��������������������Ŀ��n(��)��n(��)��3��4��
�ʴ�Ϊ��3��4��
��5���þ�����ÿ��Nԭ����Χ��4��Feԭ�ӡ�ÿ��Feԭ����Χ��2��Nԭ�ӣ����þ�̯��֪���������ϵ�ԭ������ԭ�ӵ���Ŀ��Ϊ=![]() ��
��![]() = 1��2��
= 1��2��
�ʴ�Ϊ��1��2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£����ܱ�������������¿��淴Ӧ:S2Cl2(�Ȼ�ɫҺ��)+Cl2(��)![]() 2SCl2(�ʺ�ɫҺ��)����H=-61. 16 kJ��mol-1������˵����ȷ����
2SCl2(�ʺ�ɫҺ��)����H=-61. 16 kJ��mol-1������˵����ȷ����
A. ����ѹǿ��ƽ�ⳣ��������
B. �ﵽƽ��ʱ����λʱ��������n mol S2Cl2��ͬʱҲ����n mol Cl2
C. �ﵽƽ��ʱ���������¶ȣ������İٷֺ�����С
D. ����������ƽ��������Ӧ�����ƶ���������ת����һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ���õ�����ȡ����ͭ���壬���о�����ͭ�ܷ�����������ȷֽ�ʵ����������á�ʵ�鲽�����£�

������a g������������ձ��У���ˮ�Ƴ���Һ�������еμ�����������Һ��������ȫ��
���Ѳ������е���Һ�ͳ���ת�����������У���������Һ�еij���ȫ��ɺ�ɫ����ͭΪֹ��
�����ˡ�ϴ�ӡ�����������ù�������Ϊb g��
��ȡһ����������������ͭ�����һ������������ع��壬��Ͼ��Ⱥ���ȣ��ռ���Ӧ���ɵ���������ͼ��ʾ��
��ش��������⣺
��1���������������У���Ҫ�õ�����������__________________����дǰ������ʵ�鲽�����ţ���
��2���ɵ����Ʊ�����ͭ�IJ��ʣ�ʵ�ʲ��������۲����İٷֱȣ�Ϊ____________��100%��
��3��Ϊ��֤Cu2+������ȫ������������Һ��pHӦ����10�������ⶨ��ҺpH�IJ�����____________________________ ��
��4��Ϊ֤������ͭ������صķֽⷴӦ��������ã�������ʵ����������Ӧ�ý��е�ʵ������� ����ʵ���Ⱥ�˳����д��ĸ��ţ���
�� ���� �� ��� �� �ܽ� �� ϴ�� �� ����
��5������ͬѧ��Ϊ�����������������һ��ʵ�����֤������ͭ����������ȷֽ��ʵ����������á�����Ϊ��Ӧ�ý��е���һ��ʵ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���Ƚ�����ȷ����
A. �۵㣺Li<Na<K
B. �ȶ��ԣ�CH4<NH3<H2O<HF
C. ���ԣ�HClO4<H2SO4<H3PO4
D. ��ԭ�ԣ�Br��<Cl��<S2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ�ص��ʼ��仯�������Ź㷺Ӧ�á�
��1����1. 0 L�ܱ������з���0. 10mol PCl5(g)��һ���¶Ƚ������·�Ӧ:PCl5(g)![]() PCl3(g)��Cl2(g) ��H1����Ӧʱ��(t)��������������ѹǿ(p/100kPa)�����ݼ��±���
PCl3(g)��Cl2(g) ��H1����Ӧʱ��(t)��������������ѹǿ(p/100kPa)�����ݼ��±���
ʱ��t/s �¶� | 0 | t1 | t2 | t3 | t4 | t5 |
T1 | 5. 00 | 7. 31 | 8. 00 | 8. 50 | 9. 00 | 9. 00 |
T2 | 6. 00 | -- | -- | -- | 11. 00 | 11. 00 |
�ش���������:
��PCl3�ĵ���ʽΪ_______��
��T1�¶��£���Ӧƽ�ⳣ��K=______��
��T1___T2�����������������������ͬ����PCl5��ƽ��ת���ʦ�1(T1) __��2(T2)��
��2��NO��һ�������·������·ֽ⣺3NO(g)![]() N2O(g)+NO2(g)
N2O(g)+NO2(g)
���¶Ⱥ��ݻ�����������£���˵���÷�Ӧ�Ѵﵽƽ��״̬����________(����ĸ���)��
a. n(N2O)=n(NO2) b. ������ѹǿ���ֲ��� c. v��(N2O)=v��(NO2) d. ������ɫ���ֲ���
��3����������[Co(H2PO2)2]�㷺���ڻ�ѧ���ܣ��Խ����ܺʹ�������Ϊԭ�ϣ��������ҵ������۵�ⷨ�Ʊ���ԭ������ͼ��

��Co�ĵ缫��ӦʽΪ_______��
��A��B��CΪ���ӽ���Ĥ������BΪ____���ӽ���Ĥ�����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�������Ա�������CO2��CH4ת��Ϊ�߸���ֵ��ƷCH3COOH�Ĵ���Ӧ���̡�������ʾ��ͼ���¡�(��ʾ��ԭ��������=Ŀ�������������/�μӷ�Ӧ�����з�Ӧ���������100%��������˵����ȷ����

A. �١��������������γ���C�DC��
B. CH4��CH3COOH����������C�DH����������
C. �ô�������Ч��߷�Ӧ���ƽ��ת����
D. ����CH3COOH�ܷ�Ӧ��ԭ��������С��100%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������װ��(�г���������ȥ)�������ʵ�飬װ����ȷ���ܴﵽʵ��Ŀ�ĵ���

A. ͼ1װ������������Һ
B. ͼ2װ�÷��뱽��ȡ��ˮ���ѷֲ��ˮ�����л���
C. ͼ3װ�ý���ʯ�͵ķ���
D. ͼ4װ�ò�ȡ�Ҵ���������Ũ�����Ϲ��ȵķ�����ȡ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������Ӧ�ù㷺������˵���������( )
A. ��Ϧҹɫ�ʰ�쵵��̻������˽�������ɫ��Ӧ
B. ��������β�����ŷ��ǿ�������Σ����;��֮һ
C. �������Ƶ���Ҫ������֮һ������������θ�����
D. ��ϩ������������һ�����ҵ�ʯ�ͻ�����չˮƽ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com