
����Ŀ����A��B��C��D����ѧ��ѧ�����Ļ���������ᴿ�Ļ���װ�á�
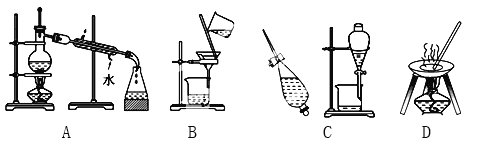
����ݻ���������ᴿ��ԭ�����ش�������ʵ������Ҫʹ����һ��װ�ã���A��B��C��D�����ʵ��Ŀո��С�
��1���ӵ�ˮ����ȡ��_____________________________��
��2��ʵ������ȡ����ˮ_____________________________��
��3��ȥ�����е���ɳ_____________________________��
��4���뺣ˮɹ��ԭ���������___________________________��
���������а������ʣ���HCl�����Cu ��CO ��CO2 �ݽ��ʯ ��KMnO4���� ��Ba(OH)2��Һ ������KAl(SO4)2
��1�����ڵ��ʵ���_________�������������������_________������״̬�ܵ���ĵ������_________��(���������ʵ����)
��2��д��Ba(OH)2��ˮ�еĵ��뷽��ʽ��____________________________________________��
��3����˫���ű�ʾ�÷�Ӧ�е���ת�Ƶķ������Ŀ_______
2KMnO4+16HCl=5Cl2��+2MnCl2+2KCl+8H2O
����0.8mol��ԭ������������ת�Ƶ��ӵ����ʵ�����_________��
���𰸡� C A B D �ڢ� �� �� Ba(OH)2=Ba2++2OH- 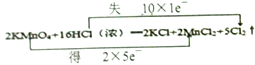 +8H2O 0.8mol
+8H2O 0.8mol
����������1�����������л��ܼ��У��ӵ�ˮ����ȡ����Ҫ��ȡ��Һ����ѡC����2��ʵ������ȡ����ˮ��Ҫ����ѡA����3��ȥ�����е���ɳ��Ҫ���ˣ���ѡB����4����ˮɹ����������ԭ������ѡD��
��1����һ��Ԫ���γɵĴ������ǵ��ʣ����ڵ��ʵ���Cu�����ʯ������Ӧ�����κ�ˮ������������������������������������CO2�����������ƶ����ӻ����ӵ����ʿ��Ե��磬�������״̬�ܵ���ĵ����������KAl(SO4)2����2��Ba(OH)2�Ƕ�Ԫǿ���ˮ�еĵ��뷽��ʽΪBa(OH)2=Ba2++2OH-����3��MnԪ�ػ��ϼ۴�+7�۽��͵�+2�۵õ�5�����ӣ�ClԪ�ػ��ϼ۴ӣ�1�����ߵ�0��ʧȥ1�����ӣ����ݵ��ӵ�ʧ�غ��֪��˫���ű�ʾ�÷�Ӧ�е���ת�Ƶķ������ĿΪ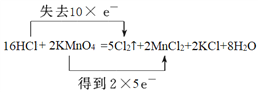 �����ݷ���ʽ��֪����0.8mol��ԭ������������ת�Ƶ��ӵ����ʵ�����0.8mol��
�����ݷ���ʽ��֪����0.8mol��ԭ������������ת�Ƶ��ӵ����ʵ�����0.8mol��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҩ�ǰѲݵijɷ�֮һM��������ɱ�����ã�M�Ľṹ��ͼ��ʾ������������ȷ���ǣ� �� 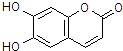
A.M����Է���������180
B.1mol M�������2mol Br2������Ӧ
C.M��������NaOH��Һ������Ӧʱ�������л�����Ļ�ѧʽΪC9H4O5Na4
D.1mol M������NaHCO3��Ӧ������2mol CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���ӷ�Ӧ�漰H2O��Cr2O72-��NO2-��H+��NO3-��Cr3+����������֪��Ӧ������NO3-Ũ�ȱ仯��ͼ��ʾ�����������ͻ�ԭ�������ʵ���֮��Ϊ1��3�������жϴ�����ǣ� ��
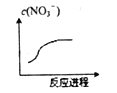
A. Cr2O72-��Cr���ϼ���+6 �� B. ��Ӧ������������NO3-
C. ����1mol��������ת�Ƶ���6mol D. ��Ӧ��Cr3+������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȼ�ϵ��Ϊ��Դ���е���ʵ��װ����ͼ��ʾ������˵������ȷ���ǣ� �� 
A.ȼ�ϵ�ع���ʱ��������Ӧ��O2+2H2O+4e���T4OH��
B.a��������b����ͭʱ��b�����ܽ⣬a������ͭ����
C.a���Ǵ�ͭ��b���Ǵ�ͭʱ�����ŷ�Ӧ�Ľ���Ũ�ȼ�С
D.a��b��������ʯīʱ������ͬ������b���������������������ĵ�H2������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ��ѧ�������ֽ�������A��B��C��I�����ֳ�������ס��ҡ���������D��E��F��G��H������֮���ܷ������·�Ӧ(ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ�����)
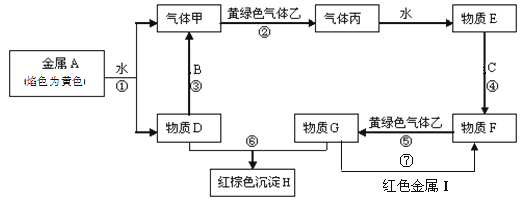
�����������Ϣ�ش��������⣺
��1��д������H�Ļ�ѧʽ��_______________������E�����ƣ�_______________��
��2��д����Ӧ�۵Ļ�ѧ����ʽ___________________��д����Ӧ�ߵ����ӷ���ʽ____________��
��3����д��ͼʾ������C��ˮ�����ڸ����·�Ӧ�Ļ�ѧ����ʽ______________��
��4������һ�ּ��鷴Ӧ�����ò����������ӵIJ���__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����( ��)
A. ������ʯ��ˮ��ͨ�������Ķ�����̼��Ca2����2OH����CO2===CaCO3����H2O
B. ��̼������Һ��ͨ�������̼��CO![]() ��CO2��H2O ===HCO3-
��CO2��H2O ===HCO3-
C. �����������ռ���Һ��Ӧ��SiO2��2OH��===SiO![]() ��H2��
��H2��
D. �Ȼ�����ʴͭ��·��:Fe3++Cu===Fe2++Cu2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺ 
��1����X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ���� ������Y���ϵĵ缫��ӦʽΪ �� ��X�������۲쵽�������� ��
��2����X��Y���Ƕ��Ե缫��a��CuSO4��Һ��X�缫�ϵĵ缫��ӦʽΪ �� ��X�������۲쵽�������� ��
��3����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����X�缫�IJ����� �� �缫��Ӧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������100mL 1.0molL��1Na2SO4��Һ����ȷ�ķ����ǣ�������
�ٽ�7.1g Na2SO4����50mLˮ��
�ڽ�32.2g Na2SO410H2O������������ˮ�У�Ȼ������ˮϡ����100mL
�۽�25mL4.0molL��1Na2SO4��Һ����75mLˮ��
�ܽ�50mL2.0molL��1Na2SO4��Һ���뵽40mLˮ�У�Ȼ������ˮϡ����100mL��
A.�٢�
B.�٢�
C.�ڢ�
D.�ڢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com