
【题目】t℃时,将3mol A和2mol B气体通入体积为2L的密闭容器中(容积不变),发生反应:3A(g) + xB(g)![]() C(g),4min时反应达到平衡状态(温度不变),剩余0.4 mol B,并测得C的浓度为0.4mol/L。请填写下列空白:
C(g),4min时反应达到平衡状态(温度不变),剩余0.4 mol B,并测得C的浓度为0.4mol/L。请填写下列空白:
(1)x=_________。
(2)用A表示该反应的速率为____________________mol/(L·min)。
(3)若继续向平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,下列说法中正确的是______________________(填写下列选项字母符号)。
A.化学平衡向正反应方向移动
B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动
D.正、逆反应的化学反应速率将发生同等程度的改变
【答案】2 0.3 C
【解析】
据三段式解题法,求出反应混合物各组分的物质的量的变化量、平衡时组分的物质的量;平衡时,C的物质的量为0.4mol/L×2L=0.8mol;
3A(g) + xB(g) ![]() C(g)
C(g)
开始 3 2 0
变化 2.4 0.8x 0.8
平衡 0.6 0.4 0.8
据以上分析解答问题。
据三段式解题法,求出反应混合物各组分的物质的量的变化量、平衡时组分的物质的量;平衡时,C的物质的量为0.4mol/L×2L=0.8mol;
3A(g) + xB(g) ![]() C(g)
C(g)
开始 3 2 0
变化 2.4 0.8x 0.8
平衡 0.6 0.4 0.8
(1)根据以上分析可知,2-0.8x=0.4,x=2;
(2)用A表示该反应的速率为[2.4mol/2L]÷4min=0.3 mol/(L·min);
(3)恒容容器中,向容器中通入少量氦气,总压增大,分压不变,不影响反应混合物各组分的浓度,正逆反应速率不变,平衡不移动,故选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将溶液(或气体)Y逐滴加入(或通入)一定量的溶液X中(下表),产生沉淀的物质的量(用纵坐标表示)与加入Y物质的量(用横坐标表示)的关系如图所示,则符合图中所示关系的一组物质是

A | B | C | D | |
X |
|
|
|
|
Y |
|
| NaOH | HCl |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,在密闭容器中,发生可逆反应2NO2(g) ![]() 2NO(g) +O2(g),达到平衡状态的标志是:
2NO(g) +O2(g),达到平衡状态的标志是:
A.单位时间生成n mol O2,同时生成2n mol NO
B.用NO2、NO、O2表示反应速率之比为2:2:1的状态
C.NO2、NO、O2的物质的量之比为2:2:1的状态
D.混合气体的颜色不再改变的状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容容器中发生N2O4(g)2NO2(g),若反应物的浓度由0.1molL﹣1降到0.06molL﹣1需20s,那么由0.06molL﹣1降到0.036molL﹣1,所需反应时间为( )
A. 10 sB. 12 sC. 大于12 sD. 小于12 s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)![]() C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
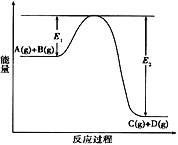
(1)该反应是___________反应(填“吸热”“放热”)。
(2)当反应达到平衡时,升高温度,A的转化率______(填“增大”、“减小”或“不变”),原因_____。
(3)反应体系中加入催化剂对反应热是否有影响?_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温时CH3COOH的电离平衡常数为K。该温度下向20 mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中错误的是( )
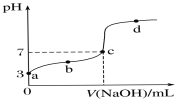
A.a点表示的溶液中c(H+)等于10-3 mol·L-1
B.b点表示的溶液中c(CH3COO-)>c(Na+)
C.c点表示CH3COOH和NaOH恰好反应完全
D.b、d点表示的溶液中![]() 均等于K
均等于K
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】潮湿环境、C1-、溶解氧是造成青铜器锈蚀的主要环境因素,腐蚀严重的青铜器表面大多存在起催化作用的多孔催化层。如图为青铜器发生电化学腐蚀的原理示意图,下列说法正确的是( )

A.腐蚀过程中,青铜基体是正极
B.若有64 g Cu腐蚀,理论上消耗氧气的体积为11.2 L(标准状况)
C.多孔催化层的形成加速了青铜器的腐蚀速率,是因为改变了反应的焓变
D.环境中的C1-、正负极产物作用生成多孔粉状锈,其离子方程式为2Cu2++3OH-+C1-=Cu2(OH)3C1↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海南粗榧新碱是从植物中提取的、具有边缘抗肿瘤活性的生物碱,合成该碱的一种常见中间体G的合成线路如图:
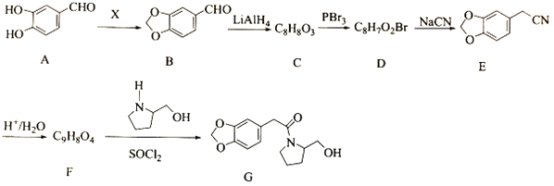
已知:①R—COOH+R’—OH ![]()
![]() +H2O
+H2O
②R—CN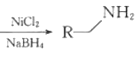
回答下列问题:
(1)X为醛类物质,其名称为_________。
(2)B→C的反应类型为_________。
(3)D→E的反应方程式为_________。
(4)化合物F的结构简式为_________。
(5)有机物Y是A的同分异构体,满足下列条件的Y还有_________种。
①能与FeC13溶液发生显色反应
②1 mo1 Y与足量金属Na反应生成1 mo1 H2
③结构中含“![]() ”
”
其中核磁共振氢谱显示为4组峰,且峰面积比为2:2:1:1的物质为_________(写出其中一种结构简式)。
(6)设计以![]() 为起始原料制备
为起始原料制备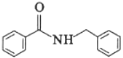 的合成线路__________(无机试剂任选)。
的合成线路__________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将氨气通入水中,发生化学反应的方程式有_______;下列有关分析中正确的是_______;
A.常温时氨气易溶于水
B.通常情况下氨气在水中的溶解度不大
C.溶于水的氨气分子有少量发生电离
D.氨水中的NH3H2O可电离出少量OH-
E.氨本身具有弱碱性
F.在饱和氨水中含量最多的溶质是NH3H2O
(2)氨水有许多用途,请任写一个用氨水制取不溶性碱的方程式_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com